下列是德国化学家哈伯工业合成氨的流程图,其中为提高原料转化率和增大反应速率而采取的措施是
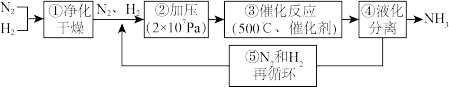
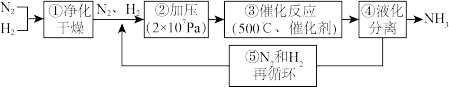
| A.①②③ | B.②④⑤ | C.②③ | D.②⑤ |
更新时间:2021-10-21 23:50:43
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】稀硫酸与过量锌粉反应,为减缓反应速率,且不影响生成氢气的总量,可加入的物质是:
①水②Na2CO3溶液③Na2SO4溶液④CH3COONa溶液⑤少量K2SO4固体⑥几滴CuSO4溶液
①水②Na2CO3溶液③Na2SO4溶液④CH3COONa溶液⑤少量K2SO4固体⑥几滴CuSO4溶液
| A.①②⑥ | B.②③④ | C.①③④ | D.③④⑤ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在2L恒温密闭容器中通入气体X并发生反应: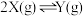 (正反应放热),X的物质的量
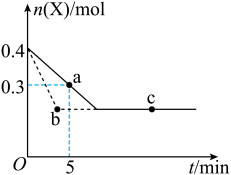
(正反应放热),X的物质的量 随时间t变化的曲线如图所示(图中的两条曲线分别代表有、无催化剂的情形),下列叙述不正确的是
随时间t变化的曲线如图所示(图中的两条曲线分别代表有、无催化剂的情形),下列叙述不正确的是
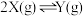 (正反应放热),X的物质的量
(正反应放热),X的物质的量 随时间t变化的曲线如图所示(图中的两条曲线分别代表有、无催化剂的情形),下列叙述不正确的是
随时间t变化的曲线如图所示(图中的两条曲线分别代表有、无催化剂的情形),下列叙述不正确的是
| A.反应进行到a点时放出的热量多于反应进行到b点时放出的热量 |
| B.虚线表示使用催化剂的情形 |
C.反应从开始到a点的平均反应速率可表示为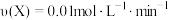 |
| D.b、c两点表明反应在相应的条件下达到了最大限度 |
您最近一年使用:0次
【推荐3】以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程如图所示。
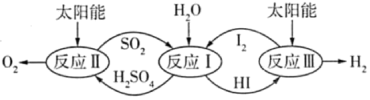
相关反应的热化学方程式为:
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) ∆H1=-213kJ·mol-1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+ O2(g) ∆H2=+327kJ·mol-1
O2(g) ∆H2=+327kJ·mol-1
反应Ⅲ:2HI(aq)=H2(g)+I2(g) ∆H3=+172kJ·mol-1
下列说法正确的是

相关反应的热化学方程式为:
反应Ⅰ:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) ∆H1=-213kJ·mol-1
反应Ⅱ:H2SO4(aq)=SO2(g)+H2O(l)+
 O2(g) ∆H2=+327kJ·mol-1
O2(g) ∆H2=+327kJ·mol-1 反应Ⅲ:2HI(aq)=H2(g)+I2(g) ∆H3=+172kJ·mol-1
下列说法正确的是
| A.该过程降低了水分解制氢的活化能,使总反应的∆H 降低 |
| B.该过程实现了化学能到太阳能的转化 |
| C.H2O、SO2和I2都对总反应起到了催化作用 |
| D.总反应的热化学方程式为2H2O(l)=2H2(g)+O2(g) ∆H =+572kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】可逆反应:mA(s)+nB(g)⇌eC(g)+fD(g),在反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图1图2所示.下列叙述正确的是( )
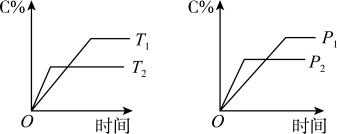
图1 图2

图1 图2
| A.达到平衡后,若升高温度,平衡向逆反应方向移动 |
| B.达到平衡后,增加A的量有利于平衡向正反应方向移动 |
| C.达到平衡后,加入催化剂则C%增大 |
| D.化学方程式中n>e+f |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】m A+n B  p C+q D,该反应在其它条件不变的情况下,以T1和T2表示不同温度,Ⅰ表示T1时的平衡状态,Ⅱ表示T2时的平衡状态,则下列叙述符合图示的是
p C+q D,该反应在其它条件不变的情况下,以T1和T2表示不同温度,Ⅰ表示T1时的平衡状态,Ⅱ表示T2时的平衡状态,则下列叙述符合图示的是

 p C+q D,该反应在其它条件不变的情况下,以T1和T2表示不同温度,Ⅰ表示T1时的平衡状态,Ⅱ表示T2时的平衡状态,则下列叙述符合图示的是
p C+q D,该反应在其它条件不变的情况下,以T1和T2表示不同温度,Ⅰ表示T1时的平衡状态,Ⅱ表示T2时的平衡状态,则下列叙述符合图示的是
| A.正反应是吸热反应 | B.T1>T2 |
| C.逆反应是放热反应 | D.T2>T1 |
您最近一年使用:0次




