下列说法不正确的是
| A.自发进行的反应不需要任何条件,就可以发生反应 |
| B.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
| C.一个化学反应能否实际进行,除了要考虑反应的自发性,还应该考虑反应速率 |
D. 、 、 的反应在任何温度下都能自发进行 的反应在任何温度下都能自发进行 |
更新时间:2021-11-08 21:14:50
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
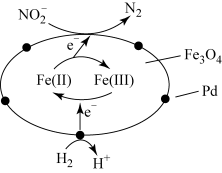
【推荐1】科学家研制出了一种在催化剂作用下用 处理废水中
处理废水中 的方法,该过程的反应原理如图所示。下列说法正确的是
的方法,该过程的反应原理如图所示。下列说法正确的是
 处理废水中
处理废水中 的方法,该过程的反应原理如图所示。下列说法正确的是
的方法,该过程的反应原理如图所示。下列说法正确的是
A.反应过程中不需要补充 |
| B.处理后的废水酸性增强 |
| C.处理过程中的催化剂只有Pd |
D.该过程中每消耗 ,同时生成 ,同时生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列图示所得出的结论正确的是
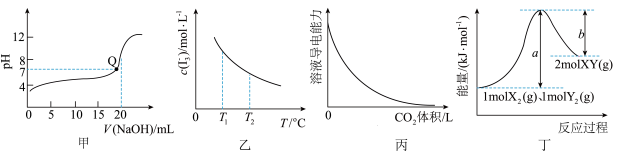

| A.图甲是常温下用0.1000mol/LNaOH溶液滴定20.00mL0.1000mol/LCH3COOH溶液的滴定曲线,Q点表示酸碱中和滴定终点 |
B.图乙是I2+I-  中 中 的平衡浓度随温度变化的曲线,说明平衡常数K(T1)<K(T2) 的平衡浓度随温度变化的曲线,说明平衡常数K(T1)<K(T2) |
| C.图丙表示CO2通入饱和Na2CO3溶液中,溶液导电能力的变化 |
| D.图丁是1molX2(g)、1molY2(g)反应生成2molXY(g)的能量变化曲线,a表示1molX2(g)、1molY2(g)变成气态原子过程中吸收的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,在1L恒容密闭容器中加入lmol的N2(g)和3molH2(g)发生反应:N2(g)+3H2(g)  2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法
2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法不正确 的是
 2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法
2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法| 时间(min) | 0 | t1 | t2 | t3 |
| NH3物质的量(mol) | 0 | 0.2 | 0.3 | 0.3 |
| A.0~t1min,v(NH3)=0.2/t1mol·L-1·min-1 |
| B.t3时再加入1mol的N2(g)和3molH2(g),反应达新平衡时,c(N2)>0.85mol·L-1 |
C.N2(g)+3H2(g)  2NH3(g)的活化能小于2NH3(g) 2NH3(g)的活化能小于2NH3(g)  N2(g)+3H2(g)的活化能 N2(g)+3H2(g)的活化能 |
| D.升高温度,可使正反应速率减小,逆反应速率增大,故平衡逆移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列措施肯定能使化学反应速率增大的是
| A.增加反应物的量 | B.升高温度 | C.增大压强 | D.减小压强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用 催化还原
催化还原 ,可以消除氮氧化物的污染。已知:
,可以消除氮氧化物的污染。已知:
①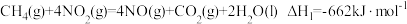
②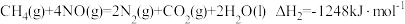
下列说法正确的是
 催化还原
催化还原 ,可以消除氮氧化物的污染。已知:
,可以消除氮氧化物的污染。已知:①
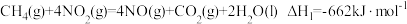
②
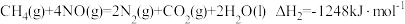
下列说法正确的是
| A.反应②在低温下不能自发进行 |
B.若反应①中消耗 (标准状况下) (标准状况下) ,则放出 ,则放出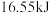 热量 热量 |
C.生成相同物质的量的 ,反应①②中转移的电子数不相同 ,反应①②中转移的电子数不相同 |
D.若用标准状况下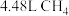 还原 还原 只生成 只生成 和 和 ,则放出的热量为 ,则放出的热量为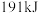 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是
| A.反应 CaCO3(s) = CaO(s) + CO2(g) △H > 0,能否自发进行与温度有关 |
| B.1 mol H2O 在不同状态时的熵值:S[H2O(s)] < S[H2O(g)] |
| C.反应 NH3(g) + HCl(g) = NH4Cl(s)在室温下可自发进行,则该反应的△H < 0 |
| D.恒温恒压下,△H < 0 且△S > 0 的反应一定不能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列说法正确的是
A.恒温恒压条件下,通入稀有气体,可以提高 的反应速率 的反应速率 |
| B.使用催化剂,能降低反应的活化能,增大反应物的平衡转化率 |
C.某反应的 , , ,则低温条件下可自发进行 ,则低温条件下可自发进行 |
D.C(石墨,s)=C(金刚石,s);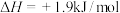 ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
您最近一年使用:0次

 R(s),对此反应来说,下列能影响其反应速率的因素是:①温度②压强③生成物的浓度
R(s),对此反应来说,下列能影响其反应速率的因素是:①温度②压强③生成物的浓度 

