回答下列问题:
(1)将 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是_______ (写化学式)。
(2)已知草酸是二元弱酸,常温下测得0.1 mol/L的 的pH为4.8,则此
的pH为4.8,则此 溶液中
溶液中
_______  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
(3)某小组同学探究饱和NaClO和 溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和
溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和 溶液,产生大量的白色胶状沉淀。出现上述现象的原因是
溶液,产生大量的白色胶状沉淀。出现上述现象的原因是_______ (请用反应的离子方程式表示)。
(4) 、
、 两种温度下
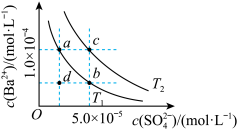
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
①
_______  (填“>”“<”或“=”),
(填“>”“<”或“=”), 温度时
温度时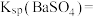
_______ 。
②根据 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是_______ (填标号)。
A.加入 固体可由a点变为b点
固体可由a点变为b点
B. 温度下,在
温度下,在 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成
C.蒸发溶剂可能由d点变为 曲线上a、b之间(不含a、b)的某一点
曲线上a、b之间(不含a、b)的某一点
D.升温可由b点变为d点
③ 温度时,现有0.2mol的
温度时,现有0.2mol的 沉淀,每次用1L饱和
沉淀,每次用1L饱和 溶液(浓度为1.7 mol/L)处理。若使
溶液(浓度为1.7 mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理_______ 次。[提示: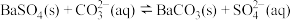 ,
, ,
,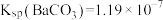 ]
]
(1)将
 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是(2)已知草酸是二元弱酸,常温下测得0.1 mol/L的
 的pH为4.8,则此
的pH为4.8,则此 溶液中
溶液中
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。(3)某小组同学探究饱和NaClO和
 溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和
溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和 溶液,产生大量的白色胶状沉淀。出现上述现象的原因是
溶液,产生大量的白色胶状沉淀。出现上述现象的原因是(4)
 、
、 两种温度下
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题。
①

 (填“>”“<”或“=”),
(填“>”“<”或“=”), 温度时
温度时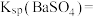
②根据
 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是A.加入
 固体可由a点变为b点
固体可由a点变为b点B.
 温度下,在
温度下,在 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成C.蒸发溶剂可能由d点变为
 曲线上a、b之间(不含a、b)的某一点
曲线上a、b之间(不含a、b)的某一点D.升温可由b点变为d点
③
 温度时,现有0.2mol的
温度时,现有0.2mol的 沉淀,每次用1L饱和
沉淀,每次用1L饱和 溶液(浓度为1.7 mol/L)处理。若使
溶液(浓度为1.7 mol/L)处理。若使 中的
中的 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理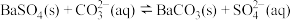 ,
, ,
,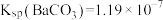 ]
]
更新时间:2021-11-12 20:06:30
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】以硫酸厂矿渣(含Fe2O3、α-Al2O3、SiO2等)为原料制备铁黄( )的一种工艺流程如图所示:
)的一种工艺流程如图所示:
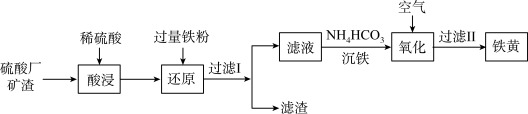
资料:i.α-Al2O3化学性质极不活泼,不溶于水也不溶于酸或碱。
ii. ;
;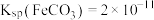 。
。
回答下列问题:
(1)为了提高“酸浸”的效率可以采用的措施有(写出其中两种)___________ 。
(2)“还原”过程中的离子方程式为___________ 。
(3)“滤渣”中主要成分为(填化学式)___________ 。
(4)①“沉铁”过程中有 气体产生,反应的离子方程式为
气体产生,反应的离子方程式为___________ 。
②“沉铁”过程中往往有副产物 生成,分析原因是
生成,分析原因是___________ 。
③若用 “沉铁”,则无副产物
“沉铁”,则无副产物 产生,当反应完成时,溶液中
产生,当反应完成时,溶液中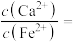
___________ 。
(5)写出氧化过程生成铁黄的化学方程式为___________ 。
(6)利用制备的铁黄进行如图实验:

①加入氯水后颜色加深的原因可能是:___________ 。
②某同学发现实验中加入过量新制氯水,放置一段时间后,深红色会逐渐褪去,褪色后的溶液中继续滴加 溶液,又出现红色,则褪色的原因可能是
溶液,又出现红色,则褪色的原因可能是___________ 。
 )的一种工艺流程如图所示:
)的一种工艺流程如图所示:
资料:i.α-Al2O3化学性质极不活泼,不溶于水也不溶于酸或碱。
ii.
 ;
;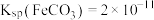 。
。回答下列问题:
(1)为了提高“酸浸”的效率可以采用的措施有(写出其中两种)
(2)“还原”过程中的离子方程式为
(3)“滤渣”中主要成分为(填化学式)
(4)①“沉铁”过程中有
 气体产生,反应的离子方程式为
气体产生,反应的离子方程式为②“沉铁”过程中往往有副产物
 生成,分析原因是
生成,分析原因是③若用
 “沉铁”,则无副产物
“沉铁”,则无副产物 产生,当反应完成时,溶液中
产生,当反应完成时,溶液中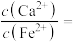
(5)写出氧化过程生成铁黄的化学方程式为
(6)利用制备的铁黄进行如图实验:

①加入氯水后颜色加深的原因可能是:
②某同学发现实验中加入过量新制氯水,放置一段时间后,深红色会逐渐褪去,褪色后的溶液中继续滴加
 溶液,又出现红色,则褪色的原因可能是
溶液,又出现红色,则褪色的原因可能是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
真题
【推荐2】甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙丁戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和。甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M。
请回答下列问题
(1)戊离子的结构示意图为_______ 。
(2)写出乙的单质的电子式:_______ 。
(3)戊的单质与X反应生成的Y和Z的物质的量之比为2 :4,反应中被氧化的物质与被还原的物质的物质的量之比为________ 。
(4)写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:_________ 。
(5)按右图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:_______ 。将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的现象是__________ 。

请回答下列问题
(1)戊离子的结构示意图为
(2)写出乙的单质的电子式:
(3)戊的单质与X反应生成的Y和Z的物质的量之比为2 :4,反应中被氧化的物质与被还原的物质的物质的量之比为
(4)写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:
(5)按右图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】以含锂的电解铝废渣(主要含AlF3、NaF、LiF、CaO)和浓硫酸为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如下:

已知:LiOH易溶于水,Li2CO3微溶于水。回答下列问题:
(1)碱解反应中,同时得到气体和沉淀,反应的离子方程式为________ 。
(2)上述流程得到的副产品冰晶石的化学方程式________ 。
(3)电池级Li2CO3可由高纯度LiOH转化而来。将电池级Li2CO3和C、FePO4高温下反应,生成LiFePO4和一种可燃性气体,该反应的化学方程式为______ 。

已知:LiOH易溶于水,Li2CO3微溶于水。回答下列问题:
(1)碱解反应中,同时得到气体和沉淀,反应的离子方程式为
(2)上述流程得到的副产品冰晶石的化学方程式
(3)电池级Li2CO3可由高纯度LiOH转化而来。将电池级Li2CO3和C、FePO4高温下反应,生成LiFePO4和一种可燃性气体,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】锶( )是第五周期ⅡA族元素。自然界中的锶存在于天青石中,天青石的主要成分为
)是第五周期ⅡA族元素。自然界中的锶存在于天青石中,天青石的主要成分为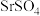 和少量
和少量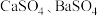 。以天青石为原料制备高纯
。以天青石为原料制备高纯 需要两个步骤。
需要两个步骤。
【步骤一】从天青石到粗 :
:
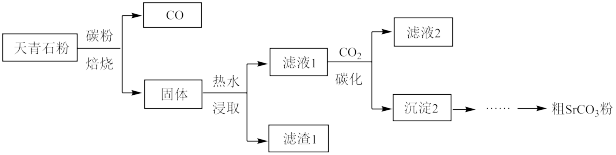
已知:ⅰ、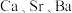 硫化物(
硫化物( )和硫氢化物
)和硫氢化物 均易溶于水。
均易溶于水。
ⅱ、 时,
时,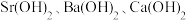 的溶解度(g)分别为1.77、3.89、0.173;
的溶解度(g)分别为1.77、3.89、0.173;
 时,
时,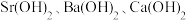 的溶解度(g)分别为20.2、101.4、0.094.
的溶解度(g)分别为20.2、101.4、0.094.
(1)焙烧过程中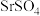 转化为
转化为 的化学方程式是
的化学方程式是___________ 。
(2)浸取时发生反应: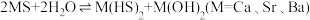 。使用热水有利于提高
。使用热水有利于提高 的平衡转化率,原因是
的平衡转化率,原因是___________ 。
(3)滤渣1的主要成分是___________ 。
【步骤二】粗 转化为高纯
转化为高纯 :
:
(4)粗 中的杂质是
中的杂质是 。有同学提出可以将粗
。有同学提出可以将粗 产物溶于酸,再加入
产物溶于酸,再加入 溶液实现
溶液实现 和
和 的分离。设
的分离。设 完全沉淀时
完全沉淀时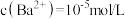 ,则溶液中
,则溶液中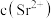 一定不大于
一定不大于___________  。此时会有
。此时会有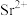 沉淀,该方案不合理。
沉淀,该方案不合理。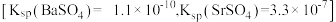
(5)实际的除杂和转化流程如下图所示:
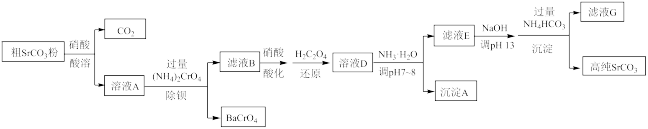
已知:ⅰ、溶液中存在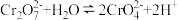 ,
,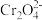 具有强氧化性。
具有强氧化性。
ⅱ、 是两性氢氧化物,难溶于水,
是两性氢氧化物,难溶于水,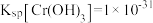 。
。
①若酸溶过程中 过量太多,则除钡过程中
过量太多,则除钡过程中 去除率会下降,请从化学平衡移动角度解释原因
去除率会下降,请从化学平衡移动角度解释原因___________ 。
②还原过程中草酸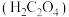 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
③为除铬,向溶液D中加入 调节
调节 为7~8.此过程不调节
为7~8.此过程不调节 为13的原因是
为13的原因是___________ 。
④加入 溶液生成高纯
溶液生成高纯 的离子方程式为
的离子方程式为___________
 )是第五周期ⅡA族元素。自然界中的锶存在于天青石中,天青石的主要成分为
)是第五周期ⅡA族元素。自然界中的锶存在于天青石中,天青石的主要成分为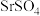 和少量
和少量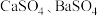 。以天青石为原料制备高纯
。以天青石为原料制备高纯 需要两个步骤。
需要两个步骤。【步骤一】从天青石到粗
 :
:
已知:ⅰ、
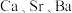 硫化物(
硫化物( )和硫氢化物
)和硫氢化物 均易溶于水。
均易溶于水。ⅱ、
 时,
时,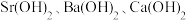 的溶解度(g)分别为1.77、3.89、0.173;
的溶解度(g)分别为1.77、3.89、0.173; 时,
时,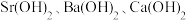 的溶解度(g)分别为20.2、101.4、0.094.
的溶解度(g)分别为20.2、101.4、0.094.(1)焙烧过程中
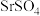 转化为
转化为 的化学方程式是
的化学方程式是(2)浸取时发生反应:
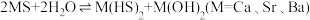 。使用热水有利于提高
。使用热水有利于提高 的平衡转化率,原因是
的平衡转化率,原因是(3)滤渣1的主要成分是
【步骤二】粗
 转化为高纯
转化为高纯 :
:(4)粗
 中的杂质是
中的杂质是 。有同学提出可以将粗
。有同学提出可以将粗 产物溶于酸,再加入
产物溶于酸,再加入 溶液实现
溶液实现 和
和 的分离。设
的分离。设 完全沉淀时
完全沉淀时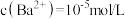 ,则溶液中
,则溶液中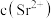 一定不大于
一定不大于 。此时会有
。此时会有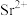 沉淀,该方案不合理。
沉淀,该方案不合理。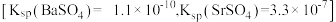
(5)实际的除杂和转化流程如下图所示:

已知:ⅰ、溶液中存在
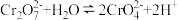 ,
,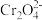 具有强氧化性。
具有强氧化性。ⅱ、
 是两性氢氧化物,难溶于水,
是两性氢氧化物,难溶于水,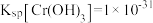 。
。①若酸溶过程中
 过量太多,则除钡过程中
过量太多,则除钡过程中 去除率会下降,请从化学平衡移动角度解释原因
去除率会下降,请从化学平衡移动角度解释原因②还原过程中草酸
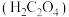 发生反应的离子方程式为
发生反应的离子方程式为③为除铬,向溶液D中加入
 调节
调节 为7~8.此过程不调节
为7~8.此过程不调节 为13的原因是
为13的原因是④加入
 溶液生成高纯
溶液生成高纯 的离子方程式为
的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】某废钒渣(主要成分为 ,含有少量
,含有少量 、CaO)为原料生产
、CaO)为原料生产 的工艺流程如图:
的工艺流程如图:
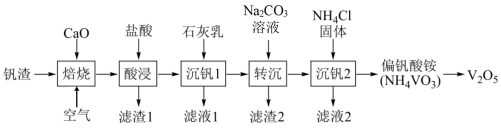
已知: 难溶于水,可溶于盐酸;
难溶于水,可溶于盐酸; 难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如下表。
难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如下表。
(1)①“酸浸”时与HCl反应的物质除了 、CaO外,还有
、CaO外,还有_______ 。
②“酸浸”后溶液pH约为4,加石灰乳后pH略大于12,则“沉钒1”时沉钒化学方程式为:_______ 。
(2)①“沉钒2”的沉钒率随温度的变化如图所示,温度高于80℃沉钒率下降的原因是_______ 。
②“沉钒2”得到偏钒酸铵( ),若“转沉”后过滤得滤液调节pH后体积为2L,
),若“转沉”后过滤得滤液调节pH后体积为2L,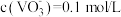 ,为使钒元素的沉降率达到98%,至少应加入
,为使钒元素的沉降率达到98%,至少应加入
_______ mol。(加入 前后溶液体积不变;
前后溶液体积不变;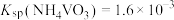 )
)

(3)400℃时,在空气中偏钒酸铵加热分解制备五氧化二钒,分解一段时间后,气体中先检测到 ,随后固体中检测到了
,随后固体中检测到了 杂质,不断搅拌充分反应后,最终无该杂质。该反应过程可描述为
杂质,不断搅拌充分反应后,最终无该杂质。该反应过程可描述为_______ 。
 ,含有少量
,含有少量 、CaO)为原料生产
、CaO)为原料生产 的工艺流程如图:
的工艺流程如图:
已知:
 难溶于水,可溶于盐酸;
难溶于水,可溶于盐酸; 难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如下表。
难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如下表。| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |
 、CaO外,还有
、CaO外,还有②“酸浸”后溶液pH约为4,加石灰乳后pH略大于12,则“沉钒1”时沉钒化学方程式为:
(2)①“沉钒2”的沉钒率随温度的变化如图所示,温度高于80℃沉钒率下降的原因是
②“沉钒2”得到偏钒酸铵(
 ),若“转沉”后过滤得滤液调节pH后体积为2L,
),若“转沉”后过滤得滤液调节pH后体积为2L,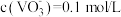 ,为使钒元素的沉降率达到98%,至少应加入
,为使钒元素的沉降率达到98%,至少应加入
 前后溶液体积不变;
前后溶液体积不变;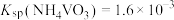 )
)
(3)400℃时,在空气中偏钒酸铵加热分解制备五氧化二钒,分解一段时间后,气体中先检测到
 ,随后固体中检测到了
,随后固体中检测到了 杂质,不断搅拌充分反应后,最终无该杂质。该反应过程可描述为
杂质,不断搅拌充分反应后,最终无该杂质。该反应过程可描述为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】2022北京冬奥会期间的交通服务用车中,氢燃料电车占了绝大多数。氢氧燃料电池中,贵金属Pt作为催化剂起到关键作用。下列是从某阳极泥中回收铂、金的工艺流程图,请仔细阅读信息后作答:
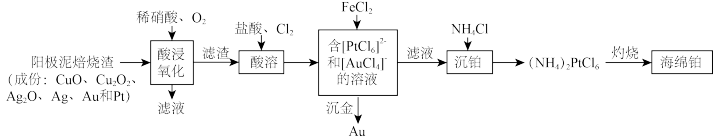
(1)“酸浸氧化”中无气体排出,此时通入氧气的目的是____ ,“滤液”中的金属阳离子有____ 。
(2)若“酸溶”得到的[PtCl6]2-和[AuCl4]-的物质的量均为1mol,则消耗的氯气至少为___________ mol。
(3)沉金过程中的离子反应方程式为___________ 。
(4)“沉铂”中,生成(NH4)2PtCl6的沉淀率随温度升高而呈升高趋势,请结合化学反应方程式解释升高温度,(NH4)2PtCl6沉淀率升高的主要原因___________ 。
(5)滤渣氯铂酸铵[(NH4)2PtCl6]表面有大量氯化铵等可溶性的盐,需要洗涤除去,洗涤沉淀的方法是___________ 。
(6)写出(NH4)2PtCl6灼烧时的化学反应方程式___________ 。

(1)“酸浸氧化”中无气体排出,此时通入氧气的目的是
(2)若“酸溶”得到的[PtCl6]2-和[AuCl4]-的物质的量均为1mol,则消耗的氯气至少为
(3)沉金过程中的离子反应方程式为
(4)“沉铂”中,生成(NH4)2PtCl6的沉淀率随温度升高而呈升高趋势,请结合化学反应方程式解释升高温度,(NH4)2PtCl6沉淀率升高的主要原因
(5)滤渣氯铂酸铵[(NH4)2PtCl6]表面有大量氯化铵等可溶性的盐,需要洗涤除去,洗涤沉淀的方法是
(6)写出(NH4)2PtCl6灼烧时的化学反应方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】“刀片电池”通过结构创新,大大提升了磷酸铁锂电池的能量密度。以下是以磷矿石(主要成分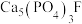 ,还有
,还有 、
、 ,等杂质)为原料生产白磷(
,等杂质)为原料生产白磷( )同时制得刀片电池正极材料
)同时制得刀片电池正极材料 的工艺流程:
的工艺流程:
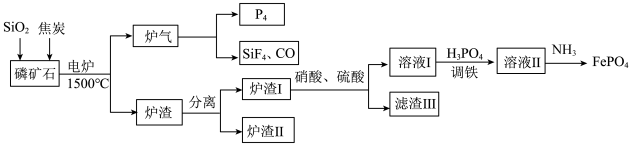
已知: 可溶于强酸性溶液。
可溶于强酸性溶液。
回答下列问题:
(1)白磷( )不溶于水但易溶于二硫化碳,说明
)不溶于水但易溶于二硫化碳,说明 是
是___________ (填“极性分子”或“非极性分子”)。
(2)炉渣Ⅰ主要含有铁单质及铁的磷化物,写出其中 溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:
溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:___________ 。
(3)炉渣Ⅱ的主要成分是___________ 。
(4)“调铁”后须向“溶液Ⅱ”中通入氨气调节溶液的pH,将pH值控制在2.0的原因是___________ 。若此条件下 恰好完全转化为
恰好完全转化为 沉淀(当溶液中某离子浓度
沉淀(当溶液中某离子浓度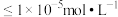 时,可视为该离子沉淀完全),求此时溶液中
时,可视为该离子沉淀完全),求此时溶液中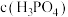 =
=___________ 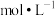 (已知
(已知 的
的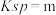 ;
; 的电离平衡常数为:
的电离平衡常数为: ,
,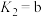 ,
,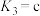 )。
)。
(5)储氢技术是目前化学家研究的热点之一;铁与镁形成的某种合金可用于储氢领域,其晶胞如图所示:
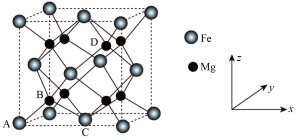
其中A的原子坐标参数为(0,0,0),B为( ,
, ,
, ),C为(
),C为( ,
, ,0),则D点的坐标参数为
,0),则D点的坐标参数为___________ 。该晶胞沿体对角线方向的投影图为___________ 。
A.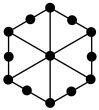 B.
B.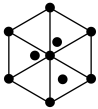 C.
C.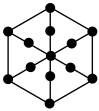 D.
D.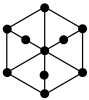
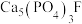 ,还有
,还有 、
、 ,等杂质)为原料生产白磷(
,等杂质)为原料生产白磷( )同时制得刀片电池正极材料
)同时制得刀片电池正极材料 的工艺流程:
的工艺流程:
已知:
 可溶于强酸性溶液。
可溶于强酸性溶液。回答下列问题:
(1)白磷(
 )不溶于水但易溶于二硫化碳,说明
)不溶于水但易溶于二硫化碳,说明 是
是(2)炉渣Ⅰ主要含有铁单质及铁的磷化物,写出其中
 溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:
溶于硝酸和硫酸的混合溶液并放出NO气体的离子方程式:(3)炉渣Ⅱ的主要成分是
(4)“调铁”后须向“溶液Ⅱ”中通入氨气调节溶液的pH,将pH值控制在2.0的原因是
 恰好完全转化为
恰好完全转化为 沉淀(当溶液中某离子浓度
沉淀(当溶液中某离子浓度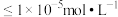 时,可视为该离子沉淀完全),求此时溶液中
时,可视为该离子沉淀完全),求此时溶液中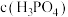 =
=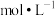 (已知
(已知 的
的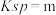 ;
; 的电离平衡常数为:
的电离平衡常数为: ,
,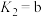 ,
,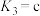 )。
)。(5)储氢技术是目前化学家研究的热点之一;铁与镁形成的某种合金可用于储氢领域,其晶胞如图所示:

其中A的原子坐标参数为(0,0,0),B为(
 ,
, ,
, ),C为(
),C为( ,
, ,0),则D点的坐标参数为
,0),则D点的坐标参数为A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备高纯硫酸锰,工艺如下图所示。回答下列问题: ]形成氢氧化物沉淀的pH范围如下:
]形成氢氧化物沉淀的pH范围如下:
(1) 的价电子排布式为
的价电子排布式为___________ ,在元素周期表中Zn处于___________ 区。
(2)提高“溶浸”速率,可采取的措施是___________ 。(答一条即可)
(3)“氧化”中添加适量的 的作用是
的作用是___________ 。
(4)“调pH”除铁和铝,溶液的pH范围应调节为___________ ~6之间。
(5)“除杂2”的目的是生成 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高, 沉淀不完全,原因是
沉淀不完全,原因是___________ 。
(6)电解酸化的硫酸锰溶液可制取二氧化锰,写出电解时阳极的电极反应式___________ 。

 ]形成氢氧化物沉淀的pH范围如下:
]形成氢氧化物沉淀的pH范围如下:| 金属离子 |  |  |  |  |  |  |  |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)
 的价电子排布式为
的价电子排布式为(2)提高“溶浸”速率,可采取的措施是
(3)“氧化”中添加适量的
 的作用是
的作用是(4)“调pH”除铁和铝,溶液的pH范围应调节为
(5)“除杂2”的目的是生成
 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高, 沉淀不完全,原因是
沉淀不完全,原因是(6)电解酸化的硫酸锰溶液可制取二氧化锰,写出电解时阳极的电极反应式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】稀土元素钪( )广泛应用于航空航天、超导、激光、核能等领域,从钛白水解工业废酸(含
)广泛应用于航空航天、超导、激光、核能等领域,从钛白水解工业废酸(含 、
、 、
、 、
、 、
、 等离子,
等离子, 浓度为18 mg/L)中提取氧化钪并制备三氯化钪(
浓度为18 mg/L)中提取氧化钪并制备三氯化钪( )的一种工艺流程如下:
)的一种工艺流程如下:
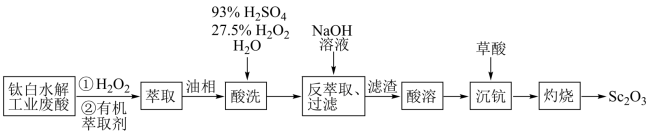
请回答下列问题:
(1)钛白水解工业废酸中加入 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的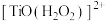 ,其中钛的化合价为
,其中钛的化合价为_______ 。
(2)钪的萃取率(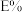 )与
)与 值[萃取剂体积(
值[萃取剂体积( )和废酸液体积(
)和废酸液体积( )之比]的关系如图,应选择最合适的
)之比]的关系如图,应选择最合适的 值为
值为_______ 。
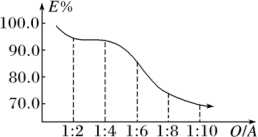
(3)酸洗步骤是为了去除油相中少量的钛。酸洗试剂是用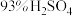 、
、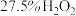 和
和 按一定比例混合而成。实验室中混合三种液体的操作是:将
按一定比例混合而成。实验室中混合三种液体的操作是:将 沿烧杯内壁慢慢注入
沿烧杯内壁慢慢注入 中,并用玻璃棒不断搅拌,冷却后再慢慢注入
中,并用玻璃棒不断搅拌,冷却后再慢慢注入 中,并不断搅拌,则
中,并不断搅拌,则 、
、 分别对应上述试剂中的
分别对应上述试剂中的_______ 、_______ 。
(4)反萃取步骤中,加入 溶液后生成
溶液后生成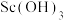 、
、 沉淀,其中,碱性条件下
沉淀,其中,碱性条件下 被
被 氧化的离子方程式为
氧化的离子方程式为_______ ;若沉淀后溶液的 为8,则残留的
为8,则残留的 浓度为
浓度为_______  。(已知:
。(已知: 时,
时,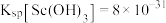 )
)
(5)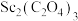 高温灼烧时只生成
高温灼烧时只生成 和
和 ,反应的化学方程式为
,反应的化学方程式为_______ 。
(6)若从 该工厂的钛白水解废酸中提取得到
该工厂的钛白水解废酸中提取得到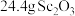 ,则钪的提取率为
,则钪的提取率为_______ (保留三位有效数字)。
 )广泛应用于航空航天、超导、激光、核能等领域,从钛白水解工业废酸(含
)广泛应用于航空航天、超导、激光、核能等领域,从钛白水解工业废酸(含 、
、 、
、 、
、 、
、 等离子,
等离子, 浓度为18 mg/L)中提取氧化钪并制备三氯化钪(
浓度为18 mg/L)中提取氧化钪并制备三氯化钪( )的一种工艺流程如下:
)的一种工艺流程如下:
请回答下列问题:
(1)钛白水解工业废酸中加入
 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的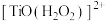 ,其中钛的化合价为
,其中钛的化合价为(2)钪的萃取率(
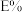 )与
)与 值[萃取剂体积(
值[萃取剂体积( )和废酸液体积(
)和废酸液体积( )之比]的关系如图,应选择最合适的
)之比]的关系如图,应选择最合适的 值为
值为
(3)酸洗步骤是为了去除油相中少量的钛。酸洗试剂是用
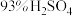 、
、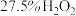 和
和 按一定比例混合而成。实验室中混合三种液体的操作是:将
按一定比例混合而成。实验室中混合三种液体的操作是:将 沿烧杯内壁慢慢注入
沿烧杯内壁慢慢注入 中,并用玻璃棒不断搅拌,冷却后再慢慢注入
中,并用玻璃棒不断搅拌,冷却后再慢慢注入 中,并不断搅拌,则
中,并不断搅拌,则 、
、 分别对应上述试剂中的
分别对应上述试剂中的(4)反萃取步骤中,加入
 溶液后生成
溶液后生成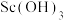 、
、 沉淀,其中,碱性条件下
沉淀,其中,碱性条件下 被
被 氧化的离子方程式为
氧化的离子方程式为 为8,则残留的
为8,则残留的 浓度为
浓度为 。(已知:
。(已知: 时,
时,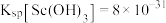 )
)(5)
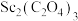 高温灼烧时只生成
高温灼烧时只生成 和
和 ,反应的化学方程式为
,反应的化学方程式为(6)若从
 该工厂的钛白水解废酸中提取得到
该工厂的钛白水解废酸中提取得到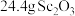 ,则钪的提取率为
,则钪的提取率为
您最近一年使用:0次



