下列事实不能用勒夏特列原理解释的是
| A.新制的氯水在光照下颜色变浅 |
B.合成氨时,加催化剂,使 和 和 在一定条件下转化为 在一定条件下转化为 |
C.由 和 和 组成的平衡体系加压后颜色先变深、后变浅 组成的平衡体系加压后颜色先变深、后变浅 |
D.增大压强,有利于 与 与 反应生成 反应生成 |
更新时间:2021-11-21 08:07:50
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】反应mA(s)+nB(g)⇌pC(g)+qD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示,下列叙述正确的是


| A.达到平衡后,加入催化剂,C%增大 |
| B.达到平衡后,若升温,平衡向左移动 |
| C.化学方程式中n<p+q |
| D.达到平衡后,增加A的量有利于平衡向右移动 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在一定条件下 和
和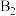 可发生反应:
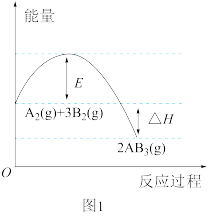
可发生反应: 。图1表示在一定温度下反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时
。图1表示在一定温度下反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时 的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物
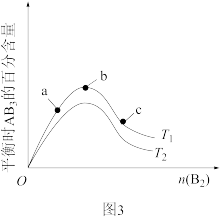
的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物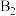 的起始物质的量对此反应平衡的影响。下列说法正确的是
的起始物质的量对此反应平衡的影响。下列说法正确的是
 和
和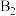 可发生反应:
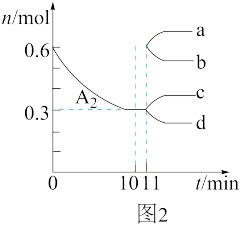
可发生反应: 。图1表示在一定温度下反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时
。图1表示在一定温度下反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时 的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物
的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物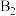 的起始物质的量对此反应平衡的影响。下列说法正确的是
的起始物质的量对此反应平衡的影响。下列说法正确的是


| A.升高温度,该反应的平衡常数增大 |
B.10min内该反应的平均速率 |
C.11min时,其他条件不变,压缩容器容积至1L,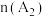 的变化趋势如图2中曲线d所示 的变化趋势如图2中曲线d所示 |
D.图3中T1<T2,a、b、c三点对应 的体积分数大小关系为: 的体积分数大小关系为: |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】一定温度下,某容器中加入足量的碳酸钙,发生反应CaCO3(s) CaO(s)+CO2(g),达到平衡,下列说法正确的是( )
CaO(s)+CO2(g),达到平衡,下列说法正确的是( )
 CaO(s)+CO2(g),达到平衡,下列说法正确的是( )
CaO(s)+CO2(g),达到平衡,下列说法正确的是( )| A.将体积缩小为原来的一半,当体系再次达到平衡时,CO2的浓度为原来的2倍 |
| B.增加CaCO3(s)的量,平衡正向移动 |
| C.将体积增大为原来的2倍,再次达到平衡时,气体的密度不变 |
| D.保持容器体积不变,充入He,平衡向逆反应方向进行 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】一定条件下,下列不能 用勒夏特列原理解释的是
| A.H2、I2、HI混合气体加压颜色变深 |
| B.NO2气体受压缩颜色先变深后变浅 |
| C.实验室用排饱和食盐水的方法收集Cl2 |
D.氨水中加酸,NH 浓度增大 浓度增大 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列事实能用勒夏特列原理解释的是
| A.实验室用排饱和食盐水法收集氯气 |
| B.加入MnO2可以加快H2O2的分解速率 |
| C.NO2与N2O4的平衡体系增大压强后颜色加深 |
| D.500°C左右比室温更有利于合成氨的反应 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列事实不能用勒夏特列原理解释的是
| A.红棕色NO2加压后颜色先变深后变浅 |
| B.实验室中常用排饱和食盐水的方法收集氯气 |
| C.SO2催化氧化成SO3的反应,使用过量的空气以提高二氧化硫的利用率 |
| D.压缩H2与I2(g)反应的平衡混合气体,颜色变深 |
您最近半年使用:0次

 HBr+HBrO,当加入AgNO3溶液并静置后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液并静置后,溶液颜色变浅 CH4(g)+H2O(g) ΔH<0,下列有关说法正确的是
CH4(g)+H2O(g) ΔH<0,下列有关说法正确的是

