纳米钴(Co)常用于CO加氢反应的催化剂:CO(g)+3H2(g) CH4(g)+H2O(g) ΔH<0,下列有关说法正确的是
CH4(g)+H2O(g) ΔH<0,下列有关说法正确的是
 CH4(g)+H2O(g) ΔH<0,下列有关说法正确的是
CH4(g)+H2O(g) ΔH<0,下列有关说法正确的是| A.纳米技术的应用,优化了催化剂的性能,提高了反应的转化率 |
| B.缩小容器体积,平衡向正反应方向移动,CO的浓度减小 |
| C.温度越低,越有利于CO催化加氢 |
| D.从平衡体系中分离出H2O(g),正反应速率减慢 |
更新时间:2021-12-01 20:24:52
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】在水溶液中,CrO 呈黄色,Cr2O
呈黄色,Cr2O 呈橙色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O
呈橙色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+,下列说法正确的是
+2H+,下列说法正确的是
 呈黄色,Cr2O
呈黄色,Cr2O 呈橙色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O
呈橙色,重铬酸钾(K2Cr2O7)在水溶液中存在以下平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+,下列说法正确的是
+2H+,下列说法正确的是| A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色 |
| B.该反应是氧化还原反应 |
| C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大 |
| D.向体系中加入少量水,平衡逆向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法正确的是
| A.升高温度,会使单位体积内分子数增多,从而加快化学反应速率 |
B. (蓝色) (蓝色)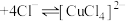 (黄色) (黄色)  , , 稀溶液受热颜色变黄 稀溶液受热颜色变黄 |
C.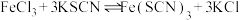 达平衡后,加入少量KCl固体,溶液红色变浅 达平衡后,加入少量KCl固体,溶液红色变浅 |
D. (橙色) (橙色) (黄色) (黄色) ,向 ,向 溶液中滴加几滴浓硫酸,溶液变为黄色 溶液中滴加几滴浓硫酸,溶液变为黄色 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】工业上用软锰矿(主要成分是MnO2,含有Al2O3、SiO2等杂质),制备KMnO4的流程如下:
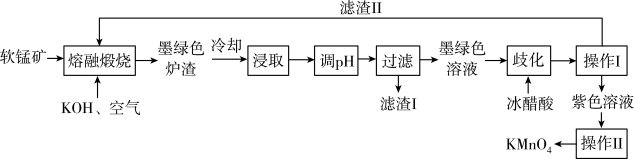
已知:K2MnO4固体和溶液均为墨绿色,溶液呈碱性,能发生可逆的歧化反应。下列说法正确的是

已知:K2MnO4固体和溶液均为墨绿色,溶液呈碱性,能发生可逆的歧化反应。下列说法正确的是
| A.向“浸取”后的溶液中通入CO2,调节其pH,经“过滤”得滤渣I,滤渣I的成分只有硅酸 |
B.“歧化”时,加入冰醋酸是为了调节溶液pH,使3MnO +2H2O +2H2O 2MnO 2MnO +MnO2+4OH-平衡正向移动,促进KMnO4的生成,提高KMnO4的产率 +MnO2+4OH-平衡正向移动,促进KMnO4的生成,提高KMnO4的产率 |
| C.“歧化”步骤中调节溶液pH时,可以用浓盐酸来代替冰醋酸 |
| D.“操作Ⅱ”时,当有大量晶体析出时,利用余热蒸干,即得紫黑色KMnO4晶体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】高温下,某反应达平衡,平衡常数K= ,恒容时,温度升高,H2浓度减小,下列说法
,恒容时,温度升高,H2浓度减小,下列说法正确 的是( )
 ,恒容时,温度升高,H2浓度减小,下列说法
,恒容时,温度升高,H2浓度减小,下列说法| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率增大,正反应速率减小 |
D.该反应的化学方程式为CO+H2O CO2+H2 CO2+H2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】在A+B C(正反应是放热反应)的反应中,如图所示,能正确表示反应速率(纵坐标)与温度(横坐标)关系的是
C(正反应是放热反应)的反应中,如图所示,能正确表示反应速率(纵坐标)与温度(横坐标)关系的是
 C(正反应是放热反应)的反应中,如图所示,能正确表示反应速率(纵坐标)与温度(横坐标)关系的是
C(正反应是放热反应)的反应中,如图所示,能正确表示反应速率(纵坐标)与温度(横坐标)关系的是A.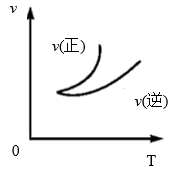 | B. |
C.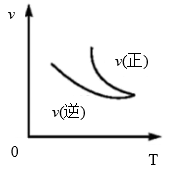 | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】乙烯气相水化法制备乙醇: 。乙烯的平衡转化率随温度、压强的变化关系如下图(起始时,
。乙烯的平衡转化率随温度、压强的变化关系如下图(起始时,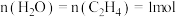 )。
)。
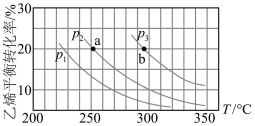
下列分析不正确的是
 。乙烯的平衡转化率随温度、压强的变化关系如下图(起始时,
。乙烯的平衡转化率随温度、压强的变化关系如下图(起始时,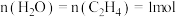 )。
)。
下列分析不正确的是
A.乙烯气相直接水化反应的 |
B.图中压强的大小关系为: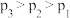 |
| C.图中a、b两点对应的化学平衡常数相等 |
D.达到平衡状态a、b所需要的时间: |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】对于已达化学平衡的下列反应:2 X (g) + Y (g)  2 Z (g) ,减小压强时,对反应产生的影响是
2 Z (g) ,减小压强时,对反应产生的影响是
 2 Z (g) ,减小压强时,对反应产生的影响是
2 Z (g) ,减小压强时,对反应产生的影响是| A.正反应速率增大,逆反应速率减小,平衡向逆反应方向移动 |
| B.正反应速率减小,逆反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】在容积不变的密闭容器中进行如下反应: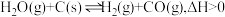 。达到平衡后,改变下列反应条件,相关叙述正确的是
。达到平衡后,改变下列反应条件,相关叙述正确的是
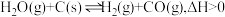 。达到平衡后,改变下列反应条件,相关叙述正确的是
。达到平衡后,改变下列反应条件,相关叙述正确的是A.加入 ,平衡正向移动,体系压强减小 ,平衡正向移动,体系压强减小 |
| B.加入少量C,正反应速率增大 |
| C.降低温度,平衡向正反应方向移动 |
D.加入 ,混合气体的密度增大 ,混合气体的密度增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列事实不能用勒夏特列原理解释的是
| A.向 Fe(SCN)3溶液中加入 KSCN 溶液,溶液颜色变深 |
| B.新制氯水在光照条件下颜色变浅 |
| C.工业上选择在温度为 400~500 ℃的条件下合成氨 |
| D.将装有 NO2 和 N2O4的混合气体的烧瓶置于热水中的颜色深于冷水中颜色 |
您最近一年使用:0次