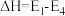一定条件下,在体积恒定的密闭容器中发生反应:N2(g)+3H2 (g) 2NH3 (g) ΔH=-QKJ·mol-1,下列说法
2NH3 (g) ΔH=-QKJ·mol-1,下列说法正确 的是
 2NH3 (g) ΔH=-QKJ·mol-1,下列说法
2NH3 (g) ΔH=-QKJ·mol-1,下列说法| A.达到平衡时反应放出的热量可能达到QkJ |
| B.升高温度,正反应速率增大,逆反应速率减小 |
| C.当混合气体的密度不再发生变化时,说明反应达到平衡状态 |
D.达到平衡时,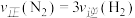 |
更新时间:2021-11-04 14:42:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法中不正确的有( )个
①反应速率用于衡量化学反应进行的快慢
②可逆反应达到化学平衡状态时,正、逆反应速率都为0
③决定反应速率的主要因素是反应物的性质
④适当增大反应物浓度,提高反应温度都能增大反应速率
⑤不管什么反应使用催化剂,都可以加快反应速率 ,并可以使平衡移动。
⑥可逆反应A(g) B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大
①反应速率用于衡量化学反应进行的快慢
②可逆反应达到化学平衡状态时,正、逆反应速率都为0
③决定反应速率的主要因素是反应物的性质
④适当增大反应物浓度,提高反应温度都能增大反应速率
⑤不管什么反应使用催化剂,都可以加快反应速率 ,并可以使平衡移动。
⑥可逆反应A(g)
 B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大
| A.2 个 | B.3 个 | C.4 个 | D.5个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】通过热分解H2S可获得氢气和单质硫,反应为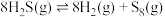 。在一定温度下,向恒容密闭容器中充入一定量的H2S进行上述反应,下列表述能判断该反应达到化学平衡状态的是
。在一定温度下,向恒容密闭容器中充入一定量的H2S进行上述反应,下列表述能判断该反应达到化学平衡状态的是
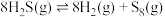 。在一定温度下,向恒容密闭容器中充入一定量的H2S进行上述反应,下列表述能判断该反应达到化学平衡状态的是
。在一定温度下,向恒容密闭容器中充入一定量的H2S进行上述反应,下列表述能判断该反应达到化学平衡状态的是A. |
| B.容器中混合气体的平均密度不再变化 |
| C.容器中混合气体总压强不再发生变化 |
| D.单位时间内,消耗1molH2S同时生成1molH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】CH4还原CO2是实现“双碳”经济的有效途径之一。相关的主要反应为CH4(g)+CO2(g) 2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
 2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是| A.低温低压 | B.低温高压 | C.高温低压 | D.高温高压 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验方案不能达到相应目的的是


| A.探究温度对化学平衡的影响 | B.研究浓度对化学平衡的影响 |
| C.实现铜棒镀银 | D.证明化学反应存在一定的限度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在某密闭容器中发生:2SO2(g)+O2(g) ⇌ 2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示。下列说法正确的是
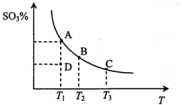

| A.在D点时v 正<v逆 |
| B.反应2SO2(g)+O2(g) ⇌2SO3(g)的∆H>0 |
| C.若B、C点的平衡常数分别为KB、KC,则KB=KC |
| D.恒温恒压下向平衡体系中通入氦气,平衡向左移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在10L密闭容器中,1moLA和3moLB在一定条件下反应:A(g)+4B(g) 2C(g),在2min后反应达到平衡时,测得混合气体共3.4moL, 则下列说法不正确的是
2C(g),在2min后反应达到平衡时,测得混合气体共3.4moL, 则下列说法不正确的是
①平衡时,物质的量之比n(A):n(B):n(C)=2:11:4
②平衡时C气体的体积分数约为11.8%
③A的转化率为20%
④平衡时B的平均反应速率为0.04moL∙L-1∙min-1
⑤温度、容积不变充入氩气平衡向右移动
⑥温度、容积不变充入A气体后B气体的转化率增大
⑦该反应若在恒温恒压的条件下充入氦气平衡向右移动
 2C(g),在2min后反应达到平衡时,测得混合气体共3.4moL, 则下列说法不正确的是
2C(g),在2min后反应达到平衡时,测得混合气体共3.4moL, 则下列说法不正确的是①平衡时,物质的量之比n(A):n(B):n(C)=2:11:4
②平衡时C气体的体积分数约为11.8%
③A的转化率为20%
④平衡时B的平均反应速率为0.04moL∙L-1∙min-1
⑤温度、容积不变充入氩气平衡向右移动
⑥温度、容积不变充入A气体后B气体的转化率增大
⑦该反应若在恒温恒压的条件下充入氦气平衡向右移动
| A.①⑤⑦ | B.②③④⑥ | C.①④⑤ | D.⑤⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】利用传感技术可探究压强对 化学平衡移动的影响。往注射器中充入适量
化学平衡移动的影响。往注射器中充入适量 气体如图甲所示;恒定温度下,再分别在
气体如图甲所示;恒定温度下,再分别在 、
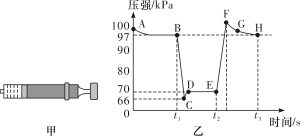
、 时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图乙所示。下列说法错误的是
时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图乙所示。下列说法错误的是
 化学平衡移动的影响。往注射器中充入适量
化学平衡移动的影响。往注射器中充入适量 气体如图甲所示;恒定温度下,再分别在
气体如图甲所示;恒定温度下,再分别在 、
、 时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图乙所示。下列说法错误的是
时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图乙所示。下列说法错误的是
A.在B、E两点,对应的正反应速率: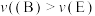 |
| B.C点到D点平衡逆向移动,针筒内气体颜色D点比B点深 |
C.B、H两点,对应的 浓度相等 浓度相等 |
| D.在E、F、H三点中,H点的气体平均相对分子质量最大 |
您最近一年使用:0次

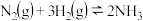
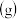 已达到平衡状态的是
已达到平衡状态的是
 分解的同时,有3个
分解的同时,有3个 的形成
的形成 的分解
的分解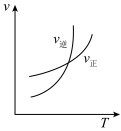
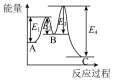
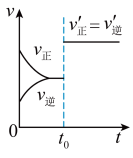
 在t1时迅速将体积缩小后
在t1时迅速将体积缩小后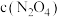 的变化
的变化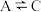 反应的
反应的