汽车尾气中的NO和CO在催化转化器中反应生成两种无毒无害的气体:
已知:碳的燃烧热为393.5 kJ/mol




则:
(1)

_______ kJ/mol。
(2)将CO和NO按 投入一恒温密闭容器,反应达平衡时,体系的总压强为a Pa、
投入一恒温密闭容器,反应达平衡时,体系的总压强为a Pa、 的体积分数为20%,该温度下反应的平衡常数
的体积分数为20%,该温度下反应的平衡常数
_______ (用平衡分压代替平衡浓度计算)。
(3)催化剂性能决定了尾气处理效果。将NO和CO以一定的流速通过两种不同的催化剂(Ⅰ、Ⅱ)进行反应,测量逸出气体中NO含量,可测算尾气脱氮率。相同时间内,脱氮率随温度变化曲线如图所示。
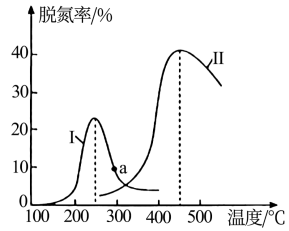
①曲线上a点的脱氮率_______ (填“>”、“<”或“=”)对应温度下的平衡脱氮率。
②催化剂Ⅱ条件下,450℃后,脱氮率随温度升高而下降的原因可能是_______ 。
(4)使用甲醇汽油能减少汽车尾气对环境的污染,某化工厂用水煤气为原料合成甲醇,恒温条件下,在体积可变的密闭容器中发生反应: ,到达平衡时,测得CO、
,到达平衡时,测得CO、 、
、 分别为1 mol、1 mol、1 mol,此时容器的体积为3 L,现往容器中继续通入3 mol CO,则v(正)
分别为1 mol、1 mol、1 mol,此时容器的体积为3 L,现往容器中继续通入3 mol CO,则v(正)_______ v(逆) (填“>”、“<”或“=”),判断的理由_______ 。
(5)二甲醚也是清洁能源,用合成气在催化剂存在下制备二甲醚的反应原理为: 。已知一定条件下,该反应中CO的平衡转化率随温度、投料比
。已知一定条件下,该反应中CO的平衡转化率随温度、投料比 的变化曲线如图:
的变化曲线如图:

①a、b、c按从小到大的顺序排序为_______ 。
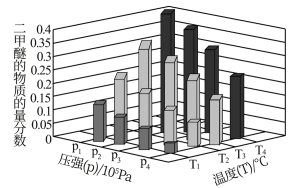
②某温度下,将2.0 mol 和4.0 mol
和4.0 mol  充入容积为2 L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中二甲醚
充入容积为2 L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中二甲醚 的物质的量分数变化情况如上图所示,在不同温度和压强下
的物质的量分数变化情况如上图所示,在不同温度和压强下 的平衡转化率最小的是
的平衡转化率最小的是_______ ;
A. 、
、 B.
B. 、
、 C.
C. 、
、 D.
D. 、
、
③在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是_______ 。
A.混合气体的平均摩尔质量变小 B.逆反应速率先增大后减小
C.化学平衡常数K值增大 D.
E.混合气体的密度减小 F.氢气的转化率减小

已知:碳的燃烧热为393.5 kJ/mol




则:
(1)


(2)将CO和NO按
 投入一恒温密闭容器,反应达平衡时,体系的总压强为a Pa、
投入一恒温密闭容器,反应达平衡时,体系的总压强为a Pa、 的体积分数为20%,该温度下反应的平衡常数
的体积分数为20%,该温度下反应的平衡常数
(3)催化剂性能决定了尾气处理效果。将NO和CO以一定的流速通过两种不同的催化剂(Ⅰ、Ⅱ)进行反应,测量逸出气体中NO含量,可测算尾气脱氮率。相同时间内,脱氮率随温度变化曲线如图所示。

①曲线上a点的脱氮率
②催化剂Ⅱ条件下,450℃后,脱氮率随温度升高而下降的原因可能是
(4)使用甲醇汽油能减少汽车尾气对环境的污染,某化工厂用水煤气为原料合成甲醇,恒温条件下,在体积可变的密闭容器中发生反应:
 ,到达平衡时,测得CO、
,到达平衡时,测得CO、 、
、 分别为1 mol、1 mol、1 mol,此时容器的体积为3 L,现往容器中继续通入3 mol CO,则v(正)
分别为1 mol、1 mol、1 mol,此时容器的体积为3 L,现往容器中继续通入3 mol CO,则v(正)(5)二甲醚也是清洁能源,用合成气在催化剂存在下制备二甲醚的反应原理为:
 。已知一定条件下,该反应中CO的平衡转化率随温度、投料比
。已知一定条件下,该反应中CO的平衡转化率随温度、投料比 的变化曲线如图:
的变化曲线如图:

①a、b、c按从小到大的顺序排序为
②某温度下,将2.0 mol
 和4.0 mol
和4.0 mol  充入容积为2 L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中二甲醚
充入容积为2 L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中二甲醚 的物质的量分数变化情况如上图所示,在不同温度和压强下
的物质的量分数变化情况如上图所示,在不同温度和压强下 的平衡转化率最小的是
的平衡转化率最小的是A.
 、
、 B.
B. 、
、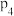 C.
C. 、
、 D.
D. 、
、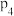
③在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是
A.混合气体的平均摩尔质量变小 B.逆反应速率先增大后减小
C.化学平衡常数K值增大 D.

E.混合气体的密度减小 F.氢气的转化率减小
更新时间:2021-11-27 08:44:29
|
相似题推荐
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐1】CO2是一种宝贵的资源,在生产、生活中有广泛的用途。同时,二氧化碳也是一种常见的温室气体,大气中CO2含量的增加是导致全球变暖的主要原因之一。为此,我国已向世界庄严承诺,力争2030年前实现碳达峰,2060年前实现碳中和。
(1)正常雨水显酸性,原因是________ 。举例说明CO2的重要用途________ (任举2例)。
(2)含碳燃料完全燃烧生成CO2。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH = 5.60, c(H2CO3)= 1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二步电离,则H2CO3
 + H+的电离常数K1=
+ H+的电离常数K1=_______ 。 (保留1位小数,已知:10-5.60 =2.5×10-6)。
(3)以CO2和NH3为原料合成尿素CO(NH2)2是固定和利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I : 2NH3(g) + CO2(g) NH2COONH4(s) △H1=-159.47 kJ·mol-1
NH2COONH4(s) △H1=-159.47 kJ·mol-1
反应II: NH2COONH4(s) CO(NH2)2(s) + H2O(g) △H2= +72.49 kJ·mol-l
CO(NH2)2(s) + H2O(g) △H2= +72.49 kJ·mol-l
请回答下列问题:
①写出CO2和NH3为原料生成尿素和气态水的热化学方程式_______ ,反应I自发进行的条件是_______ 。
②以CO2和NH3为原料合成尿素的反应中,影响CO2转化率的因素很多,图1为某特定条件下,不同水碳比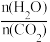 和温度影响CO2转化率变化的趋势曲线。下列说法错误的是
和温度影响CO2转化率变化的趋势曲线。下列说法错误的是_______ (填正确答案标号)。
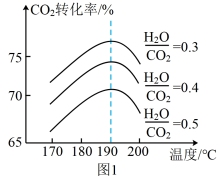
A.其他条件相同时,为提高CO2的转化率,生产中可以采取的措施是降低水碳比
B.移走部分尿素平衡向正方向移动
C.当温度低于190 °C,随温度升高CO2转化率逐渐增大,其原因可能是温度升高平衡向正方向移动
D.当温度高于190 °C后,随温度升高CO2转化率逐渐减小,其原因可能是温度升高发生了副反应
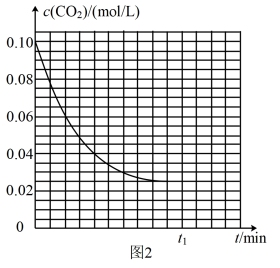
③某研究小组为探究反应I中影响c(CO2)的因素,在恒温下将0.4 mol NH3和0.2 molCO2放入容积为2L的密闭容器中,t1时达到平衡,其c(CO2)随时间t变化趋势曲线如下图2所示。则0~t1时段,用NH3表示的平均反应速率为_______ mol·L-1·min-l (用含t1的式子表示),其反应的平衡常数为______ 。(mol·L-1)-3。
(1)正常雨水显酸性,原因是
(2)含碳燃料完全燃烧生成CO2。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH = 5.60, c(H2CO3)= 1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二步电离,则H2CO3

 + H+的电离常数K1=
+ H+的电离常数K1=(3)以CO2和NH3为原料合成尿素CO(NH2)2是固定和利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I : 2NH3(g) + CO2(g)
 NH2COONH4(s) △H1=-159.47 kJ·mol-1
NH2COONH4(s) △H1=-159.47 kJ·mol-1反应II: NH2COONH4(s)
 CO(NH2)2(s) + H2O(g) △H2= +72.49 kJ·mol-l
CO(NH2)2(s) + H2O(g) △H2= +72.49 kJ·mol-l请回答下列问题:
①写出CO2和NH3为原料生成尿素和气态水的热化学方程式
②以CO2和NH3为原料合成尿素的反应中,影响CO2转化率的因素很多,图1为某特定条件下,不同水碳比
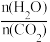 和温度影响CO2转化率变化的趋势曲线。下列说法错误的是
和温度影响CO2转化率变化的趋势曲线。下列说法错误的是
A.其他条件相同时,为提高CO2的转化率,生产中可以采取的措施是降低水碳比
B.移走部分尿素平衡向正方向移动
C.当温度低于190 °C,随温度升高CO2转化率逐渐增大,其原因可能是温度升高平衡向正方向移动
D.当温度高于190 °C后,随温度升高CO2转化率逐渐减小,其原因可能是温度升高发生了副反应
③某研究小组为探究反应I中影响c(CO2)的因素,在恒温下将0.4 mol NH3和0.2 molCO2放入容积为2L的密闭容器中,t1时达到平衡,其c(CO2)随时间t变化趋势曲线如下图2所示。则0~t1时段,用NH3表示的平均反应速率为

您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
【推荐2】N2O4和NO2的相互转化N2O4(g)⇌2NO(g)是讨 论化学平衡问题的常用体系。已知该反应在295K和315K温度下平衡常数Kp分别为0.100和0.400。将一定量的气体充入一个带活塞的特制容器,通过活塞移动使体系总压恒为lbar(lbar=100kPa)。
(1)计算295K下体系达平衡时N2O4和NO2的分压____ 。
(2)将上述体系温度升至315K,计算达平衡时N2O4和NO2的分压____ 。
(3)计算恒压下体系分别在315K和295K达平衡时的体积比及物质的量之比____ 。
(4)保持恒压条件下,不断升高温度,体系中NO2分压最大值的理论趋近值是____ (不考虑其他反应)?根据平衡关系式给出证明____ 。
(5)上述体系在保持恒外压的条件下,温度从295K升至315K,下列说法正确的是____ 。
a.平衡向左移动 b.平衡不移动 c.平衡向右移动 d.三者均有可能
(6)与体系在恒容条件下温度从295K升至315K的变化相比,恒压下体系温度升高,下列说法正确的是____ (简述理由,不要求计算)。
a.平衡移动程度更大 b.平衡移动程度更小 c.平衡移动程度不变 d.三者均有可能
(1)计算295K下体系达平衡时N2O4和NO2的分压
(2)将上述体系温度升至315K,计算达平衡时N2O4和NO2的分压
(3)计算恒压下体系分别在315K和295K达平衡时的体积比及物质的量之比
(4)保持恒压条件下,不断升高温度,体系中NO2分压最大值的理论趋近值是
(5)上述体系在保持恒外压的条件下,温度从295K升至315K,下列说法正确的是
a.平衡向左移动 b.平衡不移动 c.平衡向右移动 d.三者均有可能
(6)与体系在恒容条件下温度从295K升至315K的变化相比,恒压下体系温度升高,下列说法正确的是
a.平衡移动程度更大 b.平衡移动程度更小 c.平衡移动程度不变 d.三者均有可能
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐3】NH3是重要的化工原料,经一系列反应可得到HNO3、CO(NH2)2、HCN等产品。
(1)以氨气为原料合成HNO3工艺如下,写出N2O4转化为HNO3的反应方程式_____ 。

(2)以NH3和CO2为原料生产尿素的反应如下:
反应Ⅰ:2NH3(l) + CO2(g) NH2COONH4(l) Δ H1 = a kJ·mol-1
NH2COONH4(l) Δ H1 = a kJ·mol-1
反应Ⅱ:NH2COONH4(l) NH2CONH2(l) + H2O(l) Δ H2 = b kJ·mol-1
NH2CONH2(l) + H2O(l) Δ H2 = b kJ·mol-1
① 已知NH3(l) NH3(g) Δ H3 = c kJ·mol-1 反应2NH3(g) + CO2(g)
NH3(g) Δ H3 = c kJ·mol-1 反应2NH3(g) + CO2(g)  NH2CONH2(l) + H2O(l) Δ H4=
NH2CONH2(l) + H2O(l) Δ H4=_____ kJ·mol-1(用含a、b、c的式子表示),该反应能自发进行的主要原因是_____ 。
② 一定条件下,往恒容密闭容器中投入4 mol NH3和 1 mol CO2,测得各组分物质的量随时间变化如图1。下列说法正确的是_____ 。
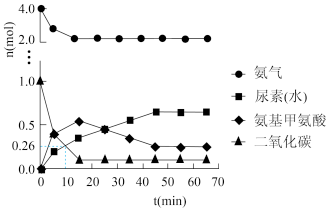
A.选择合适的碳氮比有利于提高产率
B.反应Ⅰ的活化能比反应Ⅱ小
C.过量氨气可以与反应生成的水结合,有利于尿素合成
D.气体物质的量不再变化时,反应达到平衡状态
(3)工业上利用氨气生产氢氰酸的反应为CH4(g) + NH3(g) HCN(g) + 3H2(g) Δ H>0
HCN(g) + 3H2(g) Δ H>0
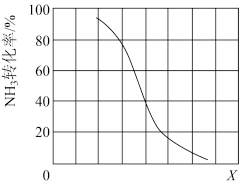
① 其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图所示。X代表的是_____ (填“温度”或“压强”)。
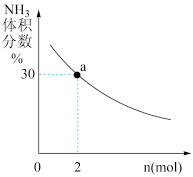
② 其它条件一定时,向2 L密闭容器中加入n mol CH4和2 mol NH3,平衡时NH3体积分数随n变化的关系如图所示。平衡常数K=_____ (请写出计算过程)
(1)以氨气为原料合成HNO3工艺如下,写出N2O4转化为HNO3的反应方程式

(2)以NH3和CO2为原料生产尿素的反应如下:
反应Ⅰ:2NH3(l) + CO2(g)
 NH2COONH4(l) Δ H1 = a kJ·mol-1
NH2COONH4(l) Δ H1 = a kJ·mol-1反应Ⅱ:NH2COONH4(l)
 NH2CONH2(l) + H2O(l) Δ H2 = b kJ·mol-1
NH2CONH2(l) + H2O(l) Δ H2 = b kJ·mol-1① 已知NH3(l)
 NH3(g) Δ H3 = c kJ·mol-1 反应2NH3(g) + CO2(g)
NH3(g) Δ H3 = c kJ·mol-1 反应2NH3(g) + CO2(g)  NH2CONH2(l) + H2O(l) Δ H4=
NH2CONH2(l) + H2O(l) Δ H4=② 一定条件下,往恒容密闭容器中投入4 mol NH3和 1 mol CO2,测得各组分物质的量随时间变化如图1。下列说法正确的是

A.选择合适的碳氮比有利于提高产率
B.反应Ⅰ的活化能比反应Ⅱ小
C.过量氨气可以与反应生成的水结合,有利于尿素合成
D.气体物质的量不再变化时,反应达到平衡状态
(3)工业上利用氨气生产氢氰酸的反应为CH4(g) + NH3(g)
 HCN(g) + 3H2(g) Δ H>0
HCN(g) + 3H2(g) Δ H>0
① 其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图所示。X代表的是

② 其它条件一定时,向2 L密闭容器中加入n mol CH4和2 mol NH3,平衡时NH3体积分数随n变化的关系如图所示。平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐1】研究氮的氧化物、硫的氧化物、碳的氧化物等大气污染物的处理具有重要意义。
(1)汽车排气管内安装的催化转化器,可使尾气中主要污染物转化为无毒物质。下列说法能说明恒温恒容条件下的反应;2NO(g)+2CO(g)=N2(g)+ 2CO2(g)△H=-746.5 kJ·mol-1已达到化学平衡的是
2CO2(g)△H=-746.5 kJ·mol-1已达到化学平衡的是 ___________________ 。
A.单位时间内消耗了2molNO的同时消耗的2molCO
B.CO与CO2的物质的量浓度相等的状态
C.气体密度保持不变的状态
D.气体平均摩尔质量保持不变的状态
(2)NO2与SO2混合可发生反应:NO2(g)+SO2(g) SO3(g)+NO(g)。
SO3(g)+NO(g)。
将一定量的NO2与SO2置于绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的趋势如图所示。由图(纵轴代表正反应速率)可知下列说法正确的是____________ (填字母)。

A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量高于生成物的总能量
D.△t1=△t2时,SO2的消耗量:a~b段大于b~c段
(3)CO在实际中有以下应用:用Li2CO3和Na2CO3熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气作为正极助燃气,制得在650℃下工作的燃料电池。完成有关的电极反应式。
负极反应式:2CO+2CO 一4e-=4CO2 正极反应式:
一4e-=4CO2 正极反应式:_______________________________ 。
(4)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol·L-1的氯化铜溶液的装置示意图:

请回答:①甲烷燃料电池的负极反应式是_________________________________________ 。
②当A中消耗0.15 mol氧气时,B中____ 极(填”a”或”b”)增重_____ g。
(1)汽车排气管内安装的催化转化器,可使尾气中主要污染物转化为无毒物质。下列说法能说明恒温恒容条件下的反应;2NO(g)+2CO(g)=N2(g)+
 2CO2(g)△H=-746.5 kJ·mol-1已达到化学平衡的是
2CO2(g)△H=-746.5 kJ·mol-1已达到化学平衡的是 A.单位时间内消耗了2molNO的同时消耗的2molCO
B.CO与CO2的物质的量浓度相等的状态
C.气体密度保持不变的状态
D.气体平均摩尔质量保持不变的状态
(2)NO2与SO2混合可发生反应:NO2(g)+SO2(g)
 SO3(g)+NO(g)。
SO3(g)+NO(g)。将一定量的NO2与SO2置于绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的趋势如图所示。由图(纵轴代表正反应速率)可知下列说法正确的是

A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量高于生成物的总能量
D.△t1=△t2时,SO2的消耗量:a~b段大于b~c段
(3)CO在实际中有以下应用:用Li2CO3和Na2CO3熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气作为正极助燃气,制得在650℃下工作的燃料电池。完成有关的电极反应式。
负极反应式:2CO+2CO
 一4e-=4CO2 正极反应式:
一4e-=4CO2 正极反应式:(4)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol·L-1的氯化铜溶液的装置示意图:

请回答:①甲烷燃料电池的负极反应式是
②当A中消耗0.15 mol氧气时,B中
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐2】研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) ΔH1=-2765.0kJ/mol
②2O2(g) +N2(g)=N2O4(l) ΔH2=-19.5kJ/mol
③H2O(g)= H2O(l) ΔH3=-44.0kJ/mol
则C2H8N2(1)+2N2O4(1)=3N2(g)+2CO2(g)+4H2O(g)的ΔH为_______ 。
(2)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g)(快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_______
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.8kJ-mol-1。实验测得:v正=k正·p2(NO)·p2(CO),v逆=k逆·p(N2)·p2(CO2)。其中k正、k逆分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数x总压)。
①达到平衡后,仅升高温度,k正增大的倍数_______ (填“大于”“小于”或“等于”)k逆增大的倍数。
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为p0kPa。达平衡时压强为0.9p0kPa,则
_______ 。
(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数Kp:
①3N2H4(1)=4NH3(g)+N2(g) ΔH1 Kp1
②4NH3(g)=2N2(g)+6H2(g) ΔH2 Kp2
绘制pKp1-T和pKp2-T的线性关系图如图所示:(已知:pKp=-1gKp)
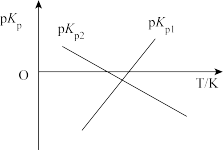
①由图可知,ΔH1_______ 0(填“>”或“<”)
②反应3N2H4(1)=3N2(g)+6H2(g)的K=_______ (用Kp1、Kp2表示);该反应的ΔH_______ 0(填“>”或“<”),写出推理过程_______
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) ΔH1=-2765.0kJ/mol
②2O2(g) +N2(g)=N2O4(l) ΔH2=-19.5kJ/mol
③H2O(g)= H2O(l) ΔH3=-44.0kJ/mol
则C2H8N2(1)+2N2O4(1)=3N2(g)+2CO2(g)+4H2O(g)的ΔH为
(2)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g)(快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_______
| A.N2O分解反应中,k值与碘蒸气浓度大小有关 |
| B.v(第二步的逆反应)<v(第三步反应) |
| C.IO为反应的催化剂 |
| D.第二步活化能比第三步大 |
①达到平衡后,仅升高温度,k正增大的倍数
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为p0kPa。达平衡时压强为0.9p0kPa,则

(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数Kp:
①3N2H4(1)=4NH3(g)+N2(g) ΔH1 Kp1
②4NH3(g)=2N2(g)+6H2(g) ΔH2 Kp2
绘制pKp1-T和pKp2-T的线性关系图如图所示:(已知:pKp=-1gKp)

①由图可知,ΔH1
②反应3N2H4(1)=3N2(g)+6H2(g)的K=
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐3】研究氮氧化物等大气污染物对打造宜居环境具有重要意义。NO在空气中存在如下反应:2NO(g)+O2(g) 2NO2(g),其反应历程分两步:
2NO2(g),其反应历程分两步:
①2NO(g) N2O2(g)(快反应) v1正=k1正·c2(NO), v1逆=k1逆·c(N2O2) ΔH1<0
N2O2(g)(快反应) v1正=k1正·c2(NO), v1逆=k1逆·c(N2O2) ΔH1<0
②N2O2(g)+O2(g) 2NO2(g)(慢反应) v2正=k2正·c(N2O2)·c(O2), v2逆=k2逆·c2(NO2) ΔH2<0
2NO2(g)(慢反应) v2正=k2正·c(N2O2)·c(O2), v2逆=k2逆·c2(NO2) ΔH2<0
反应历程的能量变化如图:
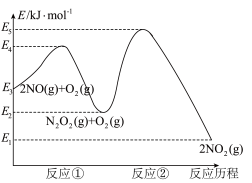
请回答下列问题:
(1)反应2NO(g)+O2(g) 2NO2(g)的ΔH
2NO2(g)的ΔH__ 0(填“>”、“<”或“=”)。
(2)决定2NO(g)+O2(g) 2NO2(g)反应速率是反应②,E4+E2
2NO2(g)反应速率是反应②,E4+E2__ E5+E3(填“>”、“<”或“=”)。
(3)一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=___ 。
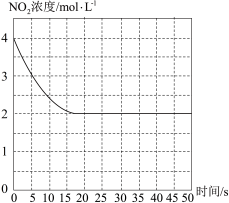
(4)T1℃下一密闭容器中充入一定量的NO2,测得NO2浓度随时间变化的曲线如图所示。前5秒内O2的平均生成速率为___ ;T1℃下反应2NO(g)+O2(g) 2NO2(g)的化学平衡常数K=
2NO2(g)的化学平衡常数K=__ 。
(5)对于(4)中的反应体系达平衡后,若降低温度,再次达平衡后,混合气体的平均相对分子质量___ (填“增大”、“减小”或“不变”);对于(4)中的反应体系达平衡后,若在恒温恒容条件下,追加NO2,再次达平衡后,NO2的体积分数___ (填“增大”、“减小”或“不变”)。
(6)对于(4)中的反应体系达平衡后(压强为P1),若在恒温恒容条件下,向其中充入一定量O2,再次达平衡后,测得压强为P2,P1︰P2 = 5︰8,则再次平衡时NO2的浓度为___ mol·L-1。(精确到小数点后两位)
 2NO2(g),其反应历程分两步:
2NO2(g),其反应历程分两步:①2NO(g)
 N2O2(g)(快反应) v1正=k1正·c2(NO), v1逆=k1逆·c(N2O2) ΔH1<0
N2O2(g)(快反应) v1正=k1正·c2(NO), v1逆=k1逆·c(N2O2) ΔH1<0②N2O2(g)+O2(g)
 2NO2(g)(慢反应) v2正=k2正·c(N2O2)·c(O2), v2逆=k2逆·c2(NO2) ΔH2<0
2NO2(g)(慢反应) v2正=k2正·c(N2O2)·c(O2), v2逆=k2逆·c2(NO2) ΔH2<0反应历程的能量变化如图:

请回答下列问题:
(1)反应2NO(g)+O2(g)
 2NO2(g)的ΔH
2NO2(g)的ΔH(2)决定2NO(g)+O2(g)
 2NO2(g)反应速率是反应②,E4+E2
2NO2(g)反应速率是反应②,E4+E2(3)一定温度下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=(4)T1℃下一密闭容器中充入一定量的NO2,测得NO2浓度随时间变化的曲线如图所示。前5秒内O2的平均生成速率为
 2NO2(g)的化学平衡常数K=
2NO2(g)的化学平衡常数K=
(5)对于(4)中的反应体系达平衡后,若降低温度,再次达平衡后,混合气体的平均相对分子质量
(6)对于(4)中的反应体系达平衡后(压强为P1),若在恒温恒容条件下,向其中充入一定量O2,再次达平衡后,测得压强为P2,P1︰P2 = 5︰8,则再次平衡时NO2的浓度为
您最近一年使用:0次
【推荐1】我国科学家首次实现利用甲烷在温和条件下高选择性氧化制甲醇。
反应Ⅰ: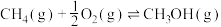

反应Ⅱ: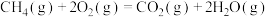
(1)已知:①
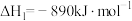
②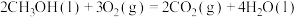
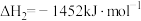
③
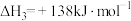
上述反应Ⅰ中的
___________  。
。
(2)在密闭容器中投入2mol 和1mol
和1mol ,起始投料量不变,在不同温度、压强下做平行实验,测得
,起始投料量不变,在不同温度、压强下做平行实验,测得 的平衡体积分数与温度、压强的关系如图所示:
的平衡体积分数与温度、压强的关系如图所示:

①由图可知,当 时,以反应
时,以反应___________ (填“Ⅰ”或“Ⅱ”)为主,理由是___________ ;
② 时,三条曲线几乎相连的原因可能是
时,三条曲线几乎相连的原因可能是___________ ;
③a、b、c由大到小排序为___________ 。
(3)在恒温的刚性(恒容)密闭容器中,分别按照(a) 、
、 的体积比为2:1以及(b)
的体积比为2:1以及(b) 、
、 、
、 (
( 的作用是活化催化剂)的体积比为2:1:8进行投料,反应相同的时间(都加入相同催化剂),所得产物的选择性[如甲醇的选择性=
的作用是活化催化剂)的体积比为2:1:8进行投料,反应相同的时间(都加入相同催化剂),所得产物的选择性[如甲醇的选择性= ]如表所示:
]如表所示:
①投料b能显著提高甲醇选择性的原因是___________ 。
②向上述刚性密闭容器中按照体积比2:1:8充入 、
、 和
和 ,在450K下达到平衡状态时,
,在450K下达到平衡状态时, 的转化率为50%,
的转化率为50%, 的选择性为90%,则副反应的压强平衡常数
的选择性为90%,则副反应的压强平衡常数
___________ (计算结果保留1位小数)。
(4)我国科学家研发新型催化剂,利用电催化法实现甲烷转化成甲醇,装置如图所示:

交换膜M的名称是___________ ;阳极的电极反应式为___________ 。
反应Ⅰ:
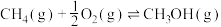

反应Ⅱ:
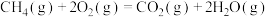
(1)已知:①

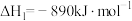
②
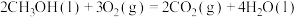
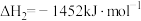
③

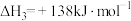
上述反应Ⅰ中的

 。
。(2)在密闭容器中投入2mol
 和1mol
和1mol ,起始投料量不变,在不同温度、压强下做平行实验,测得
,起始投料量不变,在不同温度、压强下做平行实验,测得 的平衡体积分数与温度、压强的关系如图所示:
的平衡体积分数与温度、压强的关系如图所示:
①由图可知,当
 时,以反应
时,以反应②
 时,三条曲线几乎相连的原因可能是
时,三条曲线几乎相连的原因可能是③a、b、c由大到小排序为
(3)在恒温的刚性(恒容)密闭容器中,分别按照(a)
 、
、 的体积比为2:1以及(b)
的体积比为2:1以及(b) 、
、 、
、 (
( 的作用是活化催化剂)的体积比为2:1:8进行投料,反应相同的时间(都加入相同催化剂),所得产物的选择性[如甲醇的选择性=
的作用是活化催化剂)的体积比为2:1:8进行投料,反应相同的时间(都加入相同催化剂),所得产物的选择性[如甲醇的选择性= ]如表所示:
]如表所示:| 投料方式 | a | b |
 的选择性/% 的选择性/% | 90 | 15 |
 的选择性/% 的选择性/% | 10 | 85 |
①投料b能显著提高甲醇选择性的原因是
②向上述刚性密闭容器中按照体积比2:1:8充入
 、
、 和
和 ,在450K下达到平衡状态时,
,在450K下达到平衡状态时, 的转化率为50%,
的转化率为50%, 的选择性为90%,则副反应的压强平衡常数
的选择性为90%,则副反应的压强平衡常数
(4)我国科学家研发新型催化剂,利用电催化法实现甲烷转化成甲醇,装置如图所示:

交换膜M的名称是
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐2】 、
、 为重要化工原料,常用于合成重要化合物。
为重要化工原料,常用于合成重要化合物。
Ⅰ.以 、
、 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:
ⅰ
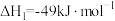
ⅱ
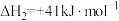
ⅲ

回答下列问题:
(1) 为分压平衡常数,各反应的
为分压平衡常数,各反应的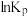 随
随 的变化如图所示。
的变化如图所示。
_______  ,其对应的曲线为
,其对应的曲线为_______ (填“a”或“c”)。
(2)在5MPa下,按照 投料,平衡时,CO和
投料,平衡时,CO和 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 的转化率随温度的变化如图:
的转化率随温度的变化如图: 的曲线为
的曲线为_______ (填“m”或“n”)。
②解释150~250℃范围内 转化率随温度升高而降低的原因
转化率随温度升高而降低的原因_______ 。
③下列说法错误的是_______ (填字母)。
A. 的平衡转化率始终低于
的平衡转化率始终低于 的
的
B.温度越低,越有利于工业生产
C.加入选择性高的催化剂,可提高 的平衡转化率
的平衡转化率
D.150-400℃范围内,温度升高, 的平衡产量先减小后增大
的平衡产量先减小后增大
④270℃时CO的分压为_______ ,反应ⅱ的平衡常数为_______ (列出算式)。
Ⅱ. 超干重整
超干重整 得到的CO经偶联反应可制得
得到的CO经偶联反应可制得 (草酸)。
(草酸)。
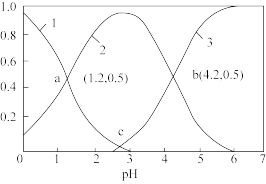
(3)在水溶液中 、
、 和
和 物质的量分数与pH关系如图所示,则c点溶液
物质的量分数与pH关系如图所示,则c点溶液
_______ 。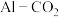 电池(工作原理如下图所示)能有效地将
电池(工作原理如下图所示)能有效地将 转化成化工原料草酸铝
转化成化工原料草酸铝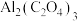
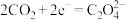 (草酸根)正极反应过程中,
(草酸根)正极反应过程中, 起催化作用,催化过程可表示为:①
起催化作用,催化过程可表示为:①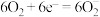 ②……
②……
(4)写出反应②的方程式_______ 。
 、
、 为重要化工原料,常用于合成重要化合物。
为重要化工原料,常用于合成重要化合物。Ⅰ.以
 、
、 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:ⅰ

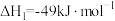
ⅱ

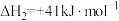
ⅲ


回答下列问题:
(1)
 为分压平衡常数,各反应的
为分压平衡常数,各反应的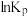 随
随 的变化如图所示。
的变化如图所示。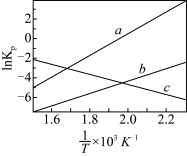

 ,其对应的曲线为
,其对应的曲线为(2)在5MPa下,按照
 投料,平衡时,CO和
投料,平衡时,CO和 在含碳产物中物质的量分数及
在含碳产物中物质的量分数及 的转化率随温度的变化如图:
的转化率随温度的变化如图: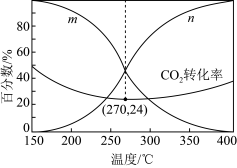
 的曲线为
的曲线为②解释150~250℃范围内
 转化率随温度升高而降低的原因
转化率随温度升高而降低的原因③下列说法错误的是
A.
 的平衡转化率始终低于
的平衡转化率始终低于 的
的B.温度越低,越有利于工业生产

C.加入选择性高的催化剂,可提高
 的平衡转化率
的平衡转化率D.150-400℃范围内,温度升高,
 的平衡产量先减小后增大
的平衡产量先减小后增大④270℃时CO的分压为
Ⅱ.
 超干重整
超干重整 得到的CO经偶联反应可制得
得到的CO经偶联反应可制得 (草酸)。
(草酸)。(3)在水溶液中
 、
、 和
和 物质的量分数与pH关系如图所示,则c点溶液
物质的量分数与pH关系如图所示,则c点溶液
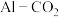 电池(工作原理如下图所示)能有效地将
电池(工作原理如下图所示)能有效地将 转化成化工原料草酸铝
转化成化工原料草酸铝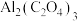
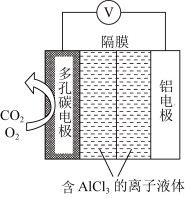
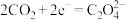 (草酸根)正极反应过程中,
(草酸根)正极反应过程中, 起催化作用,催化过程可表示为:①
起催化作用,催化过程可表示为:①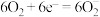 ②……
②……(4)写出反应②的方程式
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
【推荐3】含氮化合物在生产生活中有重要的应用。请回答:
(1)NOx与含硫化合物的热化学方程式如下:
反应I:CaS(s)+3NO2(g)=CaO(s)+SO2(g)+3NO(g) △H=-279.12kJ·mol-1 K1
反应II:CaS(s)+4NO2(g)=CaSO4(s)+4NO(g) △H=-714.52kJ·mol-1 K2
反应III:CaSO4(s)+NO(g)=CaO(s)+SO2(g)+NO2(g) △H K3
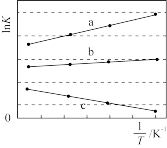
①三个反应的平衡常数的lnK随温度变化关系如图所示,则表示lnK2的曲线是____ 。
②在恒温条件下,加入反应物,一段时间后达到平衡时c(SO2)如图所示,t1时减小容器体积,t2时达到新平衡,请画出t1至t2时c(SO2)变化趋势图____ 。
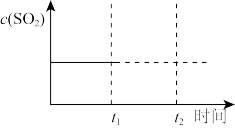
(2)合成氨工厂以“水煤气”和N2为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、H2、H2O、N2的混合气体,在反应器A进行合成氨,其催化剂III铁触媒,在500℃活性最大,反应器B中主要发生的反应为:CO(g)+H2O(g) CO2(g)+H2(g) △H<0,装置如图。
CO2(g)+H2(g) △H<0,装置如图。
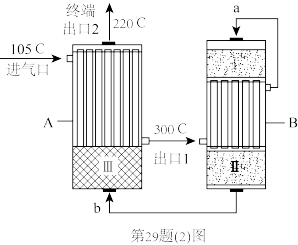
①温度比较:气流a____ 气流b(填“>”“<”或“=”)。
②气体流速一定,经由催化剂I到催化剂II,原料转化率有提升,其可能原因是:____ 。
③下列说法正确的是____ 。
A.利用焦炭与水蒸气高温制备水煤气时,适当加快通入水蒸气的流速,有利于水煤气的生成
B.N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ·mol-1反应器温度越低,终端出口2收率越高
2NH3(g) △H=-92.4kJ·mol-1反应器温度越低,终端出口2收率越高
C.终端出口2得到的气体,通过水吸收,再加热水溶液,可分离出NH3
D.反应原料气从进气口105℃到300℃出口1,已完成氨的合成
(3)已知-33℃液氨中存在:2NH3(l) NH
NH +NH
+NH K=10-29,在100mL液氨中加入0.0001mol NH4Cl固体溶解,并完全电离(忽略体积变化),则c(NH
K=10-29,在100mL液氨中加入0.0001mol NH4Cl固体溶解,并完全电离(忽略体积变化),则c(NH )=
)=____ mol·L-1。金属钾能溶解于液氨中形成蓝色的液氨溶液,反应的化学方程式为K+NH3=K++e(NH3) (电子的氨合物,显蓝色),加入NH4Cl固体,即发生共价键断裂和形成的反应,请写出离子方程式
(电子的氨合物,显蓝色),加入NH4Cl固体,即发生共价键断裂和形成的反应,请写出离子方程式____ 。
(1)NOx与含硫化合物的热化学方程式如下:
反应I:CaS(s)+3NO2(g)=CaO(s)+SO2(g)+3NO(g) △H=-279.12kJ·mol-1 K1
反应II:CaS(s)+4NO2(g)=CaSO4(s)+4NO(g) △H=-714.52kJ·mol-1 K2
反应III:CaSO4(s)+NO(g)=CaO(s)+SO2(g)+NO2(g) △H K3
①三个反应的平衡常数的lnK随温度变化关系如图所示,则表示lnK2的曲线是

②在恒温条件下,加入反应物,一段时间后达到平衡时c(SO2)如图所示,t1时减小容器体积,t2时达到新平衡,请画出t1至t2时c(SO2)变化趋势图
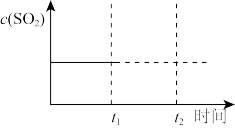
(2)合成氨工厂以“水煤气”和N2为原料,采用两段间接换热式绝热反应器,由进气口充入一定量含CO、H2、H2O、N2的混合气体,在反应器A进行合成氨,其催化剂III铁触媒,在500℃活性最大,反应器B中主要发生的反应为:CO(g)+H2O(g)
 CO2(g)+H2(g) △H<0,装置如图。
CO2(g)+H2(g) △H<0,装置如图。
①温度比较:气流a
②气体流速一定,经由催化剂I到催化剂II,原料转化率有提升,其可能原因是:
③下列说法正确的是
A.利用焦炭与水蒸气高温制备水煤气时,适当加快通入水蒸气的流速,有利于水煤气的生成
B.N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ·mol-1反应器温度越低,终端出口2收率越高
2NH3(g) △H=-92.4kJ·mol-1反应器温度越低,终端出口2收率越高C.终端出口2得到的气体,通过水吸收,再加热水溶液,可分离出NH3
D.反应原料气从进气口105℃到300℃出口1,已完成氨的合成
(3)已知-33℃液氨中存在:2NH3(l)
 NH
NH +NH
+NH K=10-29,在100mL液氨中加入0.0001mol NH4Cl固体溶解,并完全电离(忽略体积变化),则c(NH
K=10-29,在100mL液氨中加入0.0001mol NH4Cl固体溶解,并完全电离(忽略体积变化),则c(NH )=
)= (电子的氨合物,显蓝色),加入NH4Cl固体,即发生共价键断裂和形成的反应,请写出离子方程式
(电子的氨合物,显蓝色),加入NH4Cl固体,即发生共价键断裂和形成的反应,请写出离子方程式
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐1】丙烯是重要的有机化工原料之一,丙烷直接脱氢制丙烯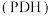 是一条绿色生产丙烯的途径。
是一条绿色生产丙烯的途径。
主反应: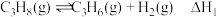
副反应: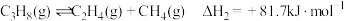
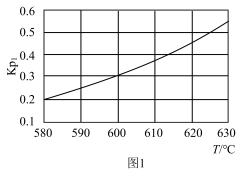
(1) 恒压下,主反应的
恒压下,主反应的 随温度变化如图1所示,
随温度变化如图1所示,
_______ 0(填”、“<”或=”),判断的理由是_______ 。
(2) 恒压下,
恒压下,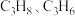 在不同温度下的平衡体积分数如图2所示,图中表示
在不同温度下的平衡体积分数如图2所示,图中表示 的体积分数的曲线为
的体积分数的曲线为_______ (填“a”或“b”), 时,
时, 的体积分数为
的体积分数为_______ 。

(3)下列关于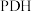 工艺说法正确的是
工艺说法正确的是
(4)丙烷氧化脱氢制丙烯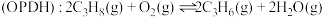
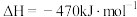 ,相比
,相比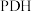 ,该途径生产丙烯的好处是
,该途径生产丙烯的好处是_______ 。
(5)用下图所示装置电解二氧化碳酸性溶液也可制得丙烯。
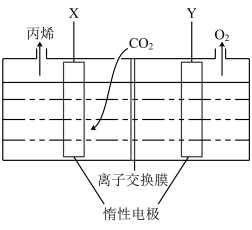
①Y极与电源_______ (填“正”或“负”)极相连。
②X极的电极反应式为_______ 。
③理论上,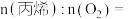
_______ 。
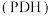 是一条绿色生产丙烯的途径。
是一条绿色生产丙烯的途径。主反应:
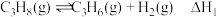
副反应:
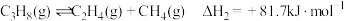
(1)
 恒压下,主反应的
恒压下,主反应的 随温度变化如图1所示,
随温度变化如图1所示,

(2)
 恒压下,
恒压下,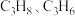 在不同温度下的平衡体积分数如图2所示,图中表示
在不同温度下的平衡体积分数如图2所示,图中表示 的体积分数的曲线为
的体积分数的曲线为 时,
时, 的体积分数为
的体积分数为
(3)下列关于
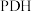 工艺说法正确的是
工艺说法正确的是A. 的物质的量分数不再改变,反应体系已达平衡 的物质的量分数不再改变,反应体系已达平衡 |
| B.采用合适的催化剂能提高主反应的平衡转化率,促使丙烯的产率提高 |
C.反应达到平衡后,增加压强,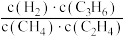 不变 不变 |
D.升高温度,生成 的速率加快,生成其他副产物的速率减慢 的速率加快,生成其他副产物的速率减慢 |
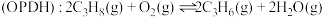
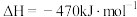 ,相比
,相比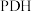 ,该途径生产丙烯的好处是
,该途径生产丙烯的好处是(5)用下图所示装置电解二氧化碳酸性溶液也可制得丙烯。

①Y极与电源
②X极的电极反应式为
③理论上,
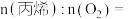
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐2】反应N2(g)+3H2(g) 2NH3(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
2NH3(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
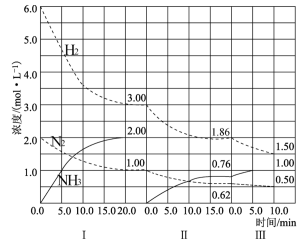
回答问题:
(1)在3个阶段中,N2的平均反应速率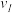 (N2)、
(N2)、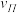 (N2)、
(N2)、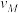 (N2)中最大的是
(N2)中最大的是________ ,其值是________ 。
(2)H2的平衡转化率αⅠ(H2)、αⅡ(H2)、αⅢ(H2)的大小关系是________________ 。
(3)由第一次平衡到第二次平衡,平衡移动的方向是_________ (填“正反应方向”或“逆反应方向”),采取的措施是____________________ 。
(4)第Ⅰ阶段时,化学平衡常数K1=___________ ;第Ⅱ、Ⅲ阶段化学平衡常数K2_________ K3;(填“>、<、=”)判断的理由是_________________ 。
 2NH3(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
2NH3(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)在3个阶段中,N2的平均反应速率
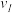 (N2)、
(N2)、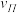 (N2)、
(N2)、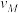 (N2)中最大的是
(N2)中最大的是(2)H2的平衡转化率αⅠ(H2)、αⅡ(H2)、αⅢ(H2)的大小关系是
(3)由第一次平衡到第二次平衡,平衡移动的方向是
(4)第Ⅰ阶段时,化学平衡常数K1=
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
【推荐3】甲醇是重要的化工原料,工业上可利用 生产甲醇,同时可减少温室气体二氧化碳,发生反应①:
生产甲醇,同时可减少温室气体二氧化碳,发生反应①:

(1)下列措施中,能提高 平衡转化率的是___________。
平衡转化率的是___________。
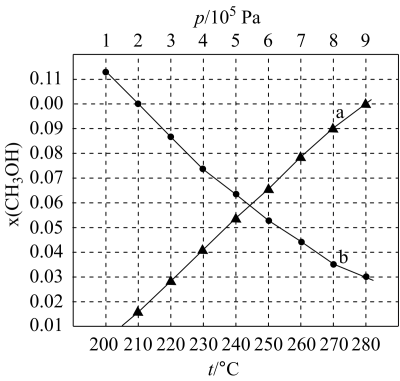
(2)当起始物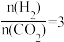 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为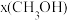 ,在
,在 下的
下的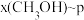 、在
、在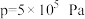 下的
下的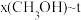 如图所示。当
如图所示。当 的平衡转化率为
的平衡转化率为 时,反应条件可能是
时,反应条件可能是___________ 。
(3)在某催化剂作用下, 和
和 除发生反应①外,还发生反应②:
除发生反应①外,还发生反应②:
 。维持压强不变,按固定初始投料比将
。维持压强不变,按固定初始投料比将 和
和 按一定流速通过该催化剂,经相同时间测得实验数据:
按一定流速通过该催化剂,经相同时间测得实验数据:
注:甲醇的选择性是指发生反应的 中转化为甲醇的百分比。
中转化为甲醇的百分比。
表中数据说明,升高温度, 的实际转化率提高而甲醇的选择性降低,其原因是
的实际转化率提高而甲醇的选择性降低,其原因是___________ 。
(4)甲醇催化制取丙烯的过程中发生反应: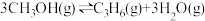 ,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为
,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数)。
为活化能,k为速率常数,R和C为常数)。
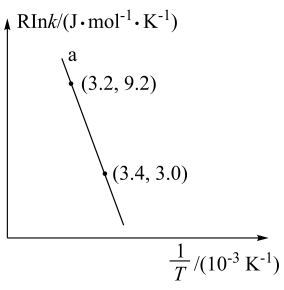
①反应的活化能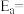
__  。
。
②当使用更高效催化剂时,在图中画出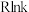 与
与 关系的示意图
关系的示意图__ 。
 生产甲醇,同时可减少温室气体二氧化碳,发生反应①:
生产甲醇,同时可减少温室气体二氧化碳,发生反应①:

(1)下列措施中,能提高
 平衡转化率的是___________。
平衡转化率的是___________。A.在原料气中加入适量 | B.从体系中不断分离出甲醇 |
| C.循环利用原料气 | D.使用高效催化剂 |
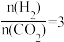 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为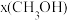 ,在
,在 下的
下的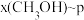 、在
、在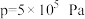 下的
下的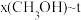 如图所示。当
如图所示。当 的平衡转化率为
的平衡转化率为 时,反应条件可能是
时,反应条件可能是
(3)在某催化剂作用下,
 和
和 除发生反应①外,还发生反应②:
除发生反应①外,还发生反应②:
 。维持压强不变,按固定初始投料比将
。维持压强不变,按固定初始投料比将 和
和 按一定流速通过该催化剂,经相同时间测得实验数据:
按一定流速通过该催化剂,经相同时间测得实验数据: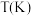 |  实际转化率(%) 实际转化率(%) | 甲醇选择性(%) |
| 543 | 12.3 | 42.3 |
| 553 | 15.3 | 39.1 |
 中转化为甲醇的百分比。
中转化为甲醇的百分比。表中数据说明,升高温度,
 的实际转化率提高而甲醇的选择性降低,其原因是
的实际转化率提高而甲醇的选择性降低,其原因是(4)甲醇催化制取丙烯的过程中发生反应:
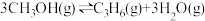 ,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为
,反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数)。
为活化能,k为速率常数,R和C为常数)。
①反应的活化能
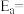
 。
。②当使用更高效催化剂时,在图中画出
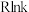 与
与 关系的示意图
关系的示意图
您最近一年使用:0次



