在一定条件下,对于反应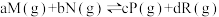
 ,M的物质的量分数(M%)与温度、压强的关系如图所示
,M的物质的量分数(M%)与温度、压强的关系如图所示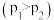 ,则下列判断正确的是
,则下列判断正确的是
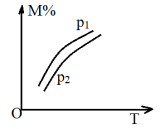
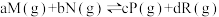
 ,M的物质的量分数(M%)与温度、压强的关系如图所示
,M的物质的量分数(M%)与温度、压强的关系如图所示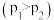 ,则下列判断正确的是
,则下列判断正确的是
A. , , | B. , , |
C. , , | D. , , |
更新时间:2021-12-23 20:32:18
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】利用无水乙醇催化脱水制备乙烯时发生反应Ⅰ、Ⅱ,有关反应在不同温度下的化学平衡常数如下表所示。下列说法正确的是
| 温度/K | 化学平衡常数 | |
Ⅰ.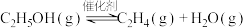 | Ⅱ.  | |
| 500 | 3.2 | 0.80 |
| 700 | 7.7 | 0.14 |
| 900 | 12.3 | 0.12 |
| A.升高温度,反应Ⅰ的速率加快,反应Ⅱ的速率减慢 |
| B.增大压强有利于提高乙烯的产量 |
| C.升高温度有利于提高乙烯的产量 |
D.700K时,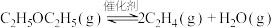 的平衡常数为15.26 的平衡常数为15.26 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列图示中的实验装置不能达到实验目的是
 |  |  |  |
Ⅰ | Ⅱ | Ⅲ | Ⅳ |
A.装置Ⅰ:2NO2 N2O4该反应为放热反应 N2O4该反应为放热反应 |
| B.装置Ⅱ:证明铁钉发生了析氢腐蚀 |
| C.装置Ⅲ:测定酸碱中和反应的中和热 |
| D.装置Ⅳ:测定反应Zn+2H+=Zn2++H2↑的平均反应速率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】将BaO2放入密闭的真空容器中,反应2BaO2(s)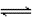 2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
 2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是| A.平衡常数减小 | B.n(BaO)不变 | C.氧气压强增大 | D.n(BaO2)增加 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列叙述中说明某化学平衡一定发生移动的是 ( )
| A.反应物的转化率改变 | B.正、逆反应速率改变 |
| C.混合物中各组分的浓度改变 | D.混合体系中气体密度发生变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列实验事实能用平衡移动原理解释的是( )
A.反应I2(g)+H2(g) 2HI(g) 达平衡后,压缩体积体系颜色变深 2HI(g) 达平衡后,压缩体积体系颜色变深 |
| B.H2O2中加入二氧化锰,生成氧气的速率加快 |
| C.棕黄色的FeCl3溶液中加入铁粉颜色逐渐变为浅绿色 |
D.反应CO(g)+NO2(g) CO2(g)+NO(g)△H<0,达平衡后,升高温度体系颜色变深 CO2(g)+NO(g)△H<0,达平衡后,升高温度体系颜色变深 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列生产、生活或化学实验中的应用,不能利用勒夏特列原理进行解释的是
| A.使用含氟牙膏可预防龋齿 |
| B.使用碳酸钠溶液处理锅炉水垢 |
C.实验室保存和配制 溶液时,加入 溶液时,加入 固体 固体 |
D.保存 溶液常在溶液中加铁粉 溶液常在溶液中加铁粉 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】在温度相同,压强分别为P1和P2的条件下,A(g)+2B(g) 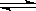 nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是
nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是
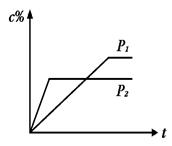
 nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是
nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如图所示,下面结论正确的是
| A.P1>P2,n<3 | B.P1<P2,n>3 |
| C.P1>P2,n>3 | D.P1<P2,n<3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在其他条件不变时,改变某一外界条件对反应 化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),下列说法不正确的是
化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),下列说法不正确的是
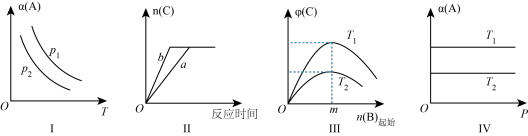
 化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),下列说法不正确的是
化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),下列说法不正确的是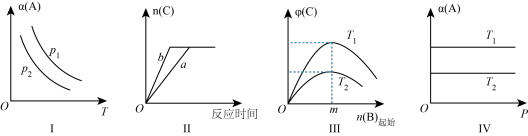
A.在Ⅰ中,若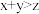 ,则 ,则 > > |
| B.在Ⅱ中,若a→b为使用合适的催化剂,则A的转化率不变 |
C.在Ⅲ中,随着B的起始物质的量的增加,在m点时,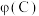 达到最大值,则m点反应物A与B的投料量比为 x:y 达到最大值,则m点反应物A与B的投料量比为 x:y |
D.在Ⅳ中,若T1>T2,则该反应的平衡常数 > > ;若T1<T2,则该反应的平衡常数 ;若T1<T2,则该反应的平衡常数 < < |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】一定条件下,通过下列反应可以制备特种陶瓷的原料 MgO, MgSO4(s) + CO(g) ⇌ MgO(s) + CO2(g) + SO2(g) ΔH > 0。该反应在恒容的密闭容器中达到平衡后(A 点),若仅改变图中横坐标 x 的值, 重新达到平衡后,纵坐标 y 随 x 变化趋势合理的是( )(忽略固体物质所占有的体积)
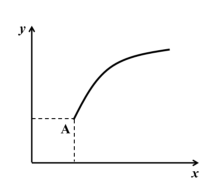

| A.x 为温度,y 为容器内混合气体的密度 |
| B.x 为 MgSO4的质量,y 为 CO 的平衡转化率 |
| C.x 为 CO2的物质的量,y 为 CO 的平衡转化率 |
| D.x 为 SO2的浓度,y 为 CO2的平衡浓度 |
您最近一年使用:0次

 nC(g)(△H<0)在不同条件下反应混合物中C的体积分数与反应过程所需时间的关系曲线。则下列有关叙述正确的是
nC(g)(△H<0)在不同条件下反应混合物中C的体积分数与反应过程所需时间的关系曲线。则下列有关叙述正确的是
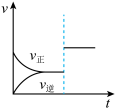
 2NH3(g)
2NH3(g) 和
和 反应生成
反应生成


