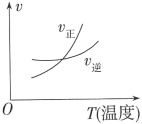
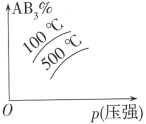
在其他条件不变时,改变某一外界条件对反应 化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),下列说法不正确的是
化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),下列说法不正确的是
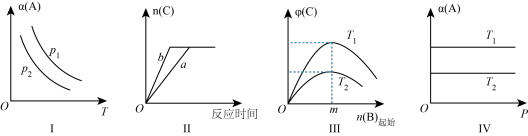
 化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),下列说法不正确的是
化学平衡的影响,得到如图所示的图像(p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,φ表示体积分数),下列说法不正确的是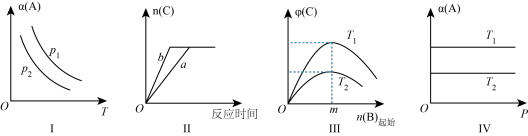
A.在Ⅰ中,若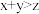 ,则 ,则 > > |
| B.在Ⅱ中,若a→b为使用合适的催化剂,则A的转化率不变 |
C.在Ⅲ中,随着B的起始物质的量的增加,在m点时,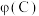 达到最大值,则m点反应物A与B的投料量比为 x:y 达到最大值,则m点反应物A与B的投料量比为 x:y |
D.在Ⅳ中,若T1>T2,则该反应的平衡常数 > > ;若T1<T2,则该反应的平衡常数 ;若T1<T2,则该反应的平衡常数 < < |
22-23高二上·四川遂宁·期末 查看更多[3]
(已下线)专题04 化学平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)重庆市杨家坪中学2023-2024学年高二上学期第一次月考化学试题四川省遂宁市2022-2023学年高二上学期期末考试化学试题
更新时间:2023-02-18 21:45:08
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】温度为T时,在密闭容器中发生反应:A(g) 2B(g) ΔH>0,反应达到平衡后,下列能使B的浓度减小的措施是
2B(g) ΔH>0,反应达到平衡后,下列能使B的浓度减小的措施是
 2B(g) ΔH>0,反应达到平衡后,下列能使B的浓度减小的措施是
2B(g) ΔH>0,反应达到平衡后,下列能使B的浓度减小的措施是| A.升高反应体系的温度 | B.缩小密闭容器的容积 |
| C.使用合适的催化剂 | D.恒压时通入稀有气体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在一定温度下,将气体X与气体Y各0.16mol充入10L恒容密闭容器中,发生反应: ,一段时间后达到平衡。反应过程中测定的数据如表,下列说法正确的是
,一段时间后达到平衡。反应过程中测定的数据如表,下列说法正确的是
 ,一段时间后达到平衡。反应过程中测定的数据如表,下列说法正确的是
,一段时间后达到平衡。反应过程中测定的数据如表,下列说法正确的是| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.反应过程中化学反应速率保持不变 |
| B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) |
| C.该温度下此反应的平衡常数K=1.44 |
| D.其他条件不变,缩小容器体积,重新达平衡时Z的体积分数增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列实验方案、对应现象和结论有错误的是
| 实验方案 | 现象 | 结论 | |
| A | 将注射器充满 气体,再将活塞往里推,压缩体积 气体,再将活塞往里推,压缩体积 | 从注射器侧面观察,气体颜色加深 | 加压平衡向生成 气体的方向移动 气体的方向移动 |
| B | 用铁片、铜片、稀硫酸等组成原电池 | 铜片表面有气泡产生 | 铁的金属性强于铜 |
| C | 室温下,测量等浓度的KA、KB两种弱酸盐溶液的pH | 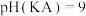 、 、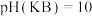 | 水解能力: |
| D | 向沸水中滴加5~6滴饱和 溶液,持续煮沸 溶液,持续煮沸 | 溶液先变成红褐色再析出沉淀 |  先水解得 先水解得 胶体再聚集成 胶体再聚集成 沉淀 沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于合成氨工业说法不正确的是
| A.将原料气进行净化处理,是为了防止其中混有的杂质使催化剂“中毒” |
| B.合成氨厂一般采用10MPa~30MPa,综合考虑了反应速率、转化率和成本等因素 |
| C.将混合气体中的氨液化有利于合成氨反应 |
| D.根据勒夏特列原理,500℃左右比室温更有利于合成氨的反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】一定条件下,在容积不变的密闭容器中进行如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g)+Q(Q>0),图曲线a表示该反应过程中NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是( )
N2(g)+2CO2(g)+Q(Q>0),图曲线a表示该反应过程中NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是( )

 N2(g)+2CO2(g)+Q(Q>0),图曲线a表示该反应过程中NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是( )
N2(g)+2CO2(g)+Q(Q>0),图曲线a表示该反应过程中NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是( )
| A.降低温度 | B.加催化剂 |
| C.增大反应物中NO的浓度 | D.向密闭容器中加入氩气 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知除去NO的一种反应如下:
主反应:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H
4N2(g)+6H2O(g) △H
副反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
相同条件下,在甲、乙两种催化剂作用下进行上述反应。下列说法错误的是

主反应:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H
4N2(g)+6H2O(g) △H副反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)相同条件下,在甲、乙两种催化剂作用下进行上述反应。下列说法错误的是

| A.△H<0 |
| B.乙催化剂的催化效果要强于甲 |
| C.改变催化剂的选择性,可以减少副反应的发生 |
| D.相同条件下选择高效催化剂,可以提高M点的平衡转化率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】对可逆反应N2(g)+3H2(g) 2NH3(g)△H<0,下列图像正确的是
2NH3(g)△H<0,下列图像正确的是
 2NH3(g)△H<0,下列图像正确的是
2NH3(g)△H<0,下列图像正确的是A.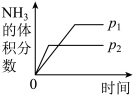 | B.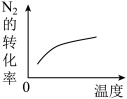 |
C.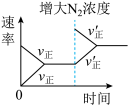 | D.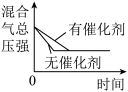 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
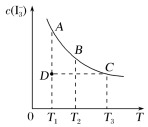
【推荐2】I2在KI溶液中存在平衡I2(aq)+I-(aq)  I
I (aq),某I2、KI混合溶液中,I
(aq),某I2、KI混合溶液中,I 的物质的量浓度c(I
的物质的量浓度c(I )与温度T的关系如图所示(曲线上任意一点都表示平衡状态)。下列说法正确的是
)与温度T的关系如图所示(曲线上任意一点都表示平衡状态)。下列说法正确的是
 I
I (aq),某I2、KI混合溶液中,I
(aq),某I2、KI混合溶液中,I 的物质的量浓度c(I
的物质的量浓度c(I )与温度T的关系如图所示(曲线上任意一点都表示平衡状态)。下列说法正确的是
)与温度T的关系如图所示(曲线上任意一点都表示平衡状态)。下列说法正确的是
A.反应I2(aq)+I-(aq)  I I (aq)的ΔH>0 (aq)的ΔH>0 |
| B.若温度为T1、T2时,平衡体系中I-的逆反应速率分别为v1、v2,则v1>v2 |
| C.若反应达到平衡状态,向混合溶液中加入KI固体,平衡向右移动 |
| D.状态D时,v正=v逆 |
您最近一年使用:0次

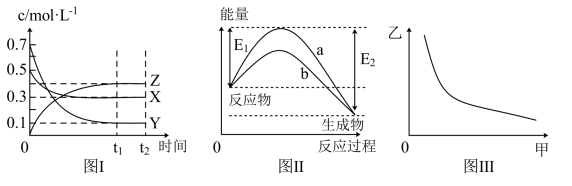
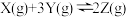
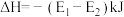
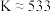 ,且若升高温度,K值减小
,且若升高温度,K值减小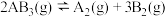
 。关于该反应的下列图象(
。关于该反应的下列图象( 为体系中
为体系中 的质量分数)不正确的是
的质量分数)不正确的是