研究表明 与CO在
与CO在 的作用下会发生反应①
的作用下会发生反应① 、②
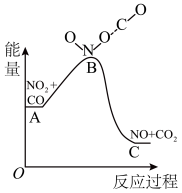
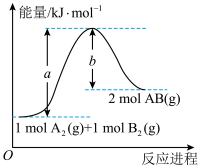
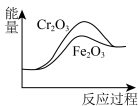
、② 其能量变化示意图如所示。下列说法错误的是
其能量变化示意图如所示。下列说法错误的是

 与CO在
与CO在 的作用下会发生反应①
的作用下会发生反应① 、②
、② 其能量变化示意图如所示。下列说法错误的是
其能量变化示意图如所示。下列说法错误的是
A. 使反应的活化能成小 使反应的活化能成小 | B.该催化剂可有效提高反应物的平衡转化率 |
C.总反应 | D.反应①过程中, 中的化学键发生了断裂 中的化学键发生了断裂 |
更新时间:2021-12-13 16:20:36
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】 和
和 在一定条件下能发生反应
在一定条件下能发生反应
已知:

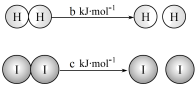
下列说法正确的是
 和
和 在一定条件下能发生反应
在一定条件下能发生反应
已知:


下列说法正确的是
| A.HI分子分解所吸收的热量主要用于克服分子间作用力 |
B.断开2molHI分子中的化学键所需能量约为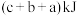 |
C.相同条件下,1mol 和1mol 和1mol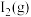 总能量小于2mol 总能量小于2mol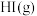 的总能量 的总能量 |
D.向密闭容器中加入1mol 和1mol 和1mol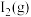 ,充分反应后放出的热量为akJ ,充分反应后放出的热量为akJ |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中的能量变化情况,判断下列说法正确的是
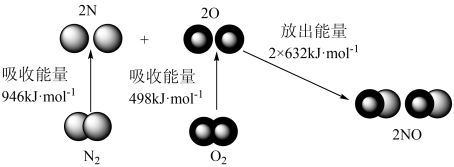

| A.N2(g)和O2(g)反应生成NO(g)是放热反应 |
| B.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量 |
| C.使用催化剂,该反应放出的热量增加 |
| D.通常情况下,N2(g)与O2(g)混合能直接生成NO(g) |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是
| A.自发反应仍需要适当的条件才能发生 |
| B.已知:①2H2(g)+O2(g)=2H2O(g) ΔH=-a kJ·mol-1,②2H2(g)+O2(g)=2H2O(l) ΔH=-bkJ·mol-1,则a>b |
| C.增大反应物浓度,单位体积内活化分子百分数增大,化学反应速率增大 |
| D.升高温度后,吸热反应的速率加快,放热反应的速率减慢 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在发射“神舟”七号的火箭推进器中装有肼(N2H4)和过氧化氢,当两者混合时即产生气体,并放出大量的热。已知:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) ΔH=-641.6 kJ·mol-1,下列说法不正确的是
| A.ΔS>0 |
| B.相同条件下,正反应活化能大于逆反应活化能 |
| C.升高温度可以提高活化分子的百分数与百分含量 |
| D.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g) ΔH<-641.6 kJ·mol-1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】甲硫醇是一种重要的化工原料,硫化氢与甲醇合成甲硫醇的催化过程如图。下列说法中不正确的是


| A.上述过程中总反应是取代反应 |
| B.1mol CH3SH中含有5NA个共价键 |
| C.若CD3OD和H2S参与,则可能生成CHD2SH和D2O |
| D.催化剂的使用大大提升了甲硫醇的平衡转化率 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】在恒温密闭容器中发生反应:CO2(g)+H2 (g) CO(g)+H2O(g) ΔH >0,下列有关说法正确的是
CO(g)+H2O(g) ΔH >0,下列有关说法正确的是
 CO(g)+H2O(g) ΔH >0,下列有关说法正确的是
CO(g)+H2O(g) ΔH >0,下列有关说法正确的是| A.反应达到平衡后,维持体积不变,充入CO2,平衡向正反应方向移动 |
| B.反应达到平衡后,维持压强不变,充入氦气,反应速率不变,平衡不移动 |
| C.使用催化剂,正反应速率增大,逆反应速率减小 |
| D.反应达到平衡后,降低温度,平衡正向移动 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列实验事实不能用平衡移动原理解释的是
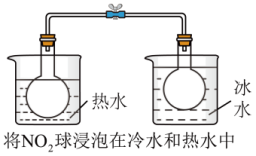
A.将NO2球浸泡在冷水中和热水中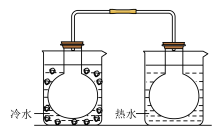 |
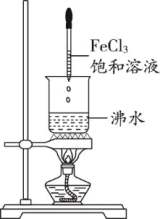
B.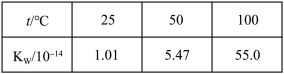 |
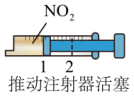
C.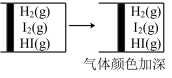 |
D.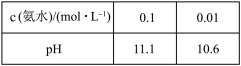 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】如图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在(1)中加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4NO3晶体,发现(1)中红棕色变深,(3)中红棕色变浅[已知反应2NO2(红棕色)⇌N2O4(无色)]。下列叙述正确的是
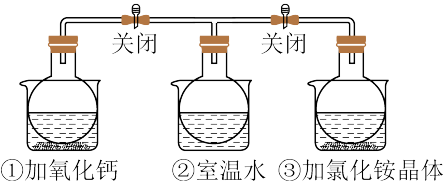

| A.2NO2⇌N2O4是放热反应 |
| B.NH4NO3溶于水时放出热量 |
| C.烧瓶(1)中平衡混合气体的相对分子质量增大 |
| D.烧瓶(3)中气体的压强增大 |
您最近半年使用:0次

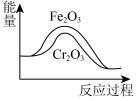
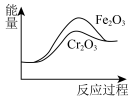
 的反应:
的反应: ,可用
,可用 和
和 作催化剂,其中
作催化剂,其中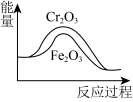
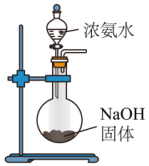
 固体制取氨气
固体制取氨气

