第四周期过渡元素常用于制造催化剂。请回答下列问题:
(1)石墨烯氧化锰复合催化剂能够使甲醛(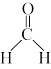 )转化生成
)转化生成 和
和 。
。
① 的基态原子的价层电子的轨道表示式为
的基态原子的价层电子的轨道表示式为_______ 。
② 是制备这种催化剂的原料,
是制备这种催化剂的原料, 中阴离子的立体构型为
中阴离子的立体构型为_______ 。
③在反应所涉及的物质中,属于极性分子的有_______ (填标号)。
A. B.
B. C.
C.
(2)铜可用作醇氧化反应的催化剂。例如苯甲醇氧化成苯甲醛:
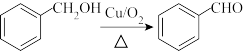 。
。
① 原子位于元素周期表中的
原子位于元素周期表中的_______ 区。
②苯甲醇分子中的碳原子的杂化类型为_______ 。
③在常压下,苯甲醇的沸点比苯甲醛的沸点高,主要原因是_______ 。
(1)石墨烯氧化锰复合催化剂能够使甲醛(
 )转化生成
)转化生成 和
和 。
。①
 的基态原子的价层电子的轨道表示式为
的基态原子的价层电子的轨道表示式为②
 是制备这种催化剂的原料,
是制备这种催化剂的原料, 中阴离子的立体构型为
中阴离子的立体构型为③在反应所涉及的物质中,属于极性分子的有
A.
 B.
B. C.
C.
(2)铜可用作醇氧化反应的催化剂。例如苯甲醇氧化成苯甲醛:
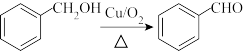 。
。①
 原子位于元素周期表中的
原子位于元素周期表中的②苯甲醇分子中的碳原子的杂化类型为
③在常压下,苯甲醇的沸点比苯甲醛的沸点高,主要原因是
21-22高二上·辽宁锦州·期末 查看更多[2]
更新时间:2022-01-23 17:41:44
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】某团队公布的研究成果中的阿比朵尔(M)可用于治疗新型冠状肺炎,可有效抑制病毒,其结构如图所示。
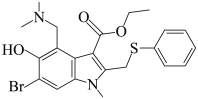
(1)基态Br原子中,核外电子占据的最高能级的符号为___________ ,基态O原子的核外电子排布图为___________ 。
(2)M分子中涉及的非金属元素中,第一电离能最大的元素是___________ (填元素符号,下同)。电负性最大的元素是___________ 。
(3)M分子中C原子杂化方式有___________ , 的键角小于
的键角小于 的键角的原因是
的键角的原因是___________ 。
(4)M分子中的元素间可形成能与金属离子(或原子)配位的配体。配合物W的结构如图所示,配合物W的中心离子是___________ (填离子符号)。

(5)硫化锌的晶胞结构如图所示, 与
与 之间的核间距为d pm,设
之间的核间距为d pm,设 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为___________ (列表达式) 。
。


(1)基态Br原子中,核外电子占据的最高能级的符号为
(2)M分子中涉及的非金属元素中,第一电离能最大的元素是
(3)M分子中C原子杂化方式有
 的键角小于
的键角小于 的键角的原因是
的键角的原因是(4)M分子中的元素间可形成能与金属离子(或原子)配位的配体。配合物W的结构如图所示,配合物W的中心离子是

(5)硫化锌的晶胞结构如图所示,
 与
与 之间的核间距为d pm,设
之间的核间距为d pm,设 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】依据原子结构知识回答下列问题。
(1)基态Cr原子的电子排布式是____________ ;基态 的价电子排布图为
的价电子排布图为____________ 。
(2)Cu、K、O、F四种元素中第一电离能最小的是______ ,电负性最大的是____________ 。
(3)下列有关微粒性质的排列顺序错误的是______。
(4)下列硼原子电子排布图表示的状态中,能量最高的为______(填选项字母)。
(5)O的基态原子核外电子空间运动状态有______ 种,其原子半径______  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(1)基态Cr原子的电子排布式是
 的价电子排布图为
的价电子排布图为(2)Cu、K、O、F四种元素中第一电离能最小的是
(3)下列有关微粒性质的排列顺序错误的是______。
| A.元素的电负性:P<O<F | B.元素的第一电离能:C<N<O |
C.离子半径: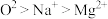 | D.原子的未成对电子数:Mn>Si>Cl |
A. | B.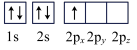 |
C. | D.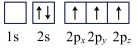 |
 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】依据原子结构知识回答下列问题。
(1)硅原子核外电子的运动状态有_____ 种。
(2)非金属性:S小于O。试用一个实验事实说明_____ 。
(3)一定温度下,对于可逆反应N2(g)+3H2(g) 2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。
2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。
(4)画出Fe3+的结构示意图_____ ;写出Mn2+的轨道表示式:_____ ;写出32号元素的元素符号及其价层电子排布式:_____ 。
(1)硅原子核外电子的运动状态有
(2)非金属性:S小于O。试用一个实验事实说明
(3)一定温度下,对于可逆反应N2(g)+3H2(g)
 2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。
2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。| A.单位时间内断裂amolN≡N键,同时断裂6amolN—H键 |
| B.NH3的生成速率与H2的生成速率之比为2∶3 |
| C.恒压容器内混合气体的总物质的量不再变化 |
| D.恒容容器内混合气体的密度不再变化 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3,其结构简式如下: ,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。请回答:
,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。请回答:
(1)与(HB=NH)3互为等电子体的分子为___________ (填分子式)。
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中共有___________ 个硼原子,___________ 个氮原子。
(3)人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷。工业上采用LiAlH4和BF3,在乙醚介质中反应制得乙硼烷(B2H6) ,同时生成另外两种产物,该反应的化学方程式为___________ 。
(4)相关化学键的键能如下表所示,简要分析和解释下列事实。
自然界中不存在硼单质,硼氢化物也很少,主要是含氧化物,其原因为___________ 。
(5)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式,图(a)为一种无限长单链状结构的多硼酸根,其化学式为___________ ;图(b)为硼砂晶体中的阴离子,其中硼原子采取的杂化类型___________ 。
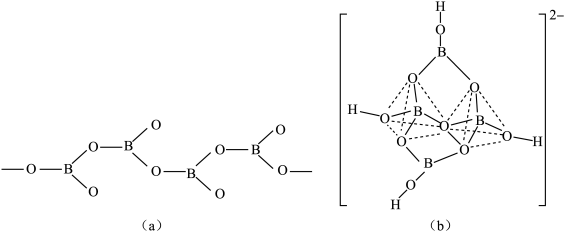
 ,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。请回答:
,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。请回答:(1)与(HB=NH)3互为等电子体的分子为
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中共有
(3)人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷。工业上采用LiAlH4和BF3,在乙醚介质中反应制得乙硼烷(B2H6) ,同时生成另外两种产物,该反应的化学方程式为
(4)相关化学键的键能如下表所示,简要分析和解释下列事实。
| 化学键 | B-H | B-O | B-B |
| 键能(KJ·mol-1) | 389 | 561 | 293 |
自然界中不存在硼单质,硼氢化物也很少,主要是含氧化物,其原因为
(5)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式,图(a)为一种无限长单链状结构的多硼酸根,其化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】我国“嫦娥”五号首次实现地外天体采样返回,这是我国航天事业的又一突破。带回的月壤中含有H、N、O、Al、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。请完成下列问题:
(1)N、O、Al、S四种元素第一电离能从大到小的顺序为_______ 。
(2)Cu、Au是同一副族的元素,Au的原子序数更大,它们属于_______ 区元素,基态Au原子的价电子排布式为_______ 。
(3)SO2分子的空间构型为_______ ,请写出一种与SO2互为等电子体的单质_______ (填化学式)。
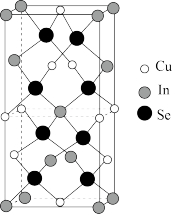
(4)某晶体的晶胞结构如图所示,该晶体的化学式为_______ 。如果将Se原子看做密堆积,则其堆积模型为_______ 。
(1)N、O、Al、S四种元素第一电离能从大到小的顺序为
(2)Cu、Au是同一副族的元素,Au的原子序数更大,它们属于
(3)SO2分子的空间构型为
(4)某晶体的晶胞结构如图所示,该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe−Sm−As−F−O组成的化合物。回答下列问题:
(1)AsH3的中心原子的杂化轨道类型为___________ ,H2O沸点比H2S的___________ (填“高”或“低”),其判断理由是___________ ,BF3的立体构型为___________ 。
(2)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为___________ 。
(3)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。图中F−和O2−共同占据晶胞的上下底面位置,若两者的比例依次用x和1−x代表,则该化合物的化学式表示为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为( ),则原子3的坐标分别为
),则原子3的坐标分别为___________ 。

(1)AsH3的中心原子的杂化轨道类型为
(2)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为
(3)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。图中F−和O2−共同占据晶胞的上下底面位置,若两者的比例依次用x和1−x代表,则该化合物的化学式表示为
 ),则原子3的坐标分别为
),则原子3的坐标分别为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】根据所学内容填空:
(1)有下列物质:①HF、②Cl2、③H2O、④CCl4、⑤BF3、⑥CO2,其中属于极性分子的是_______ (填序号,下同),既有 键又有
键又有 键的是
键的是_______ 。
(2)下列分子中,空间构型为正四面体且键角为 的是
的是_______ 。
a. b.
b. c.
c.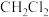 d.
d. e.
e. f.
f.
(3)H2O、 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是____ 。
(4)丙烯晴分子( )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为_______ 。
(5)VIA族元素氧、硫、硒( )的化合物在研究和生产中有许多重要用途。
)的化合物在研究和生产中有许多重要用途。
① 离子的空间构型为
离子的空间构型为_______ 。
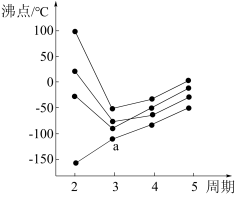
②如图所示,每条折线表示周期表IVA—VIIA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ (化学式)
(1)有下列物质:①HF、②Cl2、③H2O、④CCl4、⑤BF3、⑥CO2,其中属于极性分子的是
 键又有
键又有 键的是
键的是(2)下列分子中,空间构型为正四面体且键角为
 的是
的是a.
 b.
b. c.
c.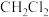 d.
d. e.
e. f.
f.
(3)H2O、
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(4)丙烯晴分子(
 )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为(5)VIA族元素氧、硫、硒(
 )的化合物在研究和生产中有许多重要用途。
)的化合物在研究和生产中有许多重要用途。①
 离子的空间构型为
离子的空间构型为②如图所示,每条折线表示周期表IVA—VIIA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】H与O可以形成H2O和H2O2两种化合物。请回答:
(1)H+可与H2O形成H3O+,H3O+的空间构型名称为_____ 。
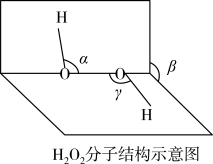
(2)H2O2分子结构如图所示,α、β、γ中相等的角是_____ ,H2O2是_____ 分子(填“极性”或“非极性”)。H2O2晶体中有4种作用力:①O-O键、②O-H键、③范德华力、④氢键,这4种作用力由强到弱依次为:_____ (用序号表示)。
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是_____ 。
A.Al3+ B.Mg2+ C.Cu2+ D.Mn2+ E.Fe2+
(4)实验测得,25℃时H2O2的pKa1小于H2O的pKa(pKa=-lgKa),原因是_____ (运用物质结构原理解释)。
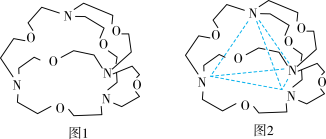
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是_____ (填标号)。
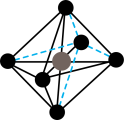
(6)SF6分子的空间结构为正八面体形,如图所示。1molSF6中含有_____ molS-F键,它的二氯代物SF4Cl2有_____ 种。
(1)H+可与H2O形成H3O+,H3O+的空间构型名称为
(2)H2O2分子结构如图所示,α、β、γ中相等的角是

(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是
A.Al3+ B.Mg2+ C.Cu2+ D.Mn2+ E.Fe2+
(4)实验测得,25℃时H2O2的pKa1小于H2O的pKa(pKa=-lgKa),原因是
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是

| A.CCl4 | B.CH4 | C.NH | D.H2O |

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硼是一种用途广泛的工业原料,除了用于生产硼砂、硼酸和硼的各种化合物外,在制备储氢材料方面也有重要的用途,试回答下列问题:
(1)Ti(BH4)3是一种储氢材料,由TiCl4和LiBH4反应制得。基态Ti原子的核外电子排布式为___________ , 的价层电子对数是
的价层电子对数是___________ 。
(2)过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为nd2n+2(n+1)sn-1,则Q元素的名称为___________ ;基态Q原子核外成对电子数和未成对电子数之比为___________ 。
(3)氨硼烷(NH3BH3)含氢量高,热稳定性好,是一种具有潜力的固体储氢材料,在四氢呋喃(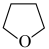 )作溶剂的条件下可合成氨硼烷:
)作溶剂的条件下可合成氨硼烷: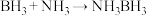 。
。
①测定晶体结构最常用的方法为___________ 。
②常温下,四氢呋喃在水中的溶解度大于环戊烷,其原因可能是___________ 。_
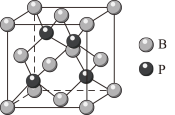
③硼与磷形成的一种晶体结构如图,晶体中离B原子最近的P原子有___________ 个;每个晶胞中的原子总数为___________ 。
(1)Ti(BH4)3是一种储氢材料,由TiCl4和LiBH4反应制得。基态Ti原子的核外电子排布式为
 的价层电子对数是
的价层电子对数是(2)过渡金属Q与镧形成的合金是一种储氢材料,其中基态Q原子的价电子排布式为nd2n+2(n+1)sn-1,则Q元素的名称为
(3)氨硼烷(NH3BH3)含氢量高,热稳定性好,是一种具有潜力的固体储氢材料,在四氢呋喃(
 )作溶剂的条件下可合成氨硼烷:
)作溶剂的条件下可合成氨硼烷: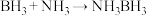 。
。①测定晶体结构最常用的方法为
②常温下,四氢呋喃在水中的溶解度大于环戊烷,其原因可能是
③硼与磷形成的一种晶体结构如图,晶体中离B原子最近的P原子有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s) KCl(l)+NaAlSi3O8(s)。
KCl(l)+NaAlSi3O8(s)。
(1)上述反应涉及的第三周期元素中,离子半径最小的是_______ (用元素符号表示)。Cl原子与Si原子可以形成的五核分子,其化学键长和键角都相等,则该物质为________ 分子(填“极性”或“非极性”)。
(2)表示原子或离子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式。从中选择最详尽描述核外电子运动状态的方式,来表示氧离子核外电子的运动状态:____________ 。
(3)上述元素的最高价氧化物对应水化物中,既能与强酸又能与强碱反应,其原因在于:__________ (用电离方程式表示)。
(4)Al与Cl可以形成分子晶体AlCl3,关于AlCl3溶液的说法错误的是___________ 。
A 水溶液中离子浓度大小:c(Cl-)>c(Al3+)> c(H+)>c(OH-)
B 升高温度,AlCl3水溶液pH减小,c(Al3+)减小
C c(Al3+)+c(H+)=c(Cl-)+c(OH-)
D c(Cl-)=3c(Al3+)+3c(AlO2-)
(5)不能用于比较Na与Al金属性相对强弱的事实是____________ 。
A 最高价氧化物对应水化物的碱性 B Na和AlCl3溶液反应
C 单质与H2O反应的难易程度 D 比较同浓度NaCl和AlCl3的pH值
(6)Na和O2反应形成Na2O和Na2O2的混合物,阴阳离子的个数比为____________ 。用电子式表示Na2O2的形成过程:_________
 KCl(l)+NaAlSi3O8(s)。
KCl(l)+NaAlSi3O8(s)。(1)上述反应涉及的第三周期元素中,离子半径最小的是
(2)表示原子或离子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式。从中选择最详尽描述核外电子运动状态的方式,来表示氧离子核外电子的运动状态:
(3)上述元素的最高价氧化物对应水化物中,既能与强酸又能与强碱反应,其原因在于:
(4)Al与Cl可以形成分子晶体AlCl3,关于AlCl3溶液的说法错误的是
A 水溶液中离子浓度大小:c(Cl-)>c(Al3+)> c(H+)>c(OH-)
B 升高温度,AlCl3水溶液pH减小,c(Al3+)减小
C c(Al3+)+c(H+)=c(Cl-)+c(OH-)
D c(Cl-)=3c(Al3+)+3c(AlO2-)
(5)不能用于比较Na与Al金属性相对强弱的事实是
A 最高价氧化物对应水化物的碱性 B Na和AlCl3溶液反应
C 单质与H2O反应的难易程度 D 比较同浓度NaCl和AlCl3的pH值
(6)Na和O2反应形成Na2O和Na2O2的混合物,阴阳离子的个数比为
您最近一年使用:0次
【推荐2】回答下列问题。
(1)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸常被用作碳包覆的碳源,其易溶于水的原因是___________ 。1mol抗坏血酸中手性碳原子的数目为___________ 。 分子的空间结构是平面四边形。它有两种空间异构体——俗称顺铂和反铂。其结构简式如图,在水中的溶解性大小为顺铂
分子的空间结构是平面四边形。它有两种空间异构体——俗称顺铂和反铂。其结构简式如图,在水中的溶解性大小为顺铂___________ (填“>”或“<”)反铂。 分子
分子___________ (填“具有”“不具有”)手性。
(3)根据等电子原理,写出两个与 具有相同空间结构的分子或离子
具有相同空间结构的分子或离子___________ 。
(4)已知苯酚(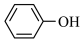 )具有弱酸性,其
)具有弱酸性,其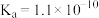 ;水杨酸离子(
;水杨酸离子( )能形成分子内氢键,据此判断相同温度下酸性强弱比较:水杨酸离子
)能形成分子内氢键,据此判断相同温度下酸性强弱比较:水杨酸离子___________ (填“>”或“<”)苯酚,其原因是___________ 。
(5)B、Al,Ga为同主族元素, ,
, 在一定条件下均易形成双聚分子,而
在一定条件下均易形成双聚分子,而 却很难形成双聚分子,其主要原因是
却很难形成双聚分子,其主要原因是 分子内形成了大
分子内形成了大 键,该大
键,该大 键可表示为
键可表示为___________ 。(分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)
键的电子数)
(1)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸常被用作碳包覆的碳源,其易溶于水的原因是

 分子的空间结构是平面四边形。它有两种空间异构体——俗称顺铂和反铂。其结构简式如图,在水中的溶解性大小为顺铂
分子的空间结构是平面四边形。它有两种空间异构体——俗称顺铂和反铂。其结构简式如图,在水中的溶解性大小为顺铂 分子
分子(3)根据等电子原理,写出两个与
 具有相同空间结构的分子或离子
具有相同空间结构的分子或离子(4)已知苯酚(
 )具有弱酸性,其
)具有弱酸性,其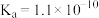 ;水杨酸离子(
;水杨酸离子( )能形成分子内氢键,据此判断相同温度下酸性强弱比较:水杨酸离子
)能形成分子内氢键,据此判断相同温度下酸性强弱比较:水杨酸离子(5)B、Al,Ga为同主族元素,
 ,
, 在一定条件下均易形成双聚分子,而
在一定条件下均易形成双聚分子,而 却很难形成双聚分子,其主要原因是
却很难形成双聚分子,其主要原因是 分子内形成了大
分子内形成了大 键,该大
键,该大 键可表示为
键可表示为 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)
键的电子数)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】我国科学家研发的全球首套千吨级太阳能燃料合成项目,为实现“碳中和”目标作出了重大贡献。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。
(1)钙钛矿( )型化合物是一类可用于生产太阳能电池的功能材料,
)型化合物是一类可用于生产太阳能电池的功能材料, 的晶胞如图所示。
的晶胞如图所示。
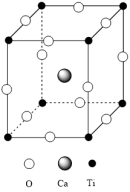
①基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
② 组成元素的电负性大小顺序是
组成元素的电负性大小顺序是_______ ;一个晶胞中含_______ O2-。
(2)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是_______ 。
(3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为 固溶体。在
固溶体。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为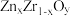 ,则y=
,则y=_______ (用含x的表达式)。
(1)钙钛矿(
 )型化合物是一类可用于生产太阳能电池的功能材料,
)型化合物是一类可用于生产太阳能电池的功能材料, 的晶胞如图所示。
的晶胞如图所示。
①基态
 原子的核外电子排布式为
原子的核外电子排布式为②
 组成元素的电负性大小顺序是
组成元素的电负性大小顺序是(2)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为
 固溶体。在
固溶体。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为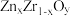 ,则y=
,则y=
您最近一年使用:0次



