下列事实与给出化学式的盐的水解有关的是
| A.浓FeCl3溶液可观察到丁达尔效应 | B.用CaSO4改良土壤的盐碱化 |
| C.用添加NaF的牙膏预防龋齿 | D.NaHSO4溶液呈酸性 |
更新时间:2022-01-24 14:58:46
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】对水进行下列操作,能抑制水的电离的是
| A.加入一小块Na | B.加入适量Ba(OH)2溶液 |
| C.升温至60℃ | D.加入碳酸钠溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在溶液中,不能发生水解的离子是
| A.ClO- | B.CO | C.Fe3+ | D.SO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.1 mol硝基(—NO2)与46 g二氧化氮(NO2)所含的电子数均为23NA |
B.一定温度下,1 L 0.50 mol·L-1 NH4Cl溶液与2 L 0.25 mol·L-1 NH4Cl溶液中NH 的物质的量均小于0.5NA,且前者更少 的物质的量均小于0.5NA,且前者更少 |
| C.1 mol过氧化钠分别与足量CO2、SO2反应,转移的电子数均为2NA |
D.1L0.01 mol·L-1 溶液中, 溶液中, 和 和 的离子数目之和为0.01NA 的离子数目之和为0.01NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温常压下,48gO2和O3的混合气体中含有O原子数为3NA |
B.8.4gNaHCO3晶体中含有CO 数为0.1NA 数为0.1NA |
| C.将0.1molAlCl3溶于1L水中,所得溶液含有Al3+数为0.1NA |
| D.1molCl2被FeBr2溶液完全吸收,转移的电子总数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】如表是几种常见的酸的电离平衡常数(25°C):
下列离子方程式书写正确的是
| 酸 | H2CO3 | HClO |
| 电离常数 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=4.0×10-8 |
A.向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+ |
B.向Na2S2O3溶液中滴加足量的稀硝酸: +2H+=S↓+SO2↑+H2O +2H+=S↓+SO2↑+H2O |
C.向草酸溶液中加入少量NaOH溶液:OH-+H2C2O4= +H2O +H2O |
D.向100mL2mol·L-1的FeI2溶液中通入标准状况下5.6L的Cl2: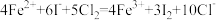 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】溴酸银(AgBrO3)溶解度随温度变化曲线如图所示。下列说法正确的是

| A.溴酸银的溶解是一个熵增、焓减过程 |
| B.对应温度下,X点的分散系中,v(溶解)>v(沉淀) |
| C.Y点的分散系中,c(Ag+)·c(BrO3-)>6.25×10-4 |
| D.60 ℃时溴酸银饱和溶液中c(BrO3-)=0.025mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】以软锰矿(主要成分是 ,含有
,含有 、
、 等杂质)制备高性能的磁性材料碳酸锰 (MnCO3)的基本工业流程如图:
等杂质)制备高性能的磁性材料碳酸锰 (MnCO3)的基本工业流程如图:

下列说法错误的是
 ,含有
,含有 、
、 等杂质)制备高性能的磁性材料碳酸锰 (MnCO3)的基本工业流程如图:
等杂质)制备高性能的磁性材料碳酸锰 (MnCO3)的基本工业流程如图:
下列说法错误的是
A.浸锰过程 发生反应的离子方程式: 发生反应的离子方程式: |
B.滤渣Ⅱ中主要成分为 |
C.氧化过程的目的是将过量的 消耗,将 消耗,将 氧化为 氧化为 |
D.沉锰过程发生的反应为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列离子方程式书写正确的是
A.NaHCO3溶液是常用的沉淀剂,向过量NaHCO3溶液中滴加饱和Ba(NO3)2溶液的离子方程式:Ba2++HCO  =BaCO3↓+H+ =BaCO3↓+H+ |
B.向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+NH +HSO +HSO =BaSO4↓+NH3•H2O+H2O =BaSO4↓+NH3•H2O+H2O |
C.硫酸铅溶解于浓盐酸中:PbSO4+4Cl-=[PbCl4]2-+SO |
D.用醋酸和淀粉-KI溶液检验加碘盐中的IO :IO :IO +I-+6H+=3I2+3H2O +I-+6H+=3I2+3H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列方案设计、现象和结论有不正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 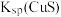 和 和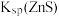 的比较 的比较 | 向含有ZnS的悬浊液中滴入少量的 溶液 溶液 | 出现黑色沉淀,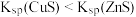 |
| B | 探究铝表面的氧化膜 | 将除去氧化膜的铝片放入盛有3mL浓硝酸的试管中,1min后取出铝片,用水洗净,再将其放入 硫酸铜溶液中,观察现象 硫酸铜溶液中,观察现象 | 铝片表面无明显现象,说明铝已被钝化 |
| C |  固体样品是否变质 固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液 溶液 | 若有白色沉淀产生,则样品已经变质 |
| D |  和 和 的 的 大小 大小 | 用pH试纸分别测  溶液和 溶液和 溶液的pH 溶液的pH | 若 则说明 则说明 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知:T℃时,Ksp(CaSO4)=4.90×10-5、Ksp(CaCO3)=2.8×10-9、Ksp(PbCO3)=8.4×10-14,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子)。下列说法错误的是


| A.a线是CaSO4沉淀溶解平衡曲线 |
B.T℃时,向10mL水中加入CaCO3和PbCO3至二者均饱和,溶液中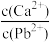 = =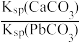 |
C.d点表示CaCO3的饱和溶液,且c(Ca2+)>c( ) ) |
| D.T℃时,向CaCO3沉淀中加入1mol•L-1的Na2SO4溶液,CaCO3沉淀会转化为CaSO4沉淀 |
您最近一年使用:0次

 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是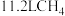 和
和 在光照条件下充分反应后的分子数为
在光照条件下充分反应后的分子数为
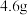 乙醇和二甲醚(
乙醇和二甲醚( )组成的混合物中,含有
)组成的混合物中,含有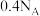 个
个 杂化的碳原子
杂化的碳原子 水溶液中阳离子个数小于
水溶液中阳离子个数小于
 中氙的价层电子对数为
中氙的价层电子对数为
 的硫酸钠溶液洗胃
的硫酸钠溶液洗胃 ,调节pH
,调节pH 溶液时,用稀盐酸溶解
溶液时,用稀盐酸溶解

