2L恒容密闭容器中发生反应: ,在不同温度下测得X的物质的量与时间的关系如表所示。下列说法正确的是
,在不同温度下测得X的物质的量与时间的关系如表所示。下列说法正确的是
 ,在不同温度下测得X的物质的量与时间的关系如表所示。下列说法正确的是
,在不同温度下测得X的物质的量与时间的关系如表所示。下列说法正确的是
 | 0 | 5 | 8 | 13 |
 | 2.0 | 1.5 | 1.3 | 1.2 |
 | 2.0 | 1.15 | 1.0 | 1.0 |
A.与 相比, 相比, 时活化分子百分数大 时活化分子百分数大 |
B. 下, 下,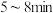 内, 内,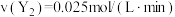 |
C. 下,反应在 下,反应在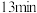 时已达到平衡状态 时已达到平衡状态 |
D.反应平衡常数: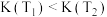 |
更新时间:2022-03-19 17:21:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列平衡体系中,当条件改变时,不能用勒夏特列原理来解释的事实是
A.N2(g)+3H2(g) 2NH3(g),高压有利于合成氨 2NH3(g),高压有利于合成氨 |
B.2NO2(g) N2O4(g) △H<0,升高温度颜色加深 N2O4(g) △H<0,升高温度颜色加深 |
C.Cl2+H2O HCl+HClO,氯水中当加入AgNO3溶液后,溶液颜色变浅 HCl+HClO,氯水中当加入AgNO3溶液后,溶液颜色变浅 |
D.H2、I2、HI平衡混合气体加压后颜色加深H2(g)+I2(g) 2HI(g) 2HI(g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验方案中能达到相应实验目的的是
| A | B | C | D | |
| 方案 |  | 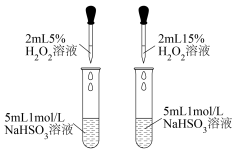 |  取铁电极附近溶液滴加铁氰化钾 |  将NO2球分别浸泡在冷水和热水中 |
| 目的 | 证明 比 比 更难溶 更难溶 | 探究浓度对化学反应速率的影响 | 证明 能在该条件下发生析氢腐蚀 能在该条件下发生析氢腐蚀 | 探究温度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】利用CH4可消除NO2的污染,反应原理为:CH4(g)+2NO2(g) ⇌ N2(g) + CO2(g) +2H2O(g),在10L密闭容器中分别加入0.50mol CH4 和1.2mol NO2,测得不同温度下 n(CH4)随时间变化的有关实验数据如表所示,下列说法正确的是
| 组别 | 温度/K | 时间/min 物质的量/mol | 0 | 10 | 20 | 40 | 50 |
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | M | 0.15 |
| A.由实验数据可知温度 T 1<T2 |
| B.组别①中 0 ~20 min 内,NO2 降解速率为0.0125 mol•L-1•min-1 |
| C.40 min 时,表格中 M 对应的数据为 0.18 |
| D.该反应只有在高温下才能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在温度t1和t2下,X2(g)和H2反应生成HX的平衡常数如下表

根据K的变化,结合已有知识推测,随着卤素原子核电荷数的降低下列说法不正确的是

根据K的变化,结合已有知识推测,随着卤素原子核电荷数的降低下列说法不正确的是
| A.在相同条件下,平衡时X2的转化率逐渐升高 |
| B.X2与H2反应的剧烈程度逐渐减弱 |
| C.HX的还原性逐渐减弱 |
| D.HX的生成为放热反应,由此可知t1<t2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】T℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积分数与时间的关系如图2所示。则下列结论正确的是
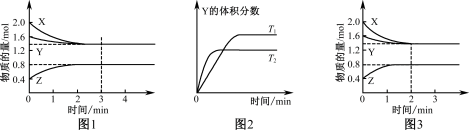

| A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol/(L·min) |
| B.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| C.保持温度和容器体积不变,4min时再向容器中充入2.0 mol X和1.6 mol Y及0.4 mol Z,达到平衡时,X的转化率增大 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
您最近一年使用:0次



 2Z(g)的平衡状态下,保持恒温恒容向容器中加入一定量的Y,下列说法正确的是(K为平衡常数,Q为浓度熵)
2Z(g)的平衡状态下,保持恒温恒容向容器中加入一定量的Y,下列说法正确的是(K为平衡常数,Q为浓度熵)

