大气层中臭氧分解反应历程如图所示,下列说法正确的是
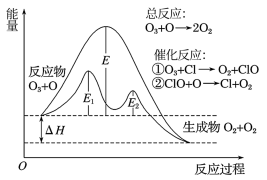

| A.因总反应为放热反应,故催化反应①②也均为放热反应 |
| B.决定O3分解反应速率的是催化反应② |
| C.催化剂为Cl,降低活化能,加快了臭氧分解反应速率 |
| D.温度升高,总反应的正反应速率的增加幅度小于逆反应速率的增加幅度,且平衡常数增大 |
更新时间:2022-03-21 12:23:03
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.原电池的电极材料中必须至少有一极是金属 |
| C.牺牲阳极法是利用了电解原理 |
| D.用电解法实现铁上镀铜,铜作阳极,铁作阴极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知反应: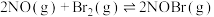
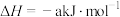 (
( ),其反应机理如下:
),其反应机理如下:
①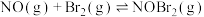 快
快
②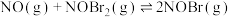 慢
慢
下列有关该反应的说法正确的是
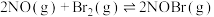
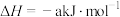 (
( ),其反应机理如下:
),其反应机理如下:①
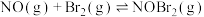 快
快②
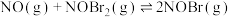 慢
慢下列有关该反应的说法正确的是
| A.该反应的速率主要取决于①的快慢 | B.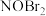 是该反应的催化剂 是该反应的催化剂 |
| C.正反应的活化能比逆反应的活化能大 | D.增大 浓度能加快反应速率 浓度能加快反应速率 |
您最近一年使用:0次
【推荐1】工厂的氨氮废水可用电化学催化氧化法加以处理,其中NH3在电极表面的氧化过程的微观示意图如图:
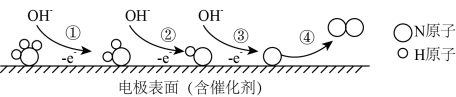
下列说法中,不正确的是

下列说法中,不正确的是
| A.过程①②均有N-H键断裂 |
B.过程③的电极反应式为: |
| C.过程④中没有非极性键形成 |
| D.催化剂可以降低该反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】我国学者通过局域晶态氮化碳调控*OCCHO中间体路径实现光催化选择性还原CO制取CH3CHO,在不同催化剂(HCN、HCN-A)作用下其反应历程中能量变化如图所示(部分物质省略),其中HCN-A表现出优异的催化性能。
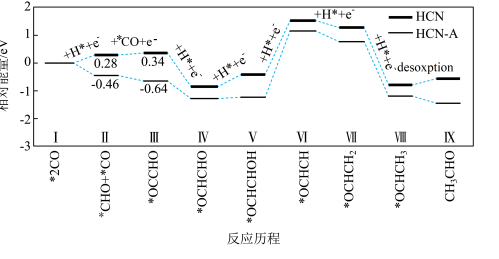
下列说法错误的是

下列说法错误的是
| A.步骤Ⅲ→Ⅳ过程中存在C-H的形成 |
| B.*CO转化为CH3CHO的反应为放热反应 |
| C.决定*CO→CH3CHO反应速率的步骤是Ⅵ→Ⅶ |
| D.HCN-A优于HCN的重要原因之一是*CHO和*CO生成*OCCHO的△H<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】二甲醚( )是一种重要的清洁燃料,可代替氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚,发生的反应为
)是一种重要的清洁燃料,可代替氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚,发生的反应为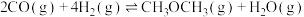 。下列说法正确的是
。下列说法正确的是
 )是一种重要的清洁燃料,可代替氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚,发生的反应为
)是一种重要的清洁燃料,可代替氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚,发生的反应为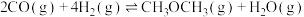 。下列说法正确的是
。下列说法正确的是
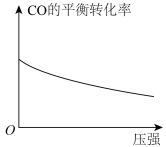
| A.CO的平衡转化率随压强的变化如图所示 |
B.该反应中,每消耗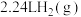 ,同时生成 ,同时生成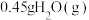 |
C.加入合适的催化剂,有利于提高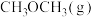 的平衡产率 的平衡产率 |
| D.保持其他条件不变,仅适当升高温度,该反应的活化分子百分数一定增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知溶液中存在平衡: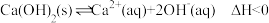 ,下列有关该平衡体系的说法正确的是
,下列有关该平衡体系的说法正确的是
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的 溶液
溶液
④恒温下,向悬浊液中加入 ,溶液的
,溶液的 变大
变大
⑤给溶液加热,溶液的 升高
升高
⑥向溶液中加入 溶液,其中固体质量增加
溶液,其中固体质量增加
⑦向溶液中加入少量 固体,
固体, 固体质量不变
固体质量不变
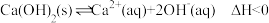 ,下列有关该平衡体系的说法正确的是
,下列有关该平衡体系的说法正确的是①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的
 溶液
溶液④恒温下,向悬浊液中加入
 ,溶液的
,溶液的 变大
变大⑤给溶液加热,溶液的
 升高
升高⑥向溶液中加入
 溶液,其中固体质量增加
溶液,其中固体质量增加⑦向溶液中加入少量
 固体,
固体, 固体质量不变
固体质量不变| A.①⑥ | B.①④⑥ | C.②③④⑥ | D.①②⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验装置或操作不能达到实验目的的是
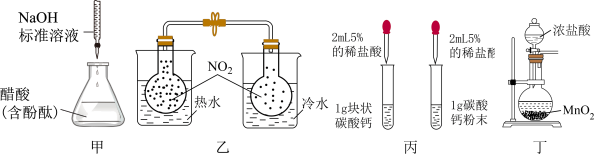

| A.图甲:测定醋酸的浓度 |
| B.图乙:探究温度对化学平衡的影响 |
| C.图丙:探究反应物的接触面积对反应速率的影响 |
| D.图丁:实验室制取氯气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列选项中的原因或结论与现象不对应的是
| 选项 | 现象 | 原因或结论 |
| A | 在H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
| B | 向5mL0.005mol/LFeCl3溶液中加入5mL0.010mol/LKSCN溶液,溶液呈红色,再滴加几滴KCl溶液,溶液颜色变浅 | 增大生成物浓度,平衡向逆反应方向移动 |
| C | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 2NO2(g) N2O4(g),△H<0,平衡向生成NO2方向移动 N2O4(g),△H<0,平衡向生成NO2方向移动 |
| D | 在密闭容器中有反应:A(?)+xB(g) 3C(g),达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的2倍,测得c(A)为0.2mol/L 3C(g),达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的2倍,测得c(A)为0.2mol/L | A为气体,x<2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】研究表明N2O与CO在Fe+作用下发生可逆反应的能量变化及反应历程如图所示。下列说法不正确的是
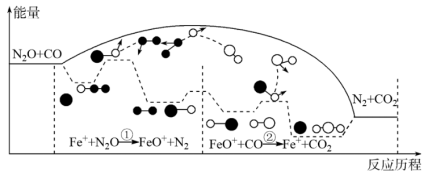

| A.总反应速率由反应①的速率决定 |
| B.反应中Fe+的存在可以增加活化分子百分数 |
| C.当反应中转移1mole-时,生成N2的体积为标况下22.4L |
| D.其他条件不变时,升高温度,总反应的平衡常数K减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
| A.2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0 |
| B.对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
C.CH3COOH 溶液加水稀释后,溶液中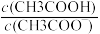 的值增大 的值增大 |
| D.Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解向左移动,溶液的pH 增大 |
您最近一年使用:0次


 I
I (aq)。某I2、KI混合溶液中,I
(aq)。某I2、KI混合溶液中,I


