葡萄糖酸锌(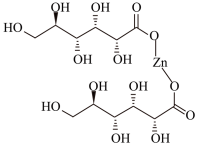 )为有机锌补剂,对胃黏膜刺激小,在体内易被人体吸收,且吸收率高,溶解性好。回答下列问题:
)为有机锌补剂,对胃黏膜刺激小,在体内易被人体吸收,且吸收率高,溶解性好。回答下列问题:
(1)锌元素位于元素周期表_______ 区,锌离子的价电子排布式为_______ 。
(2)葡萄糖酸锌组成元素中电负性最强的元素为_______ ,该元素的单质中属于极性分子的是_______ 。
(3)葡萄糖酸中C原子的杂化方式为_______ ,1 mol葡萄糖分子中含有_______ mol  键。
键。
(4)葡萄糖酸锌溶于氨水能生成 ,离子中配体为
,离子中配体为_______ ,与配体空间构型相同的阳离子为_______ 。
(5)葡萄糖酸易溶于水的原因是_______ ,葡萄糖酸的熔点_______ (填“大于”“小于”或“等于”)葡萄糖酸锌的熔点。
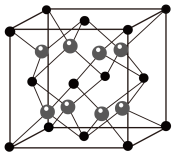
(6)若用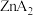 代表葡萄糖酸锌(相对分子质量为456),其晶胞结构如图所示,若晶胞参数为a nm,晶体密度为
代表葡萄糖酸锌(相对分子质量为456),其晶胞结构如图所示,若晶胞参数为a nm,晶体密度为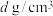 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为_______ (列出计算式即可)。
 )为有机锌补剂,对胃黏膜刺激小,在体内易被人体吸收,且吸收率高,溶解性好。回答下列问题:
)为有机锌补剂,对胃黏膜刺激小,在体内易被人体吸收,且吸收率高,溶解性好。回答下列问题:(1)锌元素位于元素周期表
(2)葡萄糖酸锌组成元素中电负性最强的元素为
(3)葡萄糖酸中C原子的杂化方式为
 键。
键。(4)葡萄糖酸锌溶于氨水能生成
 ,离子中配体为
,离子中配体为(5)葡萄糖酸易溶于水的原因是
(6)若用
 代表葡萄糖酸锌(相对分子质量为456),其晶胞结构如图所示,若晶胞参数为a nm,晶体密度为
代表葡萄糖酸锌(相对分子质量为456),其晶胞结构如图所示,若晶胞参数为a nm,晶体密度为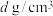 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为
2022·全国·模拟预测 查看更多[1]
(已下线)高考化学预测卷(六)
更新时间:2022-03-24 18:22:36
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】金属锂及其化合物因独特的性质而具有重要的应用价值。例如:锰酸锂可用于电池; Li2O 可用于特种玻璃、陶瓷、医药等领域: LiH、LiBH4、LiNH2为常见的储氢材料等。回答下列问题:
(1)Mn2+最外层电子排布式___________
(2)LiH、LiBH4、 LiNH2中所含非金属元素的电负性由小到大的顺序为___________ (用元素符号表示); LiBH4中阴离子的空间构型为___________
(3)Li2O的熔点(1567℃)高于LiCl的熔点(605℃)的原因是___________ 。
(4)Li2O立方晶胞结构如图所示,晶胞边长为anm。Li+在晶胞中的配位数为___________ ;Li+和O2-的最短距离为___________ nm。

(1)Mn2+最外层电子排布式
(2)LiH、LiBH4、 LiNH2中所含非金属元素的电负性由小到大的顺序为
(3)Li2O的熔点(1567℃)高于LiCl的熔点(605℃)的原因是
(4)Li2O立方晶胞结构如图所示,晶胞边长为anm。Li+在晶胞中的配位数为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】一种回收锌电解阳极泥(主要成分为 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
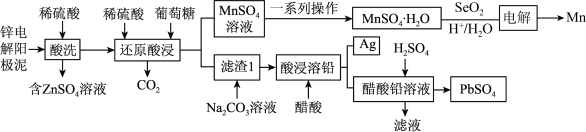
和 )中金属元素铰、锰、铅和银的工艺如图所示。回答下列问题:
)中金属元素铰、锰、铅和银的工艺如图所示。回答下列问题:
已知:① 易溶于水,不溶于乙醇;
易溶于水,不溶于乙醇;
②在较高温度及酸性催化条件下,葡萄糖( )能发生如下反应:
)能发生如下反应: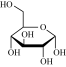
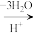
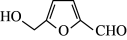
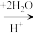
 +HCOOH。
+HCOOH。
(1)基态 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有______ 种。
(2)“还原酸浸”过程中二氧化锰参与反应的化学方程式为_______ 。
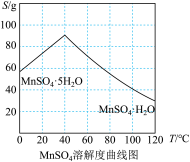
(3)结合 溶解度曲线图分析,由
溶解度曲线图分析,由 溶液制得
溶液制得 晶体的“一系列操作”是
晶体的“一系列操作”是______ 、_______ ,用_______ (填物质的名称)洗涤、干燥。
(4)实际锰浸出最适宜的葡萄糖加入量远大于理论加入量,其原因是_______ 。
(5)酸浸溶铅时用醋酸,其相对分子质量和硝酸相近,但醋酸熔点大于硝酸,原因是______ 。
(6)“电解”时,加入 与水反应生成二元弱酸
与水反应生成二元弱酸 ,在阴极放电生成
,在阴极放电生成 单质,有利于
单质,有利于 电还原沉积,则
电还原沉积,则 放电的电极反应式为
放电的电极反应式为______ 。
 和
和 ,还有少量锰铅氧化物
,还有少量锰铅氧化物 和
和 )中金属元素铰、锰、铅和银的工艺如图所示。回答下列问题:
)中金属元素铰、锰、铅和银的工艺如图所示。回答下列问题:
已知:①
 易溶于水,不溶于乙醇;
易溶于水,不溶于乙醇;②在较高温度及酸性催化条件下,葡萄糖(
 )能发生如下反应:
)能发生如下反应:
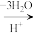

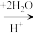
 +HCOOH。
+HCOOH。(1)基态
 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有(2)“还原酸浸”过程中二氧化锰参与反应的化学方程式为
(3)结合
 溶解度曲线图分析,由
溶解度曲线图分析,由 溶液制得
溶液制得 晶体的“一系列操作”是
晶体的“一系列操作”是
(4)实际锰浸出最适宜的葡萄糖加入量远大于理论加入量,其原因是
(5)酸浸溶铅时用醋酸,其相对分子质量和硝酸相近,但醋酸熔点大于硝酸,原因是
(6)“电解”时,加入
 与水反应生成二元弱酸
与水反应生成二元弱酸 ,在阴极放电生成
,在阴极放电生成 单质,有利于
单质,有利于 电还原沉积,则
电还原沉积,则 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有七种元素A、B、C、D、E、F、G,其中A、B、C为三个不同周期的短周期元素,E、F、G为第四周期元素。请根据下列相关信息,回答问题。
(1)C基态原子中能量最高的电子,其电子云在空间有___ 个方向,原子轨道呈___ 形,C简单离子核外有__ 种运动状态不同的电子。
(2)A2B2难溶于CS2,简要说明理由:__ 。
(3)G位于__ 族__ 区,它的一种氧化物常用于工业生产硫酸的催化剂,已知G在该氧化物中的化合价等于其价电子数,则该氧化物的化学式为___ 。
(4)ED3分子的VSEPR模型名称为__ ,其中E原子的杂化轨道类型为__ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数与s电子数相等 |
| C基态原子的价电子排布为nsn-1npn+1 |
| D的能层数与C相同,且电负性比C大 |
| E元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第五列 |
(2)A2B2难溶于CS2,简要说明理由:
(3)G位于
(4)ED3分子的VSEPR模型名称为
您最近一年使用:0次
【推荐1】中国近代化学启蒙者徐寿首次把“Nitrogen”译成中文时曾写成淡气”,意指它“冲淡”了空气中的氧气。含氮化合物种类繁多,用途广泛,根据信息回答下列问题。
(1)GaN是第三代半导体材料,基态Ga的电子排布式为___________ ,GaN晶体为共价键空间网状结构,熔点1700℃,晶体类型为___________ 。
(2)硫酸四氨合铂[Pt(NH3)4]SO4在工业上用于镀铂,Pt的配位数为___________ ,其阴离子的空间构型为___________ 。
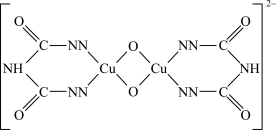
(3)氨缩脲与胆矾溶液反应得到如图所示的紫色离子,离子中C的杂化类型是___________ 。O的第二电离能比N第二电离能更大,解释其原因是___________ 。___________ 。[N(CH3)3]易与H+形成三甲胺正离子,反应中形成的化学键属于___________ 。
A.氢键 B.极性键 C.π键 D.配位键
(5)某铁氮化合物晶体的晶胞结构如图所示。___________ 。
②若晶胞中距离最近的两个铁原子距离为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为___________ g/cm3(列出计算式即可)。
(1)GaN是第三代半导体材料,基态Ga的电子排布式为
(2)硫酸四氨合铂[Pt(NH3)4]SO4在工业上用于镀铂,Pt的配位数为
(3)氨缩脲与胆矾溶液反应得到如图所示的紫色离子,离子中C的杂化类型是
A.氢键 B.极性键 C.π键 D.配位键
(5)某铁氮化合物晶体的晶胞结构如图所示。
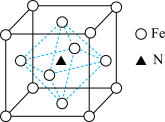
②若晶胞中距离最近的两个铁原子距离为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为___________ ,其固体的晶体类型为___________ 。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为___________ (填化学式,下同),还原性由强到弱的顺序为___________ ,键角由大到小的顺序为___________ 。
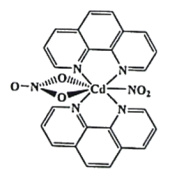
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1mol该配合物中通过螯合作用形成的配位键有___________ mol,该螯合物中N的杂化方式有___________ 种。
(1)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4.常温常压下SnCl4为无色液体,SnCl4空间构型为
(2)NH3、PH3、AsH3的沸点由高到低的顺序为
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1mol该配合物中通过螯合作用形成的配位键有

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知 、
、 、
、 、
、 、
、 都是元素周期表中前四周期的元素,它们的核电荷数依次增大。其中
都是元素周期表中前四周期的元素,它们的核电荷数依次增大。其中 与
与 、
、 与
与 在周期表中相邻,
在周期表中相邻, 原子核外有两个未成对电子,
原子核外有两个未成对电子, 的第一电离能比同周期相邻两种元素的都大,
的第一电离能比同周期相邻两种元素的都大, 原子在同周期元素原子中半径最大(稀有气体原子除外);
原子在同周期元素原子中半径最大(稀有气体原子除外); 与
与 位于不同周期,
位于不同周期, 原子核外最外层电子数与
原子核外最外层电子数与 相同,其余各电子层均充满电子。请根据以上信息,回答下列问题。
相同,其余各电子层均充满电子。请根据以上信息,回答下列问题。
(1) 、
、 、
、 、
、 四种元素的电负性由大到小的排列顺序为
四种元素的电负性由大到小的排列顺序为_________ 。
(2) 的氢化物的结构式为
的氢化物的结构式为_________ ,其分子的空间构型为________ 。
(3) 的某种化合物的结构如图所示,已知微粒间的相互作用包括化学键和分子间作用力,则此化合物中各种粒子间的相互作用力有
的某种化合物的结构如图所示,已知微粒间的相互作用包括化学键和分子间作用力,则此化合物中各种粒子间的相互作用力有___________ 。

(4) 与
与 的气态氢化物相比,
的气态氢化物相比,_________ (填化学式,下同)的沸点更高; 与
与 的气态氢化物相比,
的气态氢化物相比,________ 的沸点更高。
(5) 的稳定氧化物中,中心原子采取
的稳定氧化物中,中心原子采取________ 杂化,该氧化物分子的空间构型为______ 。
 、
、 、
、 、
、 、
、 都是元素周期表中前四周期的元素,它们的核电荷数依次增大。其中
都是元素周期表中前四周期的元素,它们的核电荷数依次增大。其中 与
与 、
、 与
与 在周期表中相邻,
在周期表中相邻, 原子核外有两个未成对电子,
原子核外有两个未成对电子, 的第一电离能比同周期相邻两种元素的都大,
的第一电离能比同周期相邻两种元素的都大, 原子在同周期元素原子中半径最大(稀有气体原子除外);
原子在同周期元素原子中半径最大(稀有气体原子除外); 与
与 位于不同周期,
位于不同周期, 原子核外最外层电子数与
原子核外最外层电子数与 相同,其余各电子层均充满电子。请根据以上信息,回答下列问题。
相同,其余各电子层均充满电子。请根据以上信息,回答下列问题。(1)
 、
、 、
、 、
、 四种元素的电负性由大到小的排列顺序为
四种元素的电负性由大到小的排列顺序为(2)
 的氢化物的结构式为
的氢化物的结构式为(3)
 的某种化合物的结构如图所示,已知微粒间的相互作用包括化学键和分子间作用力,则此化合物中各种粒子间的相互作用力有
的某种化合物的结构如图所示,已知微粒间的相互作用包括化学键和分子间作用力,则此化合物中各种粒子间的相互作用力有
(4)
 与
与 的气态氢化物相比,
的气态氢化物相比, 与
与 的气态氢化物相比,
的气态氢化物相比,(5)
 的稳定氧化物中,中心原子采取
的稳定氧化物中,中心原子采取
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】2017年4月26日,海军成立68周年时,我国第一艘国产航母成功下水。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢抗腐蚀性能强,Ni2+最高能级电子的运动状态有_________ 种,铬元素在周期表中_____ 区。
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如下图所示),其中C原子杂化方式为__________ 杂化。

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是__________ (填元素符号)
②根据价层电子对互斥理论,预测ClO3-的空间构型为__________ 形,写出一个C1O3-的等电子体的化学符号__________________ 。
③已知高碘酸有两种形式,化学式分别为H5IO6( )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_________ HIO4(填“>”“<”或“= ”)
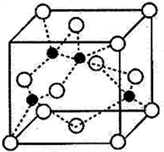
(4)海底金属软泥是在洋海底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、氧化铁、锰、锌等。Zn2+与S2-形成的一种晶体结构如图所示(黑球表示Zn2+,白球表示S2-)。则该晶体中与Zn2+等距且最近的S2-形成的立体图形为______________________ 。已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,该晶体中Zn2+和S2-原子之间的最短距离为体对角线的1/4,则该晶体中S2-和Zn2+之间的最短距离为__________________ pm。(写出计算式即可)
(1)镍铬钢抗腐蚀性能强,Ni2+最高能级电子的运动状态有
(2)航母甲板涂有一层耐高温的材料聚硅氧烷(结构如下图所示),其中C原子杂化方式为

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
③已知高碘酸有两种形式,化学式分别为H5IO6(
 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6(4)海底金属软泥是在洋海底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、氧化铁、锰、锌等。Zn2+与S2-形成的一种晶体结构如图所示(黑球表示Zn2+,白球表示S2-)。则该晶体中与Zn2+等距且最近的S2-形成的立体图形为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________ (填标号,下同),用光谱仪可捕捉到发射光谱的是___________ 。 中心原子为
中心原子为 ,
, 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大
中存在大 键(
键( )。
)。 中
中 原子的轨道杂化方式为
原子的轨道杂化方式为___________ ; 键角
键角___________  键角(填“>”“<”或“=”)。
键角(填“>”“<”或“=”)。
(3)镍能形成多种配合物,其中 是无色挥发性液体,
是无色挥发性液体,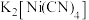 是红黄色单斜晶体。
是红黄色单斜晶体。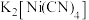 的熔点高于
的熔点高于 的原因是
的原因是___________ 。
(4)水催化氧化是“分子人工光合作用”的关键步骤。水的晶体有普通冰和重冰等不同类型。普通冰的晶胞结构与水分子间的氢键如图甲、乙所示。晶胞参数 ;标注为1、2、3的氧原子在Z轴的分数坐标分别为:
;标注为1、2、3的氧原子在Z轴的分数坐标分别为: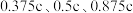 。晶胞中氢键的长度为
。晶胞中氢键的长度为___________  (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。 是重要的稀土抛光材料,图甲为理想的
是重要的稀土抛光材料,图甲为理想的 的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。
的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。 缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(
缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(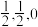 ),则氧空位处原子的分数坐标为
),则氧空位处原子的分数坐标为___________ ,该缺陷晶型的化学式可表示为___________ 。设阿伏加德罗常数的值为 ,
, 理想晶型的密度为
理想晶型的密度为 ,则
,则 原子与O原子的最近距离为
原子与O原子的最近距离为___________  (列出表达式)。
(列出表达式)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.  B.
B.
C. D.
D.
 中心原子为
中心原子为 ,
, 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大
中存在大 键(
键( )。
)。 中
中 原子的轨道杂化方式为
原子的轨道杂化方式为 键角
键角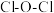 键角(填“>”“<”或“=”)。
键角(填“>”“<”或“=”)。(3)镍能形成多种配合物,其中
 是无色挥发性液体,
是无色挥发性液体,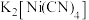 是红黄色单斜晶体。
是红黄色单斜晶体。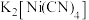 的熔点高于
的熔点高于 的原因是
的原因是(4)水催化氧化是“分子人工光合作用”的关键步骤。水的晶体有普通冰和重冰等不同类型。普通冰的晶胞结构与水分子间的氢键如图甲、乙所示。晶胞参数
 ;标注为1、2、3的氧原子在Z轴的分数坐标分别为:
;标注为1、2、3的氧原子在Z轴的分数坐标分别为: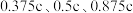 。晶胞中氢键的长度为
。晶胞中氢键的长度为 (列出数学表达式,不必计算出结果)。
(列出数学表达式,不必计算出结果)。
 是重要的稀土抛光材料,图甲为理想的
是重要的稀土抛光材料,图甲为理想的 的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。
的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在缺陷(如图乙)。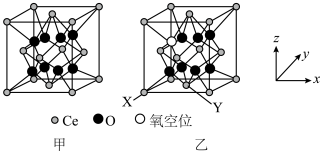
 缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(
缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分数坐标为(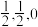 ),则氧空位处原子的分数坐标为
),则氧空位处原子的分数坐标为 ,
, 理想晶型的密度为
理想晶型的密度为 ,则
,则 原子与O原子的最近距离为
原子与O原子的最近距离为 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】按要求回答下列问题
(1)金刚石晶体中含有共价键形成的C原子环,其中最小的C环上有_______ 个C原子。
(2)CsCl晶体中每个Cs+周围有_________ 个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有________ 个。
(3)白磷分子中的键角为__________ ,分子的空间结构为__________ ,每个P原子与___ 个P原子结合成共价键。若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合_______ 个氧原子, 若每个P原子上的孤对电子再与氧原子配位,就可以得到磷的另一种氧化物_______________ (填分子式)。

(4)二氧化硅是一种________ 晶体,每个硅原子周围有_________ 个氧原子。
(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由_____ 个硼原子组成,共含有________ 个B-B键。
(1)金刚石晶体中含有共价键形成的C原子环,其中最小的C环上有
(2)CsCl晶体中每个Cs+周围有
(3)白磷分子中的键角为

(4)二氧化硅是一种
(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由
您最近一年使用:0次



