中国近代化学启蒙者徐寿首次把“Nitrogen”译成中文时曾写成淡气”,意指它“冲淡”了空气中的氧气。含氮化合物种类繁多,用途广泛,根据信息回答下列问题。
(1)GaN是第三代半导体材料,基态Ga的电子排布式为___________ ,GaN晶体为共价键空间网状结构,熔点1700℃,晶体类型为___________ 。
(2)硫酸四氨合铂[Pt(NH3)4]SO4在工业上用于镀铂,Pt的配位数为___________ ,其阴离子的空间构型为___________ 。
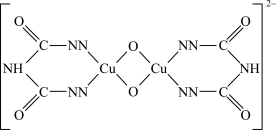
(3)氨缩脲与胆矾溶液反应得到如图所示的紫色离子,离子中C的杂化类型是___________ 。O的第二电离能比N第二电离能更大,解释其原因是___________ 。___________ 。[N(CH3)3]易与H+形成三甲胺正离子,反应中形成的化学键属于___________ 。
A.氢键 B.极性键 C.π键 D.配位键
(5)某铁氮化合物晶体的晶胞结构如图所示。___________ 。
②若晶胞中距离最近的两个铁原子距离为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为___________ g/cm3(列出计算式即可)。
(1)GaN是第三代半导体材料,基态Ga的电子排布式为
(2)硫酸四氨合铂[Pt(NH3)4]SO4在工业上用于镀铂,Pt的配位数为
(3)氨缩脲与胆矾溶液反应得到如图所示的紫色离子,离子中C的杂化类型是
A.氢键 B.极性键 C.π键 D.配位键
(5)某铁氮化合物晶体的晶胞结构如图所示。
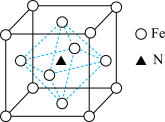
②若晶胞中距离最近的两个铁原子距离为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为
更新时间:2023-01-13 09:17:38
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】由H、C、O、N、S、Cu等元素能形成多种物质。这些物质有许多用途。请回答下列问题:
(1)基态Cu原子的价电子有_______ 种运动状态,未成对电子占据原子轨道的形状为_______ 。
(2)碳和氢形成的最简单碳正离子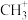 ,该阳离子的空间构型为
,该阳离子的空间构型为_______ 。
(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是_______ 。
(4)向盛有CuSO4溶液的试管中滴加少量氨水,离子反应方程式为_______ ;继续滴加氨水至过量得到深蓝色溶液。经测定深蓝色是由于存在[Cu(NH3)4]SO4。其阳离子的结构式为_______ 。
(5)金属晶体铜的晶胞如图所示。其堆积模型是_______ ,铜原子间的最短距离为apm,密度为ρg·cm-3,NA为阿伏加德罗常数。铜的相对原子质量为_______ (用a、ρ、NA表示,写出计算式即可)。

(1)基态Cu原子的价电子有
(2)碳和氢形成的最简单碳正离子
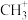 ,该阳离子的空间构型为
,该阳离子的空间构型为(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是
(4)向盛有CuSO4溶液的试管中滴加少量氨水,离子反应方程式为
(5)金属晶体铜的晶胞如图所示。其堆积模型是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】硫化物含硫量的测定、脱硫是极具价值的重要课题。
(1)稀土硫化物中硫含量的测定对其生产和质量控制具有重要意义。用如下方法对稀土硫化物中具有代表性的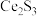 (
( 基态原子核外电子排布式为
基态原子核外电子排布式为 )样品硫含量进行测定。实验检测原理为
)样品硫含量进行测定。实验检测原理为
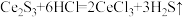
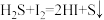

步骤1:称取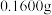 样品于反应瓶中,再准确滴加
样品于反应瓶中,再准确滴加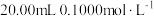 碘溶液;
碘溶液;
步骤2:缓慢滴加稍过量的稀盐酸(边滴加边摇动反应瓶),盖上瓶塞,剧烈摇动 ;
;
步骤3:滴入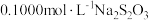 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液
溶液 。
。
①Ce元素最高正化合价为_______ 。
②步骤1中不能使用稀硝酸的原因是_______ 。
③该样品中硫的质量分数为_______ (写出计算过程)。
(2)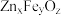 是一种复合脱硫剂,可用于脱除煤气中的
是一种复合脱硫剂,可用于脱除煤气中的 。
。
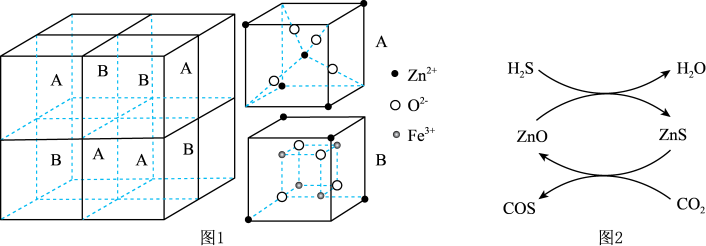
①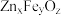 晶胞结构如图1所示(A、B分别为晶胞的
晶胞结构如图1所示(A、B分别为晶胞的 的结构),其化学式为
的结构),其化学式为_______ 。
②一定温度下将一定比例 和
和 的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到
的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到 。研究表明
。研究表明 参与了
参与了 与
与 生成
生成 的反应,反应机理如图2所示,反应前后
的反应,反应机理如图2所示,反应前后 的质量不变,该反应过程可描述为
的质量不变,该反应过程可描述为_______ 。
(1)稀土硫化物中硫含量的测定对其生产和质量控制具有重要意义。用如下方法对稀土硫化物中具有代表性的
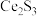 (
( 基态原子核外电子排布式为
基态原子核外电子排布式为 )样品硫含量进行测定。实验检测原理为
)样品硫含量进行测定。实验检测原理为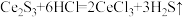
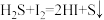

步骤1:称取
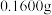 样品于反应瓶中,再准确滴加
样品于反应瓶中,再准确滴加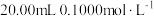 碘溶液;
碘溶液;步骤2:缓慢滴加稍过量的稀盐酸(边滴加边摇动反应瓶),盖上瓶塞,剧烈摇动
 ;
;步骤3:滴入
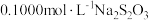 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液
溶液 。
。①Ce元素最高正化合价为
②步骤1中不能使用稀硝酸的原因是
③该样品中硫的质量分数为
(2)
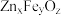 是一种复合脱硫剂,可用于脱除煤气中的
是一种复合脱硫剂,可用于脱除煤气中的 。
。
①
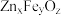 晶胞结构如图1所示(A、B分别为晶胞的
晶胞结构如图1所示(A、B分别为晶胞的 的结构),其化学式为
的结构),其化学式为②一定温度下将一定比例
 和
和 的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到
的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到 。研究表明
。研究表明 参与了
参与了 与
与 生成
生成 的反应,反应机理如图2所示,反应前后
的反应,反应机理如图2所示,反应前后 的质量不变,该反应过程可描述为
的质量不变,该反应过程可描述为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu2O。
(1)Cu2+基态核外电子排布式为_______ 。
(2)SO 的空间构型为
的空间构型为_______ (用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为_______ (填元素符号),配位体为_______ (填符号)。
(3)抗坏血酸的分子结构如图1所示,所含非氧官能团名称为_______ ;推测抗坏血酸在水中的溶解性:_______ (填“难溶于水”或“易溶于水”)。

(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为_______ 。

(1)Cu2+基态核外电子排布式为
(2)SO
 的空间构型为
的空间构型为(3)抗坏血酸的分子结构如图1所示,所含非氧官能团名称为

(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E五种元素,原子序数依次递增。A元素的周期数、主族数、原子序数相同;B元素的前六级电离能的数值变化如图所示:

C元素的基态原子核外有六种不同运动状态的价电子;D与B同主族,电负性D<B;E是第四周期d区元素,血红蛋白中的E元素更易与BC形成配合物E(BC)5。
(1)写出E的基态原子电子排布式________ 。
(2)A3C+中,C原子采用_____ 杂化,离子构型为_____ ,比较A3C+与A2C中的键角大小并解释原因_______ 。
(3)D60分子中每个D原子均采用sp2杂化,则1 molD60分子中π键的数目为____ 。
(4)A2C有多种晶体结构,其中一种晶体中分子的空间排列方式与金刚石晶体类似,该晶体晶胞中含有____ 个A2C分子,A2C的配位数为_____ ,A2C之间的作用力为_____ 。已知晶胞的棱长为a pm,阿伏加 德罗常数为NA,试列式计算此晶体的密度___ g·cm-3(用含a、NA的代数式表示)。
(5)E(BC)5中E周围的价电子总数为____ ,配位原子是_____ (填元素符号)。

C元素的基态原子核外有六种不同运动状态的价电子;D与B同主族,电负性D<B;E是第四周期d区元素,血红蛋白中的E元素更易与BC形成配合物E(BC)5。
(1)写出E的基态原子电子排布式
(2)A3C+中,C原子采用
(3)D60分子中每个D原子均采用sp2杂化,则1 molD60分子中π键的数目为
(4)A2C有多种晶体结构,其中一种晶体中分子的空间排列方式与金刚石晶体类似,该晶体晶胞中含有
(5)E(BC)5中E周围的价电子总数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】我国科学家首次用砷化镉纳米片观察到三维量子霍尔效应,并在碲化锆(ZrTe5)上发现了金属-绝缘体的转换,此项研究成果对红外探测等的研究具有应用价值。回答下列问题:
(1)基态As原子价电子排布图为_______ ,电子占据最高能级的电子云轮廓图形状为_______ 。
(2)AsH3的空间构型为_______ ;H3PO4分子中P的杂化轨道与O的_______ 轨道形成_______ 键。
(3)ZnS熔点为2830℃,CdS熔点为1750℃,ZnS熔点更高的原因是_______ 。
(4)碱式碳酸锆(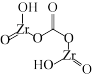 )中C原子的杂化方式为
)中C原子的杂化方式为_______ ;该化合物中非金属元素的第一电离能大小关系为_______ 。
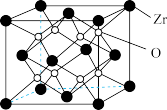
(5)氧化锆晶胞结构如图所示,其硬度极高,可用于陶瓷和耐火材料。晶胞中Zr原子的配位数为_______ ;已知阿伏加德罗常数的值为NA,若晶体的密度为ρg/cm3,则该晶胞中距离最近的两个锆原子之间的距离为_______ cm(列出计算式)。
(1)基态As原子价电子排布图为
(2)AsH3的空间构型为
(3)ZnS熔点为2830℃,CdS熔点为1750℃,ZnS熔点更高的原因是
(4)碱式碳酸锆(
 )中C原子的杂化方式为
)中C原子的杂化方式为(5)氧化锆晶胞结构如图所示,其硬度极高,可用于陶瓷和耐火材料。晶胞中Zr原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】副族元素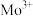 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液_______ ;锰在周期表中的_______ 区。
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为_______ 。
(3)副族元素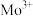 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是_______ ; 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是_______ (填元素符号),其中配体中C原子的杂化方式为_______ , 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为_______ 。
(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是_______ 。
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。_______ ;
② 的熔点
的熔点_______ (填“>”、“<”或“=”) ;
;
③若该八面体边长为 ,则晶胞的密度为
,则晶胞的密度为
_______  (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
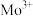 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液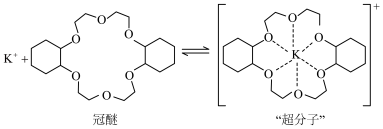
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为
(3)副族元素
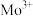 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。

②
 的熔点
的熔点 ;
;③若该八面体边长为
 ,则晶胞的密度为
,则晶胞的密度为
 (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】完成下列问题
(1)参考表中物质的熔点,问答有关问题。
①钠的卤化物熔点变化的原因是 _______ 。
②影响硅的卤化物熔点的因素是_______ 。
③钠的卤化物的熔点比相应的硅的卤化物的熔点高得多的原因是_______ 。
(2)向胆矾溶液中滴加氨水至过量,最终得到深蓝色的透明溶液,再加入乙醇后析出深蓝色晶体,写出生成深蓝色透明溶液的离子方程式:_______ 。该实验可知,与Cu2+结合生成配离子的稳定性: NH3_______ H2O(填 “>”或“<” )。
(3)我国科学家在新型二维半导体芯片材料——硒氧化铋的研究中取得突破性进展。硒氧化铋的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞参数为a pm,a pm,b pm。
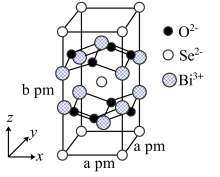
①该晶胞沿z轴方向的投影图为_______ (填标号)。
A. B.
B. C.
C. D.
D.
②该晶体中,每个 周围紧邻的
周围紧邻的 共有
共有_______ 个。
(1)参考表中物质的熔点,问答有关问题。
| 物质 | NaF | NaCl | NaBr | NaI |
| 熔点/℃ | 995 | 801 | 755 | 651 |
| 物质 | SiF4 | SiCl4 | SiBr4 | SiI4 |
| 熔点/℃ | −90.2 | −70.4 | 5.2 | 120.0 |
②影响硅的卤化物熔点的因素是
③钠的卤化物的熔点比相应的硅的卤化物的熔点高得多的原因是
(2)向胆矾溶液中滴加氨水至过量,最终得到深蓝色的透明溶液,再加入乙醇后析出深蓝色晶体,写出生成深蓝色透明溶液的离子方程式:
(3)我国科学家在新型二维半导体芯片材料——硒氧化铋的研究中取得突破性进展。硒氧化铋的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞参数为a pm,a pm,b pm。

①该晶胞沿z轴方向的投影图为
A.
 B.
B. C.
C. D.
D.
②该晶体中,每个
 周围紧邻的
周围紧邻的 共有
共有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】钛及其化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
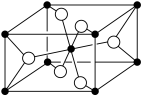
(1) 是一种储氢材料,B原子的杂化方式是
是一种储氢材料,B原子的杂化方式是________ , 含有
含有___________ (填序号)
①σ键 ②π键 ③氢键 ④配位键 ⑤离子键
研究表明, 加热释放氢的温度明显高于
加热释放氢的温度明显高于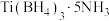 的加热释放氢的温度,其原因可能是
的加热释放氢的温度,其原因可能是___________ 。
(2) 中的
中的 具有强还原性,请从结构角度试解释原因
具有强还原性,请从结构角度试解释原因___________ 。在浓的 溶液中加入乙醚,并通入HCl至饱和,得到配位数为6、组成为
溶液中加入乙醚,并通入HCl至饱和,得到配位数为6、组成为 的绿色晶体,该晶体中两种配体的物质的量之比为2∶1,则该配离子的化学式为
的绿色晶体,该晶体中两种配体的物质的量之比为2∶1,则该配离子的化学式为___________ 。
(3)如图为具有较高催化活性材料金红石(钛的氧化物)的晶胞结构,其化学式为___________ ,判断其晶胞结构的最可靠科学方法是___________ 。
(1)
 是一种储氢材料,B原子的杂化方式是
是一种储氢材料,B原子的杂化方式是 含有
含有①σ键 ②π键 ③氢键 ④配位键 ⑤离子键
研究表明,
 加热释放氢的温度明显高于
加热释放氢的温度明显高于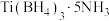 的加热释放氢的温度,其原因可能是
的加热释放氢的温度,其原因可能是(2)
 中的
中的 具有强还原性,请从结构角度试解释原因
具有强还原性,请从结构角度试解释原因 溶液中加入乙醚,并通入HCl至饱和,得到配位数为6、组成为
溶液中加入乙醚,并通入HCl至饱和,得到配位数为6、组成为 的绿色晶体,该晶体中两种配体的物质的量之比为2∶1,则该配离子的化学式为
的绿色晶体,该晶体中两种配体的物质的量之比为2∶1,则该配离子的化学式为(3)如图为具有较高催化活性材料金红石(钛的氧化物)的晶胞结构,其化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】Mn能改善钢材热加工性能,并改善钢材的冷脆倾向,同时不显著降低钢材的塑性、冲击韧性。根据要求回答下列问题:
(1) 的核外电子排布式为
的核外电子排布式为_______ ,
基态Mn原子能级最高的电子的电子云轮廓图形状为_______ 。
(2)Fe、Mn元素的部分电离能数据如下表:
从上表两元素部分电离能数据的比较可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,原因是
再失去一个电子难,原因是_______ 。
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与 形成黄色的配合物,其结构为
形成黄色的配合物,其结构为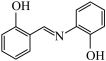 。
。
①锰试剂分子中,电负性最大的原子是_______ ,采取 杂化的原子是
杂化的原子是_______ ;
②锰试剂分子中能与 形成配位键的原子是
形成配位键的原子是_______ 。
(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),晶体结构不变。
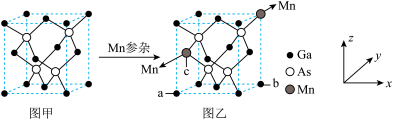
①图乙中a点和c点的原子坐标参数分别为(0,0,0)和 ,则b点的原子坐标参数为
,则b点的原子坐标参数为_______ ;
②设图甲晶体的密度为 ,设
,设 表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为
表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为_______ pm(用含 、
、 的关系式表示最简化的计算式即可)。
的关系式表示最简化的计算式即可)。
(1)
 的核外电子排布式为
的核外电子排布式为基态Mn原子能级最高的电子的电子云轮廓图形状为
(2)Fe、Mn元素的部分电离能数据如下表:
| 元素 | Fe | Mn | |
电离能/( ) ) |  | 759 | 717 |
 | 1561 | 1509 | |
 | 2957 | 3248 | |
 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,原因是
再失去一个电子难,原因是(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与
 形成黄色的配合物,其结构为
形成黄色的配合物,其结构为 。
。①锰试剂分子中,电负性最大的原子是
 杂化的原子是
杂化的原子是②锰试剂分子中能与
 形成配位键的原子是
形成配位键的原子是(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),晶体结构不变。

①图乙中a点和c点的原子坐标参数分别为(0,0,0)和
 ,则b点的原子坐标参数为
,则b点的原子坐标参数为②设图甲晶体的密度为
 ,设
,设 表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为
表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为 、
、 的关系式表示最简化的计算式即可)。
的关系式表示最简化的计算式即可)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氟化工被称为“黄金产业”,在国民经济和社会发展中占有重要地位。我国某公司利用萤石(主要成分为 ,及少量
,及少量 、
、 等)制备无水氟化铝的主要工艺流程如下所示。
等)制备无水氟化铝的主要工艺流程如下所示。 的熔点
的熔点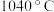 ,沸点
,沸点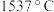 ;
;
③常温下, 。
。
请回答下列问题:
(1)在进入回转窑前,需要将萤石粉碎,其目的是_______ 。
(2)“回转窑反应”的温度控制在 之间,写出在回转窑获得
之间,写出在回转窑获得 的化学方程式:
的化学方程式:_______ 。
(3)在回转窑中的炉渣里还含有 ,将该物质在
,将该物质在 热分解,可获得两种气体(其中一种为
热分解,可获得两种气体(其中一种为 ),用多元醇选择性吸收产生的
),用多元醇选择性吸收产生的 气体,经过一系列工艺得到高纯
气体,经过一系列工艺得到高纯 。则多元醇能从两种气体中选择性吸收
。则多元醇能从两种气体中选择性吸收 的原理是
的原理是_______ 。
(4)经冷凝、精馏、脱气后的 与
与 在流化床、多级气流床中,在
在流化床、多级气流床中,在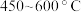 条件下进行一系列反应,由
条件下进行一系列反应,由 和
和 制备无水
制备无水 的反应的
的反应的 _______(填标号)。
_______(填标号)。
(5)常温下,向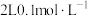 的
的 溶液中加入
溶液中加入 固体充分反应后可得
固体充分反应后可得 ,测得溶液中
,测得溶液中 的浓度为
的浓度为 ,则加入的
,则加入的 固体的物质的量为
固体的物质的量为_______ 。
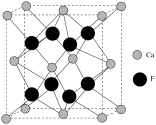
(6)已知萤石 立方晶胞参数
立方晶胞参数 ,结构如图所示,该
,结构如图所示,该 的晶体密度为
的晶体密度为_______  (列出计算式,设阿伏加德罗常数的值为
(列出计算式,设阿伏加德罗常数的值为 )。
)。
 ,及少量
,及少量 、
、 等)制备无水氟化铝的主要工艺流程如下所示。
等)制备无水氟化铝的主要工艺流程如下所示。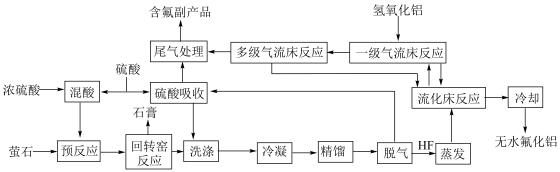
 的熔点
的熔点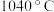 ,沸点
,沸点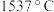 ;
;③常温下,
 。
。请回答下列问题:
(1)在进入回转窑前,需要将萤石粉碎,其目的是
(2)“回转窑反应”的温度控制在
 之间,写出在回转窑获得
之间,写出在回转窑获得 的化学方程式:
的化学方程式:(3)在回转窑中的炉渣里还含有
 ,将该物质在
,将该物质在 热分解,可获得两种气体(其中一种为
热分解,可获得两种气体(其中一种为 ),用多元醇选择性吸收产生的
),用多元醇选择性吸收产生的 气体,经过一系列工艺得到高纯
气体,经过一系列工艺得到高纯 。则多元醇能从两种气体中选择性吸收
。则多元醇能从两种气体中选择性吸收 的原理是
的原理是(4)经冷凝、精馏、脱气后的
 与
与 在流化床、多级气流床中,在
在流化床、多级气流床中,在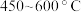 条件下进行一系列反应,由
条件下进行一系列反应,由 和
和 制备无水
制备无水 的反应的
的反应的 _______(填标号)。
_______(填标号)。| A.大于0 | B.小于0 | C.等于0 | D.无法确定 |
(5)常温下,向
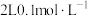 的
的 溶液中加入
溶液中加入 固体充分反应后可得
固体充分反应后可得 ,测得溶液中
,测得溶液中 的浓度为
的浓度为 ,则加入的
,则加入的 固体的物质的量为
固体的物质的量为(6)已知萤石
 立方晶胞参数
立方晶胞参数 ,结构如图所示,该
,结构如图所示,该 的晶体密度为
的晶体密度为 (列出计算式,设阿伏加德罗常数的值为
(列出计算式,设阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】我国科学家利用锰簇催化剂(Mn4CaOx,x代表氧原子数)解密光合作用。锰簇的可逆结构异构化反应如图。

请回答下列问题:
(1)基态氧原子价电子轨道表示式为______ 。基态钙原子中能量最高的电子所占据原子轨道的电子云轮廓图为______ 形。
(2)已知:在元素周期表中Mn、Cr相邻。第二电离能与第一电离能之差较小的是______ (填“Mn”或“Cr”),理由是______ 。
(3)在上述异构化反应中,1molA中由Mn形成的σ键有______ mol。
(4)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。
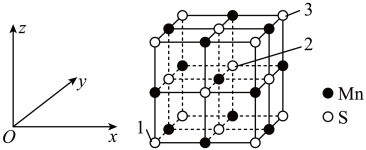
①Mn原子的配位数是______ ,距离Mn原子最近的Mn原子有______ 个。
②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在MnS晶胞坐标系中,1号S原子坐标为(0,0,0),3号S原子坐标为(1,1,1),则2号S原子坐标为______ 。
③已知:MnS晶体的密度为ρg•cm-3,NA为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为______ pm(列出计算式即可)。

请回答下列问题:
(1)基态氧原子价电子轨道表示式为
(2)已知:在元素周期表中Mn、Cr相邻。第二电离能与第一电离能之差较小的是
(3)在上述异构化反应中,1molA中由Mn形成的σ键有
(4)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。

①Mn原子的配位数是
②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在MnS晶胞坐标系中,1号S原子坐标为(0,0,0),3号S原子坐标为(1,1,1),则2号S原子坐标为
③已知:MnS晶体的密度为ρg•cm-3,NA为阿伏加德罗常数的值。则MnS晶胞中阴、阳离子最近距离为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
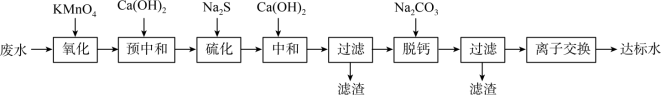
【推荐3】湿法炼锌的工业废水中主要阳离子有Zn2+、H+、Tl+、Tl3+,废水除铊的工艺流程如图。 能够在pH为0~14的范围内以离子态稳定存在,不易与
能够在pH为0~14的范围内以离子态稳定存在,不易与 形成沉淀。
形成沉淀。
②部分物质的 如表:
如表:
③排放标准:Tl的含量低于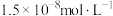 。
。
回答下列问题:
(1)Tl的原子序数为81,在元素周期表中的位置为___________ ,价电子排布式为___________ 。
(2)已知“氧化”步骤中 被还原为
被还原为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:___________ ,反应后仍存在少量的 。
。
(3)“预中和”步骤中加入 至溶液的pH约为7,可减少“硫化”步骤中
至溶液的pH约为7,可减少“硫化”步骤中 的使用量,还能减少
的使用量,还能减少___________ (填化学式)污染物的生成。
(4)“硫化”步骤的主要目的是除去___________ (填离子符号)。
(5)在“中和”步骤中,若要使溶液中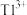 的含量低于排放标准,请根据
的含量低于排放标准,请根据 计算溶液的pH应大于
计算溶液的pH应大于___________ 。
(6)“离子交换”步骤中可用普鲁士蓝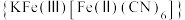 (其摩尔质量为
(其摩尔质量为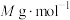 )中的
)中的 与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[
与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[ 未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为
未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为 ,则
,则 和
和 的最短距离为
的最短距离为___________ cm(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 能够在pH为0~14的范围内以离子态稳定存在,不易与
能够在pH为0~14的范围内以离子态稳定存在,不易与 形成沉淀。
形成沉淀。②部分物质的
 如表:
如表:| 物质 |  | 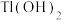 | ZnS |  |
 | 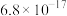 |  |  |  |
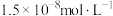 。
。回答下列问题:
(1)Tl的原子序数为81,在元素周期表中的位置为
(2)已知“氧化”步骤中
 被还原为
被还原为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式: 。
。(3)“预中和”步骤中加入
 至溶液的pH约为7,可减少“硫化”步骤中
至溶液的pH约为7,可减少“硫化”步骤中 的使用量,还能减少
的使用量,还能减少(4)“硫化”步骤的主要目的是除去
(5)在“中和”步骤中,若要使溶液中
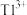 的含量低于排放标准,请根据
的含量低于排放标准,请根据 计算溶液的pH应大于
计算溶液的pH应大于(6)“离子交换”步骤中可用普鲁士蓝
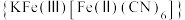 (其摩尔质量为
(其摩尔质量为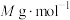 )中的
)中的 与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[
与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[ 未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为
未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为 ,则
,则 和
和 的最短距离为
的最短距离为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。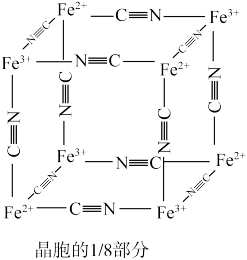
您最近一年使用:0次



