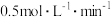以Cu/ZnO/Al2O3为催化剂,乙醇直接合成乙酸乙酯过程中发生的可逆反应如下:
C2H5OH(g)=CH3CHO(g)+H2(g);ΔH=59kJ·mol-1
2CH3CHO(g)+H2O(g)=C2H5OH(g)+CH3COOH(g);ΔH=-86kJ·mol-1
CH3COOH(g)+C2H5OH(g)=CH3COOC2H5(g)+H2O(g);ΔH=-25kJ·mol-1
2C2H5OH(g)=C2H5OC2H5(g)+H2O(g);ΔH=-44kJ·mol-1
其他条件相同,将无水乙醇经预热气化后以一定流速通过装有催化剂的反应管,将出口处收集到的乙酸乙酯、乙醛、乙醚、乙酸、乙醇冷凝,测得部分有机物占全部有机物的质量分数与反应温度的关系如图所示。下列说法正确的是

C2H5OH(g)=CH3CHO(g)+H2(g);ΔH=59kJ·mol-1
2CH3CHO(g)+H2O(g)=C2H5OH(g)+CH3COOH(g);ΔH=-86kJ·mol-1
CH3COOH(g)+C2H5OH(g)=CH3COOC2H5(g)+H2O(g);ΔH=-25kJ·mol-1
2C2H5OH(g)=C2H5OC2H5(g)+H2O(g);ΔH=-44kJ·mol-1
其他条件相同,将无水乙醇经预热气化后以一定流速通过装有催化剂的反应管,将出口处收集到的乙酸乙酯、乙醛、乙醚、乙酸、乙醇冷凝,测得部分有机物占全部有机物的质量分数与反应温度的关系如图所示。下列说法正确的是

| A.在250~300℃范围,乙醇的转化率随温度的升高而减小 |
| B.在200~325℃范围,乙醇生成乙醚的反应均已到达平衡 |
| C.在300~325℃范围,出口处氢气的量随温度的升高而减小 |
| D.研发使用催化活性高的催化剂有利于提高乙酸乙酯的平衡产率 |
2022·江苏·一模 查看更多[4]
(已下线)第七章 化学反应速率和化学平衡(测)-2023年高考化学一轮复习讲练测(全国通用)江苏省响水中学2021-2022学年高二下学期第二次学情分析考试化学试题(已下线)秘籍07 化学反应速率及平衡图象剖析-备战2022年高考化学抢分秘籍(全国通用)江苏省2022届高三下学期3月第一次调研测试化学试题
更新时间:2022-03-29 21:36:18
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】在恒容密闭容器中进行反应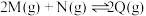
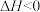 ,下列说法错误的是
,下列说法错误的是
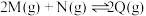
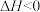 ,下列说法错误的是
,下列说法错误的是| A.正反应是熵减小的反应 |
| B.升高温度,平衡向右移动 |
| C.增大N(g)的浓度,M(g)的平衡转化率增大 |
| D.加入催化剂,反应速率增大,平衡状态不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】2022年诺贝尔化学奖授予了对点击化学和生物正交化学作出贡献的三位科学家。点击化学的代表反应为“叠氮化物-炔烃”反应,其反应原理如图所示(R1和R2代表烃基)。下列说法正确的是
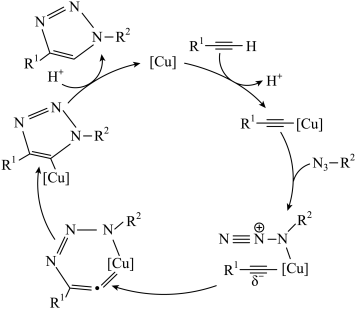

| A.转化过程中N的杂化方式未改变 |
| B.N3-R2中一定存在三种非极性键 |
| C.该反应中[Cu]和H+都能降低反应的活化能 |
D.总反应方程式为: |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】在 和
和 条件下,将一定量的
条件下,将一定量的 和
和 充入含有催化剂的密闭容器。测量容器内
充入含有催化剂的密闭容器。测量容器内 的浓度如下表所示。下列说法正确的是
的浓度如下表所示。下列说法正确的是
 和
和 条件下,将一定量的
条件下,将一定量的 和
和 充入含有催化剂的密闭容器。测量容器内
充入含有催化剂的密闭容器。测量容器内 的浓度如下表所示。下列说法正确的是
的浓度如下表所示。下列说法正确的是反应时间 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 100 |
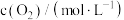 | 5 | 3.5 | 2.5 | 1.65 | 1 | 0.5 | 0.5 | 0.5 | 0.5 |
A.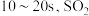 的平均反应速率为 的平均反应速率为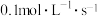 |
B.该反应一定在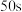 时才开始达到平衡 时才开始达到平衡 |
C.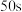 时, 时, 的转化率为 的转化率为 |
D.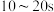 的平均反应速率比 的平均反应速率比 的慢,是因为反应物浓度减小 的慢,是因为反应物浓度减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】如图的曲线是表示其他条件一定时,2NO+O2 2NO2(正反应为放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态且v(正)>v(逆)的点是
2NO2(正反应为放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态且v(正)>v(逆)的点是
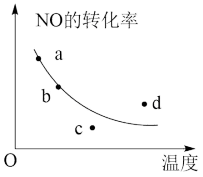
 2NO2(正反应为放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态且v(正)>v(逆)的点是
2NO2(正反应为放热反应)反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态且v(正)>v(逆)的点是
| A.a点 | B.b点 | C.c点 | D.d点 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】I2在KI溶液中存在平衡I2(aq)+I-(aq)  I
I (aq),某I2、KI混合溶液中,I
(aq),某I2、KI混合溶液中,I 的物质的量浓度c(I
的物质的量浓度c(I )与温度T的关系如图所示(曲线上任意一点都表示平衡状态)。下列说法正确的是
)与温度T的关系如图所示(曲线上任意一点都表示平衡状态)。下列说法正确的是
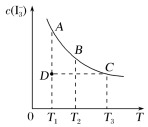
 I
I (aq),某I2、KI混合溶液中,I
(aq),某I2、KI混合溶液中,I 的物质的量浓度c(I
的物质的量浓度c(I )与温度T的关系如图所示(曲线上任意一点都表示平衡状态)。下列说法正确的是
)与温度T的关系如图所示(曲线上任意一点都表示平衡状态)。下列说法正确的是
A.反应I2(aq)+I-(aq)  I I (aq)的ΔH>0 (aq)的ΔH>0 |
| B.若温度为T1、T2时,平衡体系中I-的逆反应速率分别为v1、v2,则v1>v2 |
| C.若反应达到平衡状态,向混合溶液中加入KI固体,平衡向右移动 |
| D.状态D时,v正=v逆 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】甲烷是一种温室气体,将它转化为高附加值产品甲醇具有重要意义。目前工业上的甲烷转化大多需要先通过重整生成合成气(CO、 )再转化为甲醇,涉及的反应如下:
)再转化为甲醇,涉及的反应如下:
反应Ⅰ: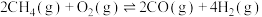

反应Ⅱ:
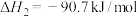
在密闭容器中通入3mol 和2mol
和2mol  ,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,其中
,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,其中 和
和 的平衡体积分数随温度变化如图所示。
的平衡体积分数随温度变化如图所示。

已知:对于反应Ⅱ, ,
, ,
, 、
、 为速率常数,只与温度有关,分压=总压×物质的量分数。下列说法不正确的是
为速率常数,只与温度有关,分压=总压×物质的量分数。下列说法不正确的是
 )再转化为甲醇,涉及的反应如下:
)再转化为甲醇,涉及的反应如下:反应Ⅰ:

反应Ⅱ:

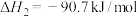
在密闭容器中通入3mol
 和2mol
和2mol  ,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,其中
,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,其中 和
和 的平衡体积分数随温度变化如图所示。
的平衡体积分数随温度变化如图所示。
已知:对于反应Ⅱ,
 ,
, ,
, 、
、 为速率常数,只与温度有关,分压=总压×物质的量分数。下列说法不正确的是
为速率常数,只与温度有关,分压=总压×物质的量分数。下列说法不正确的是A.压强为0.2MPa时,表示 和 和 的曲线分别是b、d 的曲线分别是b、d |
| B.混合气体的平均相对分子质量保持不变时,说明反应体系已达到平衡 |
C.在升温的过程中,反应Ⅱ速率常数增大的倍数; > > |
D.500K,2MPa条件下,若平衡时CO的物质的量为1mol,则 的转化率约为66.7% 的转化率约为66.7% |
您最近一年使用:0次

 通过增大反应的活化能来提高化学反应速率
通过增大反应的活化能来提高化学反应速率
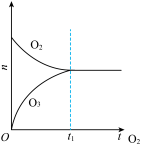
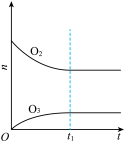
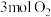 加入
加入 的反应器中,在高温下放电,经
的反应器中,在高温下放电,经 建立了平衡体系:
建立了平衡体系: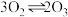 ,此时测知
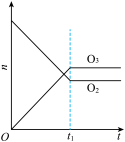
,此时测知 的转化率为30%,下列图像能正确表示气体的物质的量(n)与时间(t)的关系的是
的转化率为30%,下列图像能正确表示气体的物质的量(n)与时间(t)的关系的是
 温度下,向
温度下,向 恒容密闭容器中加入
恒容密闭容器中加入 固体,发生反应
固体,发生反应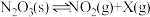 (未配平),反应过程如图,下列说法正确的是
(未配平),反应过程如图,下列说法正确的是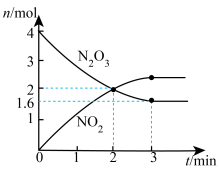

 时逆反应速率大于第
时逆反应速率大于第 时逆反应速率
时逆反应速率 用
用 表示的反应速率为
表示的反应速率为