10mL0.1mol/L的盐酸与过量的锌粉反应,若要减慢反应速率,又不影响生成H2的量,以下可行的是
| A.加少量CuSO4溶液 | B.加KNO3溶液 | C.加Na2CO3溶液 | D.加CH3COONa固体 |
更新时间:2022-03-22 11:14:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关反应的离子方程式正确的是
A.惰性电极电解氯化铁溶液: |
B.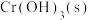 中同时加入 中同时加入 溶液和 溶液和 可制 可制 : : |
C.草酸(乙二酸)溶液和 溶液的中和: 溶液的中和: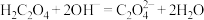 |
D.在酸性 溶液中逐渐通入少量 溶液中逐渐通入少量 气体,观察到有浑浊出现: 气体,观察到有浑浊出现: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列反应中既体现硝酸的氧化性又体现酸性的是
| A.铜与稀硝酸 | B.木炭与浓硝酸 | C.氢氧化铜与硝酸 | D.氧化铁与硝酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.足量的Cu与2mol浓硫酸H2SO4加热充分反应后得到SO2分子数目为NA |
| B.1mol Fe溶于过量稀硝酸,转移的电子数目为3NA |
| C.1mol/L HClO4溶液中含有阳离子总数为0.1NA |
| D.标准状况下,22.4LN2和H2混合气中含有的原子数为4NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知:N2(g)+3H2(g)⇌2NH3 反应1molN2放出92.4kJ的热量.在恒容密闭容器内,投入2molN2和6molH2发生反应,当反应达到平衡状态时,下列说法不正确的是
| A.其他条件不变,升高温度,平衡被破坏,逆反应速率增大,正反应速率减小 |
| B.一定存在2v(H2)正=3v(NH3)正 |
| C.若容器内有 1mol NH3生成,则放出热量46.2kJ |
| D.容器内混合气体压强不再发生变化 |
您最近一年使用:0次
【推荐2】下列有关有效碰撞理论和活化能的认识错误的是
| A.对于气体参与的反应增大压强,活化分子百分数增加,故反应速率增大 |
| B.选用适当的催化剂,降低活化能,活化分子百分数增加,碰撞频率增加 |
| C.温度升高,分子动能增加,活化分子百分数增加,增加了碰撞频率 |
| D.溶液中Ag+和Cl-的反应活化能接近于零,反应几乎在瞬间完成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关实验操作、实验现象和所得结论均正确的是
| 实验操作 | 实验现象 | 结论 | |
| A | 在2mL5%的H2O2溶液中加入1mL饱和FeCl3溶液 | 产生大量气泡 | Fe3+能催化H2O2的分解 |
| B | 向某溶液中先滴入稀HNO3溶液酸化,再滴入Ba(NO3)2溶液 | 出现白色沉淀 | 溶液中有 存在 存在 |
| C | 向Na2CO3溶液中滴入稀盐酸,再将气体通入Na2SiO3溶液中 | Na2SiO3溶液中有白色沉淀生成 | 酸性: 盐酸>H2CO3>H2SiO3 |
| D | 往某溶液中先滴NaOH溶液并加热 | 产生能使润湿的无色酚酞试纸变红的气体 | 证明原溶液中有 存在 存在 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:实验原理为2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O,实验内容及记录如下:
下列说法错误的是
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液紫色褪去所需时间/min | |||
| 0.6 mol·L﹣1H2C2O4溶液 | H2O | 3 mol·L﹣1H2SO4溶液 | 0.05 mol·L﹣1KMnO4溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | a | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | b | 3.9 |
| A.a=3.0,b=3.0 |
| B.根据上表中的实验数据可知,其他条件不变时,H2C2O4浓度越大,反应速率越快 |
| C.忽略混合前后溶液体积的微小变化,实验1这段时间内平均反应速率v(H2C2O4)=0.15mol·L﹣1·min﹣1 |
| D.为验证Mn2+是否有催化作用,可加入硫酸锰固体,实验1~3均可做对照实验 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列措施能减慢化学反应速率的是
| A.将煤块粉碎后燃烧 | B.冬天和面时,和好的面置于温水上发酵 |
| C.食物储藏在冰箱内 | D.酿酒工艺中加入酒曲 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列说法正确的是
| A.元素的存在形态只有两种:化合态和游离态 |
B.碳酸氢钠在水中的电离方程式:NaHCO3=Na++H++ |
| C.2.24L(标准状况)NH3含有的电子数为0.1NA |
| D.H2(g)+I2(g)⇌2HI(g),其他条件不变,缩小反应容器体积,正、逆反应速率不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作能达到实验目的的是
| 实验目的 | 实验操作 |
| A.除去苏打中混有的少量小苏打 | 将固体溶解,加入足量澄清石灰水后过滤、结晶 |
| B.除去乙酸乙酯中的乙酸 | 加入氢氧化钠溶液,充分反应后,静置、分液 |
| C.除去铜粉中混有的氧化铜 | 加入稀硝酸溶解、过滤、洗涤、干燥 |
| D.加快锌与稀硫酸反应制氢气的速率 | 往溶液中滴加几滴硫酸铜溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是
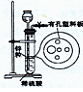
①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水

①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
| A.①③⑤ | B.①②③ | C.④⑤⑥ | D.①②③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验操作和现象对应的结论错误的是
| 选项 | 实验操作和现象 | 结论 |
| A | 分别将乙醇和H2O2溶液滴入酸性KMnO4溶液中,观察到KMnO4溶液均褪色 | 两种物质使酸性KMnO4溶液褪色的原理相同 |
| B | 向两支盛有KI3溶液的试管中分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀生成 | KI3溶液中存在平衡:I ⇌I2+I— ⇌I2+I— |
| C | 向某溶液中加入稀硫酸,生成淡黄色沉淀和有刺激性气味气体 | 该溶液中一定含有S2O |
| D | 实验室用粗锌与稀硫酸反应制H2比纯锌快 | 粗锌与稀硫酸构成原电池 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



