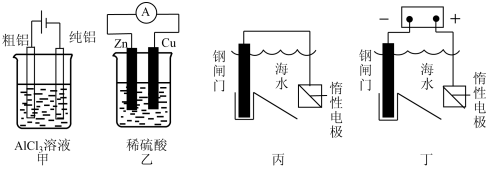
下列有关说法正确的是
| A.电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
B.反应 的 的 可通过下式估算: 可通过下式估算: (反应中形成新共价键的键能之和)-(反应中断裂旧共价键的键能之和) (反应中形成新共价键的键能之和)-(反应中断裂旧共价键的键能之和) |
C.一定温度下向恒容密闭容器中充入 和 和 ,当反应到达平衡时,容器中 ,当反应到达平衡时,容器中 、 、 、 、 的物质的量之比为2:1:2 的物质的量之比为2:1:2 |
D.常温下,向 溶液中加入少量盐酸,溶液中 溶液中加入少量盐酸,溶液中 的值增大 的值增大 |
更新时间:2022-04-04 13:08:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知一定条件下断裂或生成某些化学键的能量关系如下表:
对于反应:H2(g)+ Cl2 (g) =2HCl (g) ,下列说法错误的是
| 断裂或生成的化学键 | 能量数据 |
| 断裂1mol H2分子中的化学键 | 吸收能量436kJ |
| 断裂1mol Cl2分子中的化学键 | 吸收能量243kJ |
| 形成1mol HCl分子中的化学键 | 释放能量431kJ |
| A.该反应的反应热 △H < 0 |
| B.形成1mol HCl化学键时放热431 kJ |
| C.氯化氢分子中的化学键比氯气分子中的化学键更稳定 |
| D.相同条件下,氢气分子具有的总能量高于氯化氢分子具有的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应SiCl4(g)+2H2(g)⇌Si(s)+4HCl(g)可用于纯硅的制备。下列有关该反应的说法正确的是
| A.该反应ΔH>0、ΔS<0 |
B.该反应的平衡常数K= |
| C.υ正(H2)=2υ逆(HCl)时,上述反应达到了限度 |
| D.用E表示键能,该反应ΔH=4E(Si-Cl)+2E(H-H)-4E(H-Cl) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,在2 L密闭容器中,A、B、C三种气体的物质的量随时间变化的曲线如图所示,下列说法正确的是

A.a点时, |
| B.5 min时,反应停止 |
| C.5 min时,A的转化率为25% |
D.反应的化学方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于反应2SO2(g)+O2 (g) 2SO3(g)(放热反应),下列判断正确的是
2SO3(g)(放热反应),下列判断正确的是
 2SO3(g)(放热反应),下列判断正确的是
2SO3(g)(放热反应),下列判断正确的是| A.2体积SO2和足量O2反应,生成2体积SO3 |
| B.其他条件不变,降低温度,正反应速率增大,逆反应速率减小 |
| C.给定条件下该反应进行的限度为SO2消耗速率等于O2生成速率的两倍 |
| D.平衡时,SO2浓度必定等于O2浓度的两倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验过程可以达到实验目的的是
实验目的 | 实验过程 | |
| A | 根据褪色时间来研究浓度对反应速率的影响 | 往2支试管中分别加入同体积、等浓度的草酸溶液,再分别加入同体积、不同浓度的KMnO4溶液 |
| B | 比较HClO和CH3COOH酸性的强弱 | 常温下,用pH计分别测定等物质的量浓度的NaClO溶液和CH3COONa溶液的pH |
| C | 证明HA是弱酸 | 等体积、浓度均为0.1mol/L的HA和HB两种酸分别与足量Zn反应,HA放出的H2多 |
| D | 制备Al2O3固体 | 将NaAlO2溶液蒸干并灼烧 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关实验,对应现象以及结论都正确的是
| 实验 | 现象 | 结论 | |
| A | 向盛有H2O2溶液的试管中加入几滴酸化的FeSO4溶液 | 溶液变成棕黄色,一段时间后溶液中出现气泡,随后有红褐色沉淀生成 | Fe3+催化H2O2分解产生O2,分解反应放热,促进Fe3+的水解 |
| B | 向装有Ag2O晶体的两支试管中分别加入稀硝酸和氨水 | 两支试管中的Ag2O晶体均溶解 | Ag2O是两性氧化物 |
| C | 分别取少量CuSO4、CuCl2、CuBr2、K2SO4、NaCl、KBr固体溶于水 | CuSO4、CuCl2、CuBr2溶液均呈蓝色,K2SO4、NaCl、KBr溶液均呈无色 | Cu2+呈蓝色 |
| D | 将氢氧化镁固体投入到足量浓氯化铵溶液中 | 氢氧化镁固体溶解 | 氯化铵溶液呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据表中提供的数据,判断下列说法中错误的是
| 酸 | 电离平衡常数 |
| HClO | Ka=3.2×10-8 |
 | Ka1=4.4×10-7,Ka2=4.7×10-11 |
A.常温下,等浓度的HClO、 的电离度: 的电离度: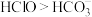 |
B.常温下,等浓度的 和NaClO溶液的pH: 和NaClO溶液的pH: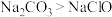 |
C.常温下, 的电离常数和水解常数: 的电离常数和水解常数: |
D.将过量的CO2通入NaClO溶液中发生反应: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】假设图中原电池产生的电压、电流强度均能满足电解、电镀要求,即为理想化。①~⑧为各装置中的电极编号。下列说法错误的是
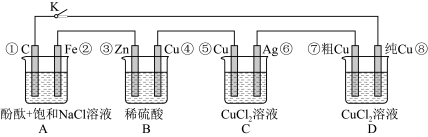

| A.当K闭合时,装置A发生吸氧腐蚀,在电路中作电源 |
| B.当K断开时,装置B锌片溶解,有氢气产生 |
| C.当K闭合后,装置C为电镀池,可以实现在银上镀铜 |
| D.当K闭合后,装置D中粗铜电极减少质量与纯铜电极增加的质量不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用如图所示装置模拟电解原理在工业生产中的应用,下列说法正确的是
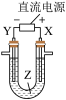

| A.在铁片上镀铜时,每转移2mol电子,Y极增重64g |
B.电解精炼铜时,Z溶液中的 浓度不变 浓度不变 |
C.氯碱工业中,X电极上的反应式是 |
| D.制取金属铝时,Z是熔融的氯化铝 |
您最近一年使用:0次

 ) 是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产,根据能量循环图和表格中的键能,下列说法正确的是
) 是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产,根据能量循环图和表格中的键能,下列说法正确的是

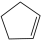 (g)转化为
(g)转化为 (g)的过程中,有C-H的断裂和形成
(g)的过程中,有C-H的断裂和形成