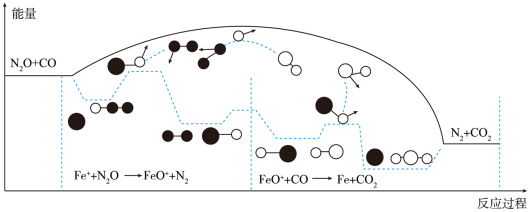
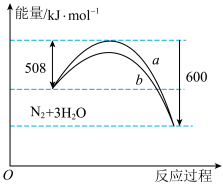
研究表明汽车尾气处理存在反应:N2O(g)+CO(g)=N2(g)+CO2(g),N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示。下列说法不正确的是

| A.升高温度,该反应的平衡常数减小 |
| B.Fe+不影响该反应的焓变 |
| C.FeO+可以有效提高反应物的平衡转化率 |
| D.Fe++N2O→FeO++N2,FeO++CO→Fe++CO2两步反应,前者反应速率慢 |
更新时间:2022-04-05 20:26:41
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
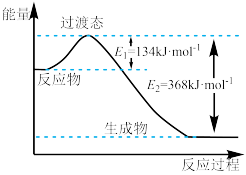
【推荐1】已知方程式2H2(g)+O2(g)=2H2O(l) ΔH1=-571.6 kJ·mol-1,则关于方程式2H2O(l)=2H2(g)+O2(g) ΔH2=?的说法正确的是
| A.方程式中化学计量数表示分子数 | B.该反应的ΔH2=-571.6 kJ·mol-1 |
| C.该反应ΔH2大于零 | D.该反应是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】实验室以苯甲醛为原料合成苯甲酸苯甲酯的反应机理如图(已知RO⁻极易结合H+转化为ROH)。下列说法正确的是
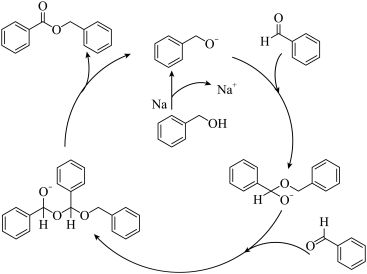
| A.该反应的催化剂为苯甲醇钠,能降低反应的焓变 |
B.合成苯甲酸甲酯总反应方程式为: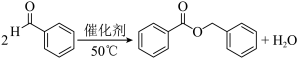 |
| C.与酯化反应相比,该反应的原子利用率高 |
| D.久置的苯甲醛中含有少量苯甲酸,能加快该历程反应速率 |
您最近一年使用:0次
【推荐1】下列操作不能达到实验目的的是
| 实验目的 | 实验操作 | |
| A | 证明非金属性:S>C | 向硫酸溶液中滴入碳酸钠溶液,有气泡产生 |
| B | 证明葡萄糖有还原性 | 向2 mL10%CuSO4溶液中滴加5滴5%NaOH溶液,再加入2 mL10%葡萄糖溶液,加热 |
| C | 探究催化剂对化学反应速率的影响 | 两只大小相同的试管中均加入5%的H2O2溶液2 mL,向其中一支试管滴加 1 mol•L-1 FeCl3溶液1 mL,另一支试管中滴加H2O 1 mL |
| D | 比较乙醇分子中羟基氢原子和水分子中氢原子的活泼性 | 将颗粒大小相同的钠分别与等体积的无水乙醇、水反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.向等体积的20%的H2O2溶液和10%的H2O2溶液中分别滴加等体积的0.1mol•L-1FeCl3溶液和0.1mol•L-1CuCl2溶液,前者产生气泡快,这个实验可以充分证明催化剂具有选择性 |
| B.将0.1mol•L-1醋酸加水稀释,溶液中各离子浓度均减小 |
| C.相同温度下,用分压表示的平衡常数Kp不随体系的总压强变化 |
| D.室温下同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】可逆反应A+B(s) C达到平衡后,加压或降温,A的转化率都增大,则下列结论正确的是
C达到平衡后,加压或降温,A的转化率都增大,则下列结论正确的是
 C达到平衡后,加压或降温,A的转化率都增大,则下列结论正确的是
C达到平衡后,加压或降温,A的转化率都增大,则下列结论正确的是| A.A为非气体,C为气体,正反应为放热反应 |
| B.A为气体,C为非气体,正反应为吸热反应 |
| C.A、C均为气体,正反应为吸热反应 |
| D.A为气体,C为非气体,正反应为放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定条件下存在反应:CO(g) + H2O(g)  CO2(g) + H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1 mol CO和1 molH2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO和2 mol H2O,700°C条件下开始反应。达到平衡时,下列说法正确的是
CO2(g) + H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1 mol CO和1 molH2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO和2 mol H2O,700°C条件下开始反应。达到平衡时,下列说法正确的是
 CO2(g) + H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1 mol CO和1 molH2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO和2 mol H2O,700°C条件下开始反应。达到平衡时,下列说法正确的是
CO2(g) + H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1 mol CO和1 molH2O,在II中充入1 mol CO2和1 mol H2,在III中充入2 mol CO和2 mol H2O,700°C条件下开始反应。达到平衡时,下列说法正确的是| A.容器I、II中正反应速率相同 |
| B.容器I中CO的转化率与容器II中CO2的转化率相等 |
| C.容器II、III中反应的平衡常数相同 |
| D.容器I中CO的物质的量比容器II中的多。 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知反应:A(g)+B(g) C(g)+D(g),在一定压强下,按x=
C(g)+D(g),在一定压强下,按x= (A的物质的量始终为1 mol)向密闭容器中充入A气体与B气体。图甲表示平衡时,A气体的体积分数(V%)与温度(T)、x的关系。图乙表示x=2时,正逆反应的平衡常数与温度的关系。则下列说法正确的是
(A的物质的量始终为1 mol)向密闭容器中充入A气体与B气体。图甲表示平衡时,A气体的体积分数(V%)与温度(T)、x的关系。图乙表示x=2时,正逆反应的平衡常数与温度的关系。则下列说法正确的是

 C(g)+D(g),在一定压强下,按x=
C(g)+D(g),在一定压强下,按x= (A的物质的量始终为1 mol)向密闭容器中充入A气体与B气体。图甲表示平衡时,A气体的体积分数(V%)与温度(T)、x的关系。图乙表示x=2时,正逆反应的平衡常数与温度的关系。则下列说法正确的是
(A的物质的量始终为1 mol)向密闭容器中充入A气体与B气体。图甲表示平衡时,A气体的体积分数(V%)与温度(T)、x的关系。图乙表示x=2时,正逆反应的平衡常数与温度的关系。则下列说法正确的是
| A.图甲中,x2<1 |
| B.图乙中,A线表示正反应的平衡常数 |
| C.由图乙可知,T1时,K=1,B的转化率约为33.3% |
| D.若在恒容绝热装置中进行上述反应,达到平衡时,装置内的气体压强将减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】工业上利用 还原
还原 ,从源头上减少煤粉燃烧产生的大气污染。一定温度下,在
,从源头上减少煤粉燃烧产生的大气污染。一定温度下,在 的恒容密闭容器中,充入1molCO和1molNO,反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g)达到平衡时,测得c(N2)=0.2mol/L,下列说法不正确的是
的恒容密闭容器中,充入1molCO和1molNO,反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g)达到平衡时,测得c(N2)=0.2mol/L,下列说法不正确的是
 还原
还原 ,从源头上减少煤粉燃烧产生的大气污染。一定温度下,在
,从源头上减少煤粉燃烧产生的大气污染。一定温度下,在 的恒容密闭容器中,充入1molCO和1molNO,反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g)达到平衡时,测得c(N2)=0.2mol/L,下列说法不正确的是
的恒容密闭容器中,充入1molCO和1molNO,反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g)达到平衡时,测得c(N2)=0.2mol/L,下列说法不正确的是| A.加入催化剂使正反应速率加快,逆反应活化能减小 |
| B.升高温度,正、逆反应速率增大的倍数不同 |
| C.该温度下,该反应的平衡常数K≈0.25 |
D.若平衡时,往容器中通入2molCO和1molN2,则此时 |
您最近一年使用:0次

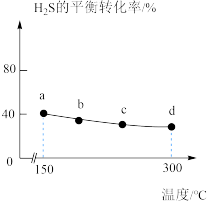
 ,发生反应
,发生反应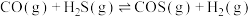 。在不同温度下达到平衡时,
。在不同温度下达到平衡时,