工业合成氨反应:N2(g)+3H2(g)  2NH3(g) △H= -92.4kJ/mol。下列措施有利于提高H2平衡转化率的是
2NH3(g) △H= -92.4kJ/mol。下列措施有利于提高H2平衡转化率的是
 2NH3(g) △H= -92.4kJ/mol。下列措施有利于提高H2平衡转化率的是
2NH3(g) △H= -92.4kJ/mol。下列措施有利于提高H2平衡转化率的是| A.升高温度 | B.增大压强 |
| C.使用铁触媒做催化剂 | D.增大H2的浓度 |
更新时间:2022-04-16 13:54:55
|
相似题推荐
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】NO和CO都是汽车尾气中的有害物质,它们能缓慢地发生反应,反应的化学方程式为2CO+2NO=N2+2CO2,为了控制大气污染,下列建议你认为可行的是
| A.使用催化剂 | B.改变压强 |
| C.适当提高反应温度 | D.将尾气点燃 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】下列事实不能用平衡移动原理解释的是
| A.夏天打开啤酒瓶盖后产生大量气泡 |
| B.压缩H2和I2反应的平衡混合气体,气体颜色变深 |
| C.浓氨水中加入NaOH固体产生有刺激性气味气体 |
| D.实验室用排饱和食盐水的方法收集氯气 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】合成氨所需的H2可由反应CO(g)+H2O(g)=CO2(g)+H2(g) ∆H<0提供,下列措施中,能提高CO转化率的是
| A.增大水蒸气浓度 | B.升高温度 | C.增大CO浓度 | D.增大压强 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】对于可逆反应:
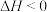 ,下列措施能加快反应速率且使平衡逆向移动的是
,下列措施能加快反应速率且使平衡逆向移动的是

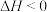 ,下列措施能加快反应速率且使平衡逆向移动的是
,下列措施能加快反应速率且使平衡逆向移动的是| A.增大压强 | B.升高温度 | C.使用催化剂 | D.充入 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】有一处于平衡状态的反应:3A(s)+2B(g) 3C(g),ΔH>0。为了使平衡向生成C的方向移动,应选择的条件是
3C(g),ΔH>0。为了使平衡向生成C的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加催化剂
 3C(g),ΔH>0。为了使平衡向生成C的方向移动,应选择的条件是
3C(g),ΔH>0。为了使平衡向生成C的方向移动,应选择的条件是①高温 ②低温 ③高压 ④低压 ⑤加催化剂
| A.①③ | B.①③⑤ | C.①④ | D.②④⑤ |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】化学与生活息息相关。下列说法正确的是
| A.使用加酶洗衣粉洗涤衣物时,水温越高效果越好 |
B. 作腌制品的保鲜剂,能减缓食物腐败变质的速率 作腌制品的保鲜剂,能减缓食物腐败变质的速率 |
| C.使用催化剂消除汽车尾气污染物时,催化剂颗粒大小对其反应速率无影响 |
| D.打开啤酒瓶盖后冒出大量气泡,压强减小,二氧化碳的溶解度增大 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】下列事实不能 用勒夏特列原理来解释的是
| A.实验室中常用排饱和食盐水的方法收集Cl2 |
| B.鼓入过量空气有利于SO2转化为SO3 |
| C.开启啤酒瓶后,瓶中立刻泛起大量泡沫 |
| D.煅烧硫铁矿时先将矿石粉碎 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】下列事实不能 用勒夏特列原理解释的是
| A.光照新制的氯水时,溶液的pH逐渐减小 |
| B.高温,使N2和H2转化为更多的NH3(△H<0) |
| C.可用浓氨水和氢氧化钠固体快速制取氨气 |
| D.增大压强,有利于SO2和O2反应生成SO3 |
您最近一年使用:0次

 ,发生反应:
,发生反应: ,达到平衡后,保持温度不变,再通入适量
,达到平衡后,保持温度不变,再通入适量 (
(


