碳排放问题是第26届联合国气候变化大会讨论的焦点。我国向国际社会承诺2030年“碳达峰”,2060年实现“碳中和”。为了实现这个目标,加强了对CO2转化的研究。下面是CO2转化为高附加值化学品的反应。相关反应的热化学方程式如下:
反应Ⅰ:CO2(g)+H2(g) H2O(g)+CO(g) △H1
H2O(g)+CO(g) △H1
反应Ⅱ:CO(g)+2H2(g) CH3OH(g) △H2=-90.0kJ·mol-1
CH3OH(g) △H2=-90.0kJ·mol-1
反应Ⅲ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3=-49.0kJ·mol-1
CH3OH(g)+H2O(g) △H3=-49.0kJ·mol-1
反应Ⅳ:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H4=-165.0kJ·mol-1
CH4(g)+2H2O(g) △H4=-165.0kJ·mol-1
反应Ⅴ:2CO2g)+6H2(g) C2H4(g)+4H2O(g) △H5=-122.7kJ·mol-1
C2H4(g)+4H2O(g) △H5=-122.7kJ·mol-1
回答下列问题:
(1)反应Ⅲ一般认为通过反应Ⅰ、Ⅱ来实现,则反应Ⅰ的△H1=____ kJ·mol-1;已知:由实验测得反应Ⅰ的v正=k正c(CO2)·c(H2),v逆=k逆·c(H2O)·c(CO)(k正、k逆为速率常数,与温度、催化剂有关)。若平衡后升高温度,则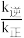 =
=____ (填“增大”、“不变”或“减小”)。
(2)在2L恒容密闭容器中充入总物质的量为8mol的CO2和H2发生反应Ⅲ,改变氢碳比 ,在不同温度下反应达到平衡状态,测得的实验数据如表:
,在不同温度下反应达到平衡状态,测得的实验数据如表:
①下列说法中正确的是____ (填英文字母)。
A.增大氢碳比,平衡正向移动,平衡常数增大
B.v(CH3OH)=v(CO2)时,反应达到平衡
C.当混合气体平均摩尔质量不变时,达到平衡
D.当混合气体密度不变时,达到平衡
②在700K、氢碳比为3.0的条件下,某时刻测得容器内CO2、H2、CH3OH、H2O的物质的量分别为2mol、2mol、1mol和1mol,则此时正反应速率和逆反应速率的关系是_____ (填英文字母)。
A.v(正)>v(逆) B.v(正)<v(逆) C.(正)=r(逆) D.无法判断
(3)CO2在一定条件下催化加氢生成CH3OH,主要发生三个竞争反应(即反应Ⅲ、Ⅳ、Ⅴ),为分析催化剂对反应的选择性,在1L恒容密闭容器中充入2.0molCO2和5.3molH2,测得反应进行相同时间后,有关物质的物质的量随温度变化如图所示:
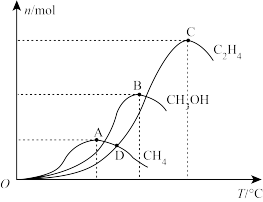
①该催化剂在较低温度时主要选择反应____ (“Ⅲ”或“Ⅳ”或“Ⅴ”)。研究发现,若温度过高,三种含碳产物的物质的量会迅速降低,其主要原因可能是:____ 。
②在一定温度下达到平衡,此时测得容器中部分物质的含量为:n(CH4)=0.1mol,n(C2H4)=0.4mol,n(CH3OH)=0.5mol。则该温度下反应Ⅲ的平衡常数K(Ⅲ)=____ L2/mol2(保留两位小数)。
(4)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。欲用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为____ mol/L(已知:常温下Ksp(BaSO4)=1×10-11,Ksp(BaCO3)=1×10-10。忽略溶液体积的变化,保留两位有效数字)。
(5)研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示。温度小于900℃时进行电解反应,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,阳极的电极反应式为2CO -4e-=2CO2↑+O2↑,则阴极的电极反应式为
-4e-=2CO2↑+O2↑,则阴极的电极反应式为____ 。

反应Ⅰ:CO2(g)+H2(g)
 H2O(g)+CO(g) △H1
H2O(g)+CO(g) △H1反应Ⅱ:CO(g)+2H2(g)
 CH3OH(g) △H2=-90.0kJ·mol-1
CH3OH(g) △H2=-90.0kJ·mol-1反应Ⅲ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3=-49.0kJ·mol-1
CH3OH(g)+H2O(g) △H3=-49.0kJ·mol-1反应Ⅳ:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H4=-165.0kJ·mol-1
CH4(g)+2H2O(g) △H4=-165.0kJ·mol-1反应Ⅴ:2CO2g)+6H2(g)
 C2H4(g)+4H2O(g) △H5=-122.7kJ·mol-1
C2H4(g)+4H2O(g) △H5=-122.7kJ·mol-1回答下列问题:
(1)反应Ⅲ一般认为通过反应Ⅰ、Ⅱ来实现,则反应Ⅰ的△H1=
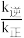 =
=(2)在2L恒容密闭容器中充入总物质的量为8mol的CO2和H2发生反应Ⅲ,改变氢碳比
 ,在不同温度下反应达到平衡状态,测得的实验数据如表:
,在不同温度下反应达到平衡状态,测得的实验数据如表:| 温度/K CO2转化率  | 500 | 600 | 700 | 800 |
| 1 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 40 | 22 |
A.增大氢碳比,平衡正向移动,平衡常数增大
B.v(CH3OH)=v(CO2)时,反应达到平衡
C.当混合气体平均摩尔质量不变时,达到平衡
D.当混合气体密度不变时,达到平衡
②在700K、氢碳比为3.0的条件下,某时刻测得容器内CO2、H2、CH3OH、H2O的物质的量分别为2mol、2mol、1mol和1mol,则此时正反应速率和逆反应速率的关系是
A.v(正)>v(逆) B.v(正)<v(逆) C.(正)=r(逆) D.无法判断
(3)CO2在一定条件下催化加氢生成CH3OH,主要发生三个竞争反应(即反应Ⅲ、Ⅳ、Ⅴ),为分析催化剂对反应的选择性,在1L恒容密闭容器中充入2.0molCO2和5.3molH2,测得反应进行相同时间后,有关物质的物质的量随温度变化如图所示:

①该催化剂在较低温度时主要选择反应
②在一定温度下达到平衡,此时测得容器中部分物质的含量为:n(CH4)=0.1mol,n(C2H4)=0.4mol,n(CH3OH)=0.5mol。则该温度下反应Ⅲ的平衡常数K(Ⅲ)=
(4)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。欲用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为
(5)研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图所示。温度小于900℃时进行电解反应,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,阳极的电极反应式为2CO
 -4e-=2CO2↑+O2↑,则阴极的电极反应式为
-4e-=2CO2↑+O2↑,则阴极的电极反应式为
更新时间:2022-04-16 21:59:48
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】
(1)已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1.那么用太阳能分解10mol水消耗的能量是___________ kJ;
(2)由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:
(i)CO(g) + 2H2(g) = CH3OH(g) ΔH1 = -90.1kJ•mol-1
(ii)CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) ΔH2 = -49.0kJ•mol-1
水煤气变换反应:
(iii)CO(g) + H2O(g) = CO2(g) + H2 (g) ΔH3 = -41.1kJ•mol-1
二甲醚合成反应:
(iV)2 CH3OH(g) = CH3OCH3(g) + H2O(g) ΔH4 = -24.5kJ•mol-1
则由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为___________ 。
(3)在容积为1.00L的容器中,通入一定量N2O4,发生N2O4(g)⇌2NO2(g), 100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,v(N2O4)=___________ ,

(4)已知反应2HI(g)=H2(g) + I2(g)的ΔH= +11kJ·mol-1,1molH2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___________ kJ。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表
上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数, 若k正 = 0.0027min-1,在t=40min时,v正=___________ min-1。
(1)已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1.那么用太阳能分解10mol水消耗的能量是
(2)由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:
(i)CO(g) + 2H2(g) = CH3OH(g) ΔH1 = -90.1kJ•mol-1
(ii)CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) ΔH2 = -49.0kJ•mol-1
水煤气变换反应:
(iii)CO(g) + H2O(g) = CO2(g) + H2 (g) ΔH3 = -41.1kJ•mol-1
二甲醚合成反应:
(iV)2 CH3OH(g) = CH3OCH3(g) + H2O(g) ΔH4 = -24.5kJ•mol-1
则由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为
(3)在容积为1.00L的容器中,通入一定量N2O4,发生N2O4(g)⇌2NO2(g), 100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,v(N2O4)=

(4)已知反应2HI(g)=H2(g) + I2(g)的ΔH= +11kJ·mol-1,1molH2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数, 若k正 = 0.0027min-1,在t=40min时,v正=
您最近一年使用:0次
【推荐2】环氧乙烷常用于一次性口罩生产过程中灭菌和新冠病毒的消杀,工业上常利用乙烯直接氧化法生产环氧乙烷(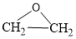 ),发生的反应如下。
),发生的反应如下。
主反应Ⅰ:2CH2=CH2(g)+O2(g) 2
2 (g) ΔH1=-210kJ·mol-1
(g) ΔH1=-210kJ·mol-1
副反应Ⅱ:CH2=CH2(g)+3O2(g) 2CO2(g)+2H2O(l) ΔH2=-1324kJ·mol-1
2CO2(g)+2H2O(l) ΔH2=-1324kJ·mol-1
副反应Ⅲ:2 (g)+5O2(g)
(g)+5O2(g) 4CO2(g)+4H2O(g) ΔH3
4CO2(g)+4H2O(g) ΔH3
已知:环氧乙烷选择性是指乙烯进行反应Ⅰ生成环氧乙烷的优势。
(1)ΔH3=__ kJ·mol-1。
(2)①图1是乙烯转化率、环氧乙烷选择性与流速关系的图象,图中随进料气的流速加快,乙烯的转化率下降,其可能原因是__ 。
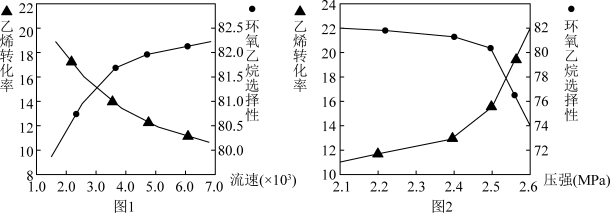
②图2是乙烯转化率、环氧乙烷选择性与压强关系的图象,图中当反应体系的压强高于2.4MPa,环氧乙烷选择性下降,其可能原因是__ 。
(3)实验测得反应Ⅰ中,υ正=K正·x2(CH2=CH2)·x(O2),υ逆=K逆·x2( ),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。
),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。
①若在1L的密闭容器中充2molCH2=CH2(g)和1molO2(g),在一定温度下只发生反应I,达到平衡时CH2=CH2的转化率为75%,则该反应平衡常数的值为__ 。
②若平衡后仅升高温度,则下列说法正确的是___ 。
A.x(CH2=CH2)增大,x( )减小
)减小
B.K正与K逆的比值增大
C.υ正减小,υ逆增大
D.K正与K逆的比值减小
(4)将乙烯与饱和食盐水的电解产物反应,转化为氯乙醇[CH2(OH)CH2Cl],氯乙醇进一步反应生成环氧乙烷,其电解简易装置如图所示。
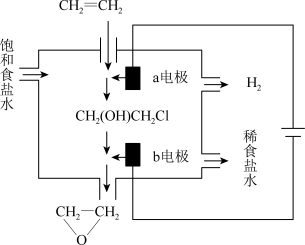
已知:CH2=CH2+H2O+Cl2→CH2(OH)CH2Cl+HCl
①a电极为__ (选填“阴极”或“阳极”),其电极反应式为:__ 。
②b电极区域生成环氧乙烷的化学方程式为__ 。
 ),发生的反应如下。
),发生的反应如下。主反应Ⅰ:2CH2=CH2(g)+O2(g)
 2
2 (g) ΔH1=-210kJ·mol-1
(g) ΔH1=-210kJ·mol-1副反应Ⅱ:CH2=CH2(g)+3O2(g)
 2CO2(g)+2H2O(l) ΔH2=-1324kJ·mol-1
2CO2(g)+2H2O(l) ΔH2=-1324kJ·mol-1副反应Ⅲ:2
 (g)+5O2(g)
(g)+5O2(g) 4CO2(g)+4H2O(g) ΔH3
4CO2(g)+4H2O(g) ΔH3已知:环氧乙烷选择性是指乙烯进行反应Ⅰ生成环氧乙烷的优势。
(1)ΔH3=
(2)①图1是乙烯转化率、环氧乙烷选择性与流速关系的图象,图中随进料气的流速加快,乙烯的转化率下降,其可能原因是

②图2是乙烯转化率、环氧乙烷选择性与压强关系的图象,图中当反应体系的压强高于2.4MPa,环氧乙烷选择性下降,其可能原因是
(3)实验测得反应Ⅰ中,υ正=K正·x2(CH2=CH2)·x(O2),υ逆=K逆·x2(
 ),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。
),(式中x为物质的量分数;K正、K逆为速率常数,只与温度有关)。①若在1L的密闭容器中充2molCH2=CH2(g)和1molO2(g),在一定温度下只发生反应I,达到平衡时CH2=CH2的转化率为75%,则该反应平衡常数的值为
②若平衡后仅升高温度,则下列说法正确的是
A.x(CH2=CH2)增大,x(
 )减小
)减小B.K正与K逆的比值增大
C.υ正减小,υ逆增大
D.K正与K逆的比值减小
(4)将乙烯与饱和食盐水的电解产物反应,转化为氯乙醇[CH2(OH)CH2Cl],氯乙醇进一步反应生成环氧乙烷,其电解简易装置如图所示。

已知:CH2=CH2+H2O+Cl2→CH2(OH)CH2Cl+HCl
①a电极为
②b电极区域生成环氧乙烷的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】CO2的资源化可以推动经济高质量发展和生态环境质量的持续改善。由CO2合成甲醇是CO2资源化利用的重要方法。
Ⅰ.合成甲醇
(1)由CO2催化加氢合成甲醇醇。
①一定条件下,由CO2和H2制备甲醇的过程中有下列反应:
反应1:CO2(g)+H2(g) CO(g)+H2O(g) △H1
CO(g)+H2O(g) △H1
反应2:CO(g)+2H2(g) CH3OH(g) △H2
CH3OH(g) △H2
反应3:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图所示。____ △H3(填“>”“<”或“=”)。
②对于上述CO2加氢合成CH3OH的反应体系,下列说法不正确 的是____ (填字母)。
a.增大初始投料比 ,有利于提高CO2的转化率
,有利于提高CO2的转化率
b.当气体的平均摩尔质量保持不变时,说明反应体系已达平衡
c.体系达平衡后,若压缩容器体积,则反应1平衡不移动,反应3平衡正向移动
d.选用合适的催化剂可以提高反应3中CO2的平衡转化率
(2)电化学原理将CO2转化为甲醇。
在光电催化条件下可以高效地将CO2和H2O转化为甲醇,从电极反应的角度分析:
①甲醇在____ (填“阴”或“阳”)极生成;
②氧化反应为____ 。
Ⅱ.甲醇是重要的化工原料,也可用作甲醇燃料电池。以稀硫酸为电解质溶液,甲醇燃料电池的工作原理如图所示。_____ 。
(4)该电池负极的电极反应式是_____ 。
Ⅰ.合成甲醇
(1)由CO2催化加氢合成甲醇醇。
①一定条件下,由CO2和H2制备甲醇的过程中有下列反应:
反应1:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1
CO(g)+H2O(g) △H1反应2:CO(g)+2H2(g)
 CH3OH(g) △H2
CH3OH(g) △H2反应3:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图所示。
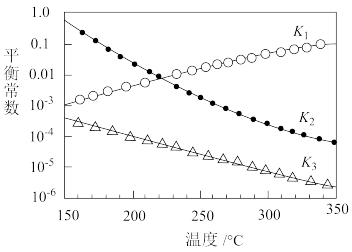
②对于上述CO2加氢合成CH3OH的反应体系,下列说法
a.增大初始投料比
 ,有利于提高CO2的转化率
,有利于提高CO2的转化率b.当气体的平均摩尔质量保持不变时,说明反应体系已达平衡
c.体系达平衡后,若压缩容器体积,则反应1平衡不移动,反应3平衡正向移动
d.选用合适的催化剂可以提高反应3中CO2的平衡转化率
(2)电化学原理将CO2转化为甲醇。
在光电催化条件下可以高效地将CO2和H2O转化为甲醇,从电极反应的角度分析:
①甲醇在
②氧化反应为
Ⅱ.甲醇是重要的化工原料,也可用作甲醇燃料电池。以稀硫酸为电解质溶液,甲醇燃料电池的工作原理如图所示。
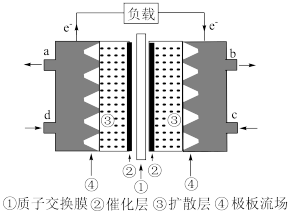
(4)该电池负极的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】煤和天然气都是重要的化石资源,在工业生产中用途广泛。
(1)燃煤时往往在煤中添加石灰石,目的是___________ ,达到该目的时发生反应的化学方程式为___________ 。
(2)煤的综合利用包括___________ (将煤隔绝空气加强热)、煤的气化和液化。煤的气化是将其转化为可燃性气体的过程,主要发生的反应的化学方程式为___________ 。
(3)CO是煤气的主要成分,可与水蒸气反应生成氢气:CO(g)+ H2O(g) CO2(g)+H2(g)△H。 查阅资料得出相关数据如下:
CO2(g)+H2(g)△H。 查阅资料得出相关数据如下:
①该反应升高到一定温度时,反应将不能正向进行,由此判断该反应的△S___________ (填“>”或“<”)0。
②在容积为10 L的密闭容器中通入0.1 mol CO(g)和0.1 mol H2O(g)发生反应,在400℃时反应达到平衡,此时CO(g)的转化率为___________ 。
(1)燃煤时往往在煤中添加石灰石,目的是
(2)煤的综合利用包括
(3)CO是煤气的主要成分,可与水蒸气反应生成氢气:CO(g)+ H2O(g)
 CO2(g)+H2(g)△H。 查阅资料得出相关数据如下:
CO2(g)+H2(g)△H。 查阅资料得出相关数据如下:| 温度/°C | 400 | 500 |
| 平衡常数K | 9 | 5.3 |
①该反应升高到一定温度时,反应将不能正向进行,由此判断该反应的△S
②在容积为10 L的密闭容器中通入0.1 mol CO(g)和0.1 mol H2O(g)发生反应,在400℃时反应达到平衡,此时CO(g)的转化率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】氯乙烯是用途广泛的石油化工产品,工业上常利用乙烯氧氯化法生产:

已知:ⅰ.
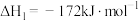
ⅱ.
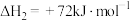
ⅲ.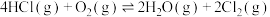
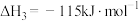
回答下列问题:
(1)
___________  。
。
(2)已知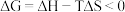 ,反应可自发进行。若
,反应可自发进行。若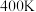 时反应ⅱ中
时反应ⅱ中 ,此时反应ⅱ
,此时反应ⅱ___________ (“能”或“不能”)自发进行。
(3)为提高反应ⅱ中氯乙烯的平衡产率,可采取的措施有___________ 。
a.加入合适的催化剂 b.升高温度 c.增大压强 d.及时氧化
(4)向 密闭容器中初始投入
密闭容器中初始投入 、
、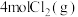 和
和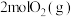 发生乙烯氧氯化反应,不同温度下测得反应在平衡时
发生乙烯氧氯化反应,不同温度下测得反应在平衡时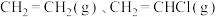 、
、 三种组分的体积分数随温度的变化如图1所示。
三种组分的体积分数随温度的变化如图1所示。___________ 和___________ 的体积分数随温度的变化。
②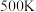 时反应进行到
时反应进行到 达到平衡,
达到平衡, 内用
内用 的浓度变化表示的
的浓度变化表示的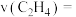
___________ ,该反应的平衡常数
___________ 。
(5) 时,控制进料浓度
时,控制进料浓度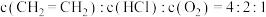 。容器中发生反应
。容器中发生反应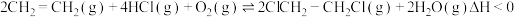 ,不同温度对
,不同温度对 的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过
的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过 转化为
转化为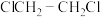 的转化率大小来体现)
的转化率大小来体现)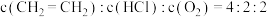 ,所得
,所得 的平衡转化率曲线应在点M的
的平衡转化率曲线应在点M的___________ (填“上”或“下”)方。
②因受现有工业设备限制,需保持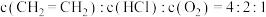 不变,在235℃、
不变,在235℃、 下,若要进一步增大
下,若要进一步增大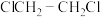 的选择性,可选择从
的选择性,可选择从___________ 方向进一步展开研究。

已知:ⅰ.

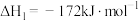
ⅱ.

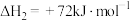
ⅲ.
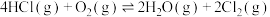
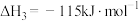
回答下列问题:
(1)

 。
。(2)已知
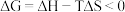 ,反应可自发进行。若
,反应可自发进行。若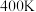 时反应ⅱ中
时反应ⅱ中 ,此时反应ⅱ
,此时反应ⅱ(3)为提高反应ⅱ中氯乙烯的平衡产率,可采取的措施有
a.加入合适的催化剂 b.升高温度 c.增大压强 d.及时氧化

(4)向
 密闭容器中初始投入
密闭容器中初始投入 、
、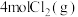 和
和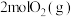 发生乙烯氧氯化反应,不同温度下测得反应在平衡时
发生乙烯氧氯化反应,不同温度下测得反应在平衡时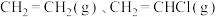 、
、 三种组分的体积分数随温度的变化如图1所示。
三种组分的体积分数随温度的变化如图1所示。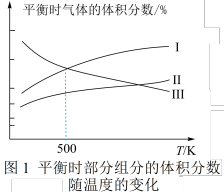
②
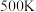 时反应进行到
时反应进行到 达到平衡,
达到平衡, 内用
内用 的浓度变化表示的
的浓度变化表示的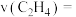

(5)
 时,控制进料浓度
时,控制进料浓度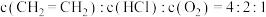 。容器中发生反应
。容器中发生反应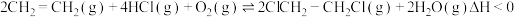 ,不同温度对
,不同温度对 的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过
的平衡转化率和催化剂的催化效率的影响如图2所示。(备注:催化效率是指催化剂转化反应物为生成物的能力,通常通过产物的选择性和反应速率来衡量。图2中通过 转化为
转化为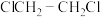 的转化率大小来体现)
的转化率大小来体现)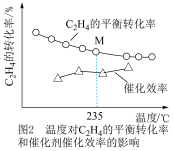
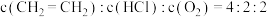 ,所得
,所得 的平衡转化率曲线应在点M的
的平衡转化率曲线应在点M的②因受现有工业设备限制,需保持
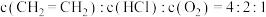 不变,在235℃、
不变,在235℃、 下,若要进一步增大
下,若要进一步增大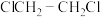 的选择性,可选择从
的选择性,可选择从
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】氮族元素及其化合物在工农业生产、环境等方面有重要应用和影响。
(1)燃料在汽车发动机中燃烧时会产生污染环境的 、
、 ,加装三元催化转化器可使汽车尾气中的
,加装三元催化转化器可使汽车尾气中的 、
、 转化为无毒物质。
转化为无毒物质。
已知:I.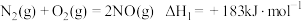
II.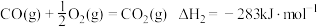
①则反应III: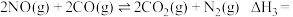
_______  ,该反应能自发进行的条件是在
,该反应能自发进行的条件是在_______ (填“低温”、“高温”或“任意温度”)下。
②向某绝热恒容密闭容器内充入一定量的 和
和 ,发生反应III。下列能说明该反应达到平衡状态的是
,发生反应III。下列能说明该反应达到平衡状态的是_______ (填标号)。
A.容器内气体的密度不再改变 B.容器内气体的温度不再改变
C.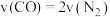 D.容器内气体的平均摩尔质量不再改变
D.容器内气体的平均摩尔质量不再改变
③向容积均为 的三个恒容密闭容器中分别通入
的三个恒容密闭容器中分别通入 和
和 ,发生上述反应Ⅲ,a、b、c三组实验的反应温度分别记为
,发生上述反应Ⅲ,a、b、c三组实验的反应温度分别记为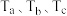 。恒温恒容条件下反应各体系压强的变化如图所示。则达到平衡时
。恒温恒容条件下反应各体系压强的变化如图所示。则达到平衡时 由大到小的顺序是
由大到小的顺序是_______ ;实验b中,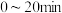 内,
内, 分压的平均变化率为
分压的平均变化率为_______  ,该反应的压强平衡常数
,该反应的压强平衡常数
_______  (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。

(2)氮能与氢、氟形成结构相似的化合物 和
和 ,请判断键角:
,请判断键角:
_______ (填“>”、“<”或“=”) ,原因为
,原因为_______ 。
(3) 是一种重要的半导体材料,其晶胞结构如图所示,设
是一种重要的半导体材料,其晶胞结构如图所示,设 为阿伏加德罗常数的值,1号原子的坐标为
为阿伏加德罗常数的值,1号原子的坐标为 、3号原子的坐标为
、3号原子的坐标为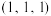 ,
, 晶体的密度为
晶体的密度为 。
。

①2号原子的坐标为_______ 。
② 原子和
原子和 原子之间的最短距离为
原子之间的最短距离为_______ (不用化到最简) 。
。
(1)燃料在汽车发动机中燃烧时会产生污染环境的
 、
、 ,加装三元催化转化器可使汽车尾气中的
,加装三元催化转化器可使汽车尾气中的 、
、 转化为无毒物质。
转化为无毒物质。已知:I.
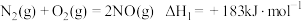
II.
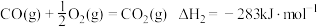
①则反应III:
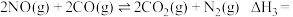
 ,该反应能自发进行的条件是在
,该反应能自发进行的条件是在②向某绝热恒容密闭容器内充入一定量的
 和
和 ,发生反应III。下列能说明该反应达到平衡状态的是
,发生反应III。下列能说明该反应达到平衡状态的是A.容器内气体的密度不再改变 B.容器内气体的温度不再改变
C.
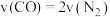 D.容器内气体的平均摩尔质量不再改变
D.容器内气体的平均摩尔质量不再改变③向容积均为
 的三个恒容密闭容器中分别通入
的三个恒容密闭容器中分别通入 和
和 ,发生上述反应Ⅲ,a、b、c三组实验的反应温度分别记为
,发生上述反应Ⅲ,a、b、c三组实验的反应温度分别记为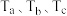 。恒温恒容条件下反应各体系压强的变化如图所示。则达到平衡时
。恒温恒容条件下反应各体系压强的变化如图所示。则达到平衡时 由大到小的顺序是
由大到小的顺序是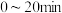 内,
内, 分压的平均变化率为
分压的平均变化率为 ,该反应的压强平衡常数
,该反应的压强平衡常数
 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
(2)氮能与氢、氟形成结构相似的化合物
 和
和 ,请判断键角:
,请判断键角:
 ,原因为
,原因为(3)
 是一种重要的半导体材料,其晶胞结构如图所示,设
是一种重要的半导体材料,其晶胞结构如图所示,设 为阿伏加德罗常数的值,1号原子的坐标为
为阿伏加德罗常数的值,1号原子的坐标为 、3号原子的坐标为
、3号原子的坐标为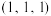 ,
, 晶体的密度为
晶体的密度为 。
。
①2号原子的坐标为
②
 原子和
原子和 原子之间的最短距离为
原子之间的最短距离为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
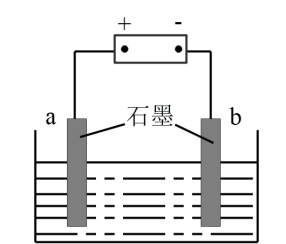
【推荐1】锅炉水垢既会降低燃料的利用率、影响锅炉的使用寿命,还可能造成安全隐患。某锅炉水垢的主要成分有CaCO3、CaSO4、Mg(OH)2、Fe2O3,用酸洗法可除去该水垢,其基本原理如下图所示。

(1)“酸洗”时,一般不选用稀硫酸的原因是_______________________________ 。
(2)“不溶物”用碳酸钠溶液浸泡的目的是________________________________ (用离子方程式表示)。
(3)为防止洗出液中的Fe3+腐蚀铁质管道,常在洗出液中加入SnCl2溶液,反应中Sn2+转化为Sn4+,则Sn2+与Fe3+反应的物质的量之比为________ 。
(4)柠檬酸(用H3R表示)可用作酸洗剂,溶液中H3R、H2R-、HR2-、R3-的含量与pH的关系如图所示。图中a曲线所代表的微粒的百分含量随溶液pH的改变而变化的原因是_____________________ (用平衡移动原理解释)。HR2-电离常数为Ka3,请根据图示信息计算出pKa3=________ (pKa3=-lgKa3)。

(5)利用如图2所示装置对锅炉水(含Ca2+、Mg2+、 )进行预处理,可有效防止锅炉水垢的形成。写出电解过程中,Ca2+形成沉淀的电极反应方程式:
)进行预处理,可有效防止锅炉水垢的形成。写出电解过程中,Ca2+形成沉淀的电极反应方程式:__________________ 。

(1)“酸洗”时,一般不选用稀硫酸的原因是
(2)“不溶物”用碳酸钠溶液浸泡的目的是
(3)为防止洗出液中的Fe3+腐蚀铁质管道,常在洗出液中加入SnCl2溶液,反应中Sn2+转化为Sn4+,则Sn2+与Fe3+反应的物质的量之比为
(4)柠檬酸(用H3R表示)可用作酸洗剂,溶液中H3R、H2R-、HR2-、R3-的含量与pH的关系如图所示。图中a曲线所代表的微粒的百分含量随溶液pH的改变而变化的原因是

(5)利用如图2所示装置对锅炉水(含Ca2+、Mg2+、
 )进行预处理,可有效防止锅炉水垢的形成。写出电解过程中,Ca2+形成沉淀的电极反应方程式:
)进行预处理,可有效防止锅炉水垢的形成。写出电解过程中,Ca2+形成沉淀的电极反应方程式:
您最近一年使用:0次
【推荐2】研究催化去除汽车尾气、工业烟气中的氮及硫的化化物是环境保护、促进社会可持续发展的重要课题。
(1)汽车尾气主要含CO2、N2、CO、SO2、NOx等。
①用Na2CO3溶液能吸收SO2的原因是_______ 。
②汽车尾气中形成硝酸型酸雨的物质是_______ 。
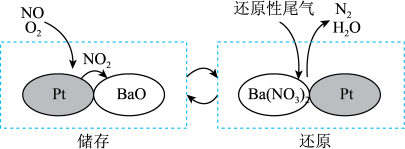
(2)NOx储存还原技术可有效降低柴油发动机在空气过量条件下NOx的排放。如下图所示NOx的储存和还原在不同时段交替进行,通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。
①储存NOx的物质是_______ (填写化学式)。
②与Ba(NO3)2反应生成1molN2需要还原性尾气H2_______ mol。
(3)生物法脱H2S的原理为:
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(S04)3+2H2O
2Fe2(S04)3+2H2O
①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是_______ 。
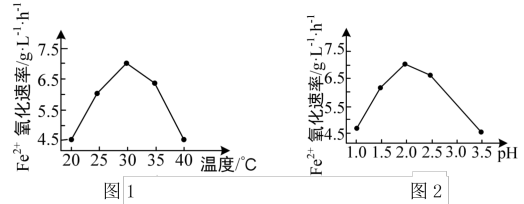
②由图1和图2判断使用硫杆菌的最佳条件为_______ 。
(4)太阳能光电催化—化学耦合分解H2S的装置如图所示。
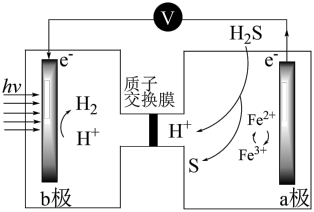
该太阳能光电催化—化学耦合分解H2S的过程可描述为_______ 。
(1)汽车尾气主要含CO2、N2、CO、SO2、NOx等。
①用Na2CO3溶液能吸收SO2的原因是
②汽车尾气中形成硝酸型酸雨的物质是
(2)NOx储存还原技术可有效降低柴油发动机在空气过量条件下NOx的排放。如下图所示NOx的储存和还原在不同时段交替进行,通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。

①储存NOx的物质是
②与Ba(NO3)2反应生成1molN2需要还原性尾气H2
(3)生物法脱H2S的原理为:
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4
 2Fe2(S04)3+2H2O
2Fe2(S04)3+2H2O①硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是
②由图1和图2判断使用硫杆菌的最佳条件为

(4)太阳能光电催化—化学耦合分解H2S的装置如图所示。

该太阳能光电催化—化学耦合分解H2S的过程可描述为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】 是用途广泛的重要工业品,用途广泛,将
是用途广泛的重要工业品,用途广泛,将 通入
通入 溶液中可制备
溶液中可制备 ,反应化学方程式为
,反应化学方程式为 。某同学设计如图实验装置(夹持仪器已省略)制备
。某同学设计如图实验装置(夹持仪器已省略)制备 。回答下列问题:
。回答下列问题:

(1)装置A中反应的离子方程式为___________ 。
(2)装置B中盛放的试剂是___________ ,装置C中仪器X的名称为___________ 。
(3)已知 在100℃时溶解度约为156g,
在100℃时溶解度约为156g, 在100℃时的溶解度约为48g。简述从仪器X中获得
在100℃时的溶解度约为48g。简述从仪器X中获得 粗品的步骤:
粗品的步骤:______________________ 。
(4) 粗品中
粗品中 纯度的测定称取a g粗品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,加入少量的稀硫酸,用0.100
纯度的测定称取a g粗品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,加入少量的稀硫酸,用0.100 的
的 溶液滴定至终点时,消耗b mL
溶液滴定至终点时,消耗b mL  溶液(
溶液(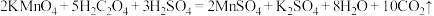 )。粗品中
)。粗品中 的质量分数为
的质量分数为___________ (用含有a、b的代数式表示)。
(5)电解 溶液也可以制备
溶液也可以制备 ,阳极电极反应式为
,阳极电极反应式为________ 。
(6)实验室若配制 溶液。下列操作会使配制的
溶液。下列操作会使配制的 溶液浓度偏大的是
溶液浓度偏大的是________ (填字母,假设其他操作均正确)。
A.没有冷却至室温就转移液体到容量瓶并完成定容
B.将溶液移入容量瓶过程中有少量溶液溅出
C.使用容量瓶配制溶液,定容时,仰视刻度线
D.容量瓶刚用蒸馏水洗净,没有烘干就用来配制溶液
E.定容时,滴加蒸馏水,不慎加多高于刻度线,吸出少量水使凹液面最低点与刻度线相切
 是用途广泛的重要工业品,用途广泛,将
是用途广泛的重要工业品,用途广泛,将 通入
通入 溶液中可制备
溶液中可制备 ,反应化学方程式为
,反应化学方程式为 。某同学设计如图实验装置(夹持仪器已省略)制备
。某同学设计如图实验装置(夹持仪器已省略)制备 。回答下列问题:
。回答下列问题:
(1)装置A中反应的离子方程式为
(2)装置B中盛放的试剂是
(3)已知
 在100℃时溶解度约为156g,
在100℃时溶解度约为156g, 在100℃时的溶解度约为48g。简述从仪器X中获得
在100℃时的溶解度约为48g。简述从仪器X中获得 粗品的步骤:
粗品的步骤:(4)
 粗品中
粗品中 纯度的测定称取a g粗品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,加入少量的稀硫酸,用0.100
纯度的测定称取a g粗品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,加入少量的稀硫酸,用0.100 的
的 溶液滴定至终点时,消耗b mL
溶液滴定至终点时,消耗b mL  溶液(
溶液(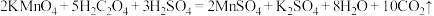 )。粗品中
)。粗品中 的质量分数为
的质量分数为(5)电解
 溶液也可以制备
溶液也可以制备 ,阳极电极反应式为
,阳极电极反应式为(6)实验室若配制
 溶液。下列操作会使配制的
溶液。下列操作会使配制的 溶液浓度偏大的是
溶液浓度偏大的是A.没有冷却至室温就转移液体到容量瓶并完成定容
B.将溶液移入容量瓶过程中有少量溶液溅出
C.使用容量瓶配制溶液,定容时,仰视刻度线
D.容量瓶刚用蒸馏水洗净,没有烘干就用来配制溶液
E.定容时,滴加蒸馏水,不慎加多高于刻度线,吸出少量水使凹液面最低点与刻度线相切
您最近一年使用:0次



