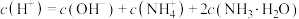室温下,通过下列实验探究NaHCO3、NaHSO3溶液的性质:
下列说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测定浓度为0.1mol·L-1NaHSO3溶液的pH,pH≈5 |
| 2 | 用pH试纸测定浓度为0.1mol·L-1NaHCO3溶液的pH,pH≈8 |
| 3 | 将浓度均为0.1mol·L-1的NaHSO3和Ba(OH)2溶液等体积混合,产生白色沉淀 |
| A.实验1可得0.1mol·L-1NaHSO3溶液中:Ka1(H2SO3)·Ka2(H2SO3)<10-10 |
B.实验2可得0.1mol·L-1NaHCO3溶液中:c(HCO )>c(CO )>c(CO )>c(H2CO3) )>c(H2CO3) |
C.实验3所得溶液中:c(Ba2+)·c(SO )=2.5×10−3 )=2.5×10−3 |
D.浓度均为0.1mol·L-1的NaHSO3和NaHCO3两份溶液中:c(HCO )+2c(CO )+2c(CO )<c(HSO )<c(HSO )+2c(SO )+2c(SO ) ) |
更新时间:2022-04-22 16:28:21
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温下,用 的盐酸滴定
的盐酸滴定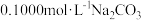 溶液
溶液 。用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是
。用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是

 的盐酸滴定
的盐酸滴定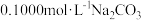 溶液
溶液 。用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是
。用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是 
A.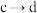 发生的主要离子反应: 发生的主要离子反应: |
B.在b点时, |
C.在d点时, |
D.在e点时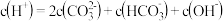 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】Cr(VI)常见存在形式有 、
、 、
、 和
和 。常温下,向
。常温下,向
 溶液中逐滴加入稀硫酸,含Cr(VI)各微粒的浓度随pH变化曲线如下所示。已知:
溶液中逐滴加入稀硫酸,含Cr(VI)各微粒的浓度随pH变化曲线如下所示。已知: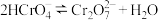 ,平衡常数
,平衡常数 。下列有关说法正确的是
。下列有关说法正确的是

 、
、 、
、 和
和 。常温下,向
。常温下,向
 溶液中逐滴加入稀硫酸,含Cr(VI)各微粒的浓度随pH变化曲线如下所示。已知:
溶液中逐滴加入稀硫酸,含Cr(VI)各微粒的浓度随pH变化曲线如下所示。已知: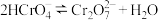 ,平衡常数
,平衡常数 。下列有关说法正确的是
。下列有关说法正确的是
A. 的电离平衡常数 的电离平衡常数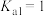 ; ;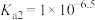 |
B.常温时,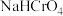 溶液的pH>7 溶液的pH>7 |
C.当pH<8时,Cr(VI)粒子浓度大小顺序可能为: |
D.调节pH为6~8时,主要反应离子方程式为: 且平衡常数 且平衡常数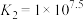 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】实验室使用pH传感器来测定某Na2A和NaHA混合溶液中NaHA的含量。用0.1 mol·L-1盐酸滴定该混合溶液,得到如下曲线。以下说法不正确 的是


| A.未滴定时该混合溶液中:c(A2-)+2c(OH-)=2c(H2A)+c(HA-)+2c(H+) |
| B.滴加10 mL盐酸时:c(Na+)=c(H2A)+c(HA-)+c(A2-)+c(Cl-) |
| C.滴加30 mL盐酸时:c(Na+)=c(Cl-)>c(H2A)>c(H+)>c(OH-) |
| D.将等浓度的H2A水溶液和等浓度的Na2A混合,溶液可能显酸性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知25℃时CH3COOH的电离常数K=1.6×10-5.该温度下向20ml 0.01mol•L-1 CH3COOH溶液中逐滴加入0.01mol•L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是
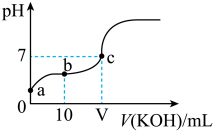

| A.a点溶液中c(H+)为4.0×10-5mol/L |
| B.c点溶液中的离子浓度大小顺序为c(K+)>c(CH3COO-)>c(H+)=c(OH-) |
| C.V=20 |
| D.a、b、c三点中水的电离程度最大的是c点 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,下列溶液中各粒子的物质的量浓度关系正确的是
| A.0.1 mol·L-1的氨水中,c(NH4+)=c(OH-)=0.1 mol·L-1 |
| B.NH4Cl溶液中,若溶液的pH=6,则c(Cl-)-c(NH4+)=9.9×10-7 mol·L-1 |
| C.0.1 mol·L-1的Na2SO4溶液中,c(SO42-)>c(Na+)>c(OH-)=c(H+) |
| D.0.1 mol·L-1的Na2SO3溶液中,c(Na+)=2 c(SO32-)+c(HCO3-)+c(H2SO3) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】室温下,甘氨酸在水溶液中主要以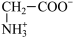 、
、 和
和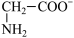 三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )
三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )

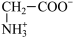 、
、 和
和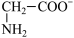 三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )
三种微粒形式存在,实验测得不同pH甘氨酸溶液中各成分分布分数δ与pH关系如图所示。下列说法正确的是( )
| A.a点溶液中,水的电离程度大于b点 |
B.c点溶液中,c(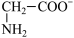 )>c( )>c(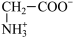 ) ) |
C.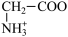 +H2O +H2O 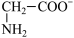 +H3O+的平衡常数为x +H3O+的平衡常数为x |
D.a点溶液中,存在关系式:c( )+c(H+)=c( )+c(H+)=c(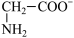 )+c(OH-) )+c(OH-) |
您最近一年使用:0次



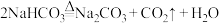
 比“盐析”前溶液
比“盐析”前溶液 、
、 的浓度更大
的浓度更大
 10-9
10-9 。初始温度25℃时,向
。初始温度25℃时,向 氨水中滴加
氨水中滴加 的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。下列说法不正确的是
的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。下列说法不正确的是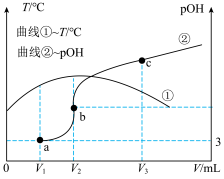
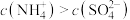
 的水解平衡常数:
的水解平衡常数: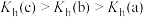
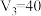 ,则c点对应溶液中
,则c点对应溶液中