利用CO2和CH4反应制备合成气(CO、H2)的原理是CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH>0。温度为T℃时,该反应的平衡常数为K。下列说法正确的是
2CO(g)+2H2(g) ΔH>0。温度为T℃时,该反应的平衡常数为K。下列说法正确的是
 2CO(g)+2H2(g) ΔH>0。温度为T℃时,该反应的平衡常数为K。下列说法正确的是
2CO(g)+2H2(g) ΔH>0。温度为T℃时,该反应的平衡常数为K。下列说法正确的是| A.K越大,说明反应速率、CO2的平衡转化率越大 |
| B.增大压强,平衡向逆反应方向移动,K减小 |
| C.升高温度,反应速率和平衡常数K都增大 |
| D.加入催化剂,能提高合成气的平衡产率 |
21-22高三下·海南海口·期中 查看更多[6]
海南省海口市2021-2022学年高三下学期学生学科能力诊断化学试题辽宁省协作校2022-2023学年高二上学期期中考试化学试题辽宁省辽南2022-2023学年高二上学期期中考试化学试题(已下线)第05讲 影响化学平衡的因素-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)辽宁省鞍山市岫岩满族自治县2022-2023学年高二上学期11月期中考试化学试题陕西师范大学附属中学2022-2023学年高一下学期6月期末考试化学试题
更新时间:2022/04/26 16:07:03
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列事实不能用平衡移动原理解释的是
A. 溶液中加入固体KSCN后颜色变深 溶液中加入固体KSCN后颜色变深 |
| B.实验室用排饱和食盐水的方法收集氯气 |
C.工业合成氨:  ,采用400℃~500℃的高温条件 ,采用400℃~500℃的高温条件 |
D.工业制备 : :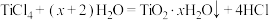 ,加入大量水,同时加热 ,加入大量水,同时加热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定条件下密闭容器中发生反应:NO(g) + CO(g)  1/2N2(g) + CO2(g) △H = -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
1/2N2(g) + CO2(g) △H = -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
 1/2N2(g) + CO2(g) △H = -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
1/2N2(g) + CO2(g) △H = -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是| A.升高温度 | B.充入NO | C.增大压强 | D.加催化剂 |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
名校
【推荐1】在起始温度均为T℃、容积均为 的密闭容器A(恒温)、B(绝热)中均加入
的密闭容器A(恒温)、B(绝热)中均加入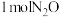 和
和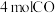 ,发生反应
,发生反应
 。已知:
。已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数,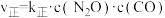 ,
,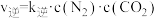 ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法中正确的是
的转化率随时间的变化关系如图所示。下列说法中正确的是
 的密闭容器A(恒温)、B(绝热)中均加入
的密闭容器A(恒温)、B(绝热)中均加入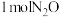 和
和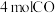 ,发生反应
,发生反应
 。已知:
。已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数,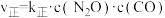 ,
,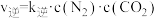 ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法中正确的是
的转化率随时间的变化关系如图所示。下列说法中正确的是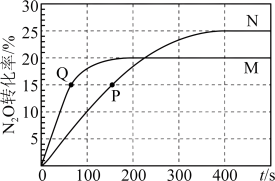
A.用 的浓度变化表示曲线N在 的浓度变化表示曲线N在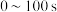 内的平均速率为 内的平均速率为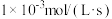 |
B. 与 与 浓度比为 浓度比为 时,标志此反应已达平衡 时,标志此反应已达平衡 |
C.曲线M、N的平衡常数大小为: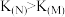 |
D.T℃时,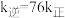 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)⇌2NH3(g) △H=-92.4kJ/moL。实验测得起始、平衡时的有关数据如下表:
下列叙述错误 的是
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.1kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A.容器①、②中反应的平衡常数相等 |
B.平衡时,两个容器中NH3的体积分数均为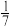 |
| C.容器②中达平衡时放出的热量Q=23.1kJ |
| D.若容器①体积为0.5L,则平衡时放出的热量小于23.1kJ |
您最近一年使用:0次
【推荐3】O3也是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生反应如下:
反应①O3 O2+[O] ΔH1>0,平衡常数为K1
O2+[O] ΔH1>0,平衡常数为K1
反应②[O]+O3 2O2 ΔH2<0,平衡常数为K2
2O2 ΔH2<0,平衡常数为K2
总反应:2O3 3O2 ΔH<0,平衡常数为K
3O2 ΔH<0,平衡常数为K
下列叙述正确的是
反应①O3
 O2+[O] ΔH1>0,平衡常数为K1
O2+[O] ΔH1>0,平衡常数为K1反应②[O]+O3
 2O2 ΔH2<0,平衡常数为K2
2O2 ΔH2<0,平衡常数为K2总反应:2O3
 3O2 ΔH<0,平衡常数为K
3O2 ΔH<0,平衡常数为K下列叙述正确的是
| A.压强增大,K2减小 | B.总反应中当2v正(O2)=3v逆(O3)时,反应达到平衡 |
| C.[O]为催化剂 | D.K=K1+K2 |
您最近一年使用:0次

 的转化率
的转化率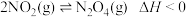 ,测定
,测定 相对分子质量时采用“高温低压”,是因为“高温低压”平衡都向逆方向移动,有利于测定
相对分子质量时采用“高温低压”,是因为“高温低压”平衡都向逆方向移动,有利于测定

