某化学兴趣小组进行了实验:向2支试管中分别加入0.5 g Na2CO3固体和0.5 g NaHCO3固体,再分别加入30 mL0.3 mol·L-1盐酸,充分反应后,用手触摸试管,明显感觉到加Na2CO3固体的试管变热了,加NaHCO3固体的试管变冷了。甲同学由此得出结论: (aq)+2H+(aq)=H2O(l)+CO2(g) △H1<0,
(aq)+2H+(aq)=H2O(l)+CO2(g) △H1<0, (aq)+H+ (aq) =H2O(l) +CO2(g) △H2>0。回答下列问题:
(aq)+H+ (aq) =H2O(l) +CO2(g) △H2>0。回答下列问题:
(1)乙同学认为该实验不一定能得到甲同学的结论,因为碳酸钠或碳酸氢钠固体溶于水时会有能量变化,乙同学的观点_______ (填“合理”或“不合理”)。
(2)查阅资料:
反应I: (aq)+2H+(aq)=H2O(l)+CO2(g) △H1=-12.14kJ· mol-1
(aq)+2H+(aq)=H2O(l)+CO2(g) △H1=-12.14kJ· mol-1
反应II: (aq)+H+(aq)=H2O(l) +CO2(g) △H2 +12.64 kJ·mol-1
(aq)+H+(aq)=H2O(l) +CO2(g) △H2 +12.64 kJ·mol-1
反应III: (aq)+ H+ (aq)=
(aq)+ H+ (aq)= (aq) △H3=
(aq) △H3=_______ kJ·mol-1
②向VmLc mol·L-1碳酸钠溶液中,逐滴加入2V mL c mol·L-1稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是_______ (填标号)。
A.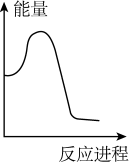 B.
B.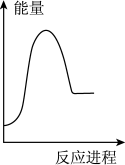 C.
C.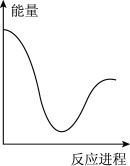 D.
D.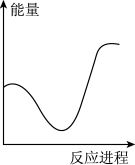
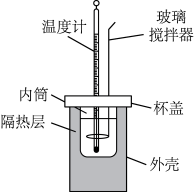
(3)该化学兴趣小组用如图所示装置设计实验验证碳酸钠、碳酸氢钠分别与稀盐酸反应的热效应。
表格一:
表格二:
表格三:
实验操作:将试剂1与试剂2混合,测混合后溶液的温度,静置,冷却至定温,再将试剂3与之前的。混合溶液混合,再测混合溶液的温度。
①实验中玻璃搅拌器的使用方法是_______ (填 “顺时针搅动”“逆时针搅动”或“上下移动”)。
②表格二对应实验得出的结论是_______ 。
③反应IV:Na2CO3(s)+2H+(aq)= 2Na+(aq)+H2O(l)+CO2(g) △H4;
反应V:NaHCO3(s)+H+(aq)=Na+(aq)+H2O(1)+CO2(g) △H5
则△H1_______ △H4(填“>”“ <”或“=”,下同),△H2_______ △H5。
 (aq)+2H+(aq)=H2O(l)+CO2(g) △H1<0,
(aq)+2H+(aq)=H2O(l)+CO2(g) △H1<0, (aq)+H+ (aq) =H2O(l) +CO2(g) △H2>0。回答下列问题:
(aq)+H+ (aq) =H2O(l) +CO2(g) △H2>0。回答下列问题:(1)乙同学认为该实验不一定能得到甲同学的结论,因为碳酸钠或碳酸氢钠固体溶于水时会有能量变化,乙同学的观点
(2)查阅资料:
反应I:
 (aq)+2H+(aq)=H2O(l)+CO2(g) △H1=-12.14kJ· mol-1
(aq)+2H+(aq)=H2O(l)+CO2(g) △H1=-12.14kJ· mol-1反应II:
 (aq)+H+(aq)=H2O(l) +CO2(g) △H2 +12.64 kJ·mol-1
(aq)+H+(aq)=H2O(l) +CO2(g) △H2 +12.64 kJ·mol-1反应III:
 (aq)+ H+ (aq)=
(aq)+ H+ (aq)= (aq) △H3=
(aq) △H3=②向VmLc mol·L-1碳酸钠溶液中,逐滴加入2V mL c mol·L-1稀盐酸。下列图象中,能正确表示该反应过程中的能量变化的是
A.
 B.
B. C.
C. D.
D.
(3)该化学兴趣小组用如图所示装置设计实验验证碳酸钠、碳酸氢钠分别与稀盐酸反应的热效应。

表格一:
| 试剂1 | 试剂2混合前温度/℃ | 混合后温度/℃ |
| 0.5 g Na2CO3 | 40mL HCl 19.0 | 21.7 |
| 0.5 g NaHCO3 | 40 mL HCl 19.0 | 18.1 |
| 试剂1 | 试剂2混合前温度/℃ | 溶解后温度/℃ | 静置后的温度/℃ | 试剂3混合前温度/℃ | 混合后温度/℃ |
| 0.5 g Na2CO3 | 10mLH2O19.0 | 22.3 | 19.0 | 10mLH2O19.0 | 19.0 |
| 0.5 g NaHCO3 | 10mLH2O19.0 | 17.5 | 19.0 | 10mLH2O19.0 | 19.0 |
| 试剂1 | 试剂2混合温度/℃ | 溶解后温度/℃ | 静置后的温度/℃ | 试剂3混合前温度/℃ | 混合后温度/℃ |
| 0.5 g Na2CO3 | 10mLH2O19.0 | 22.3 | 19.0 | 10mLHCl19.0 | 20.5 |
| 0.5 g NaHCO3 | 10mLH2O19.0 | 17.5 | 19.0 | 10mLHCl19.0 | 18.3 |
①实验中玻璃搅拌器的使用方法是
②表格二对应实验得出的结论是
③反应IV:Na2CO3(s)+2H+(aq)= 2Na+(aq)+H2O(l)+CO2(g) △H4;
反应V:NaHCO3(s)+H+(aq)=Na+(aq)+H2O(1)+CO2(g) △H5
则△H1
更新时间:2022-04-26 22:44:12
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验小组设计了下图所示的5组实验,探究化学能与热能的转化。___________ ,反应的化学方程式是___________ 。
(2)实验②中反应的能量变化可用下图中的_______ (填序号A或B)表示_______ (填序号)
(4)从微观角度分析实验⑤化学反应中能量变化的原因:___________ 、___________ (填“吸收”或“释放”)。氢气与氧气反应生成1mol水蒸气时,释放___________ kJ能量。
(5)当前,很多地区倡导用天然气替代煤作为家用燃料,从尽可能多的角度分析其原因是___________ 。已知:

(2)实验②中反应的能量变化可用下图中的

(4)从微观角度分析实验⑤化学反应中能量变化的原因:

(5)当前,很多地区倡导用天然气替代煤作为家用燃料,从尽可能多的角度分析其原因是
| 燃料 | 燃烧释放的能量(每1千克) |
| 天然气 | 55812kJ |
| 煤 | 20908kJ |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】工业尾气H2S对环境和人体健康产生危害,必须经过处理才可排放。依据题意回答下列问题:
(1)生物脱硫可处理含H2S的烟气,过程中使用的硫杆菌是一种微生物。
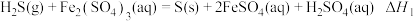

①反应 的
的 =
=_______ 。
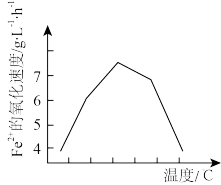
②若反应温度过高,反应速率下降(如图),其原因是_______ 。
(2)科研工作者利用微波法处理尾气中的H2S并回收H2和S,反应为: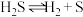 ,一定条件下,H2S的转化率随温度变化的曲线如图。
,一定条件下,H2S的转化率随温度变化的曲线如图。
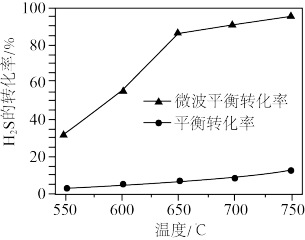
①H2S分解生成H2和S的反应为_______ 反应(填“吸热”或“放热”)。
②微波的作用是_______ 。
(3)利用电化学法也可处理尾气H2S。为避免硫磺沉积在阳极,将氧化吸收和电解制氢过程分开进行,装置如下图所示。氧化吸收器中为Fe2(SO4)3溶液,电解反应器中,以石墨为阳极,以 为阴极,中间用质子交换膜隔开。
为阴极,中间用质子交换膜隔开。
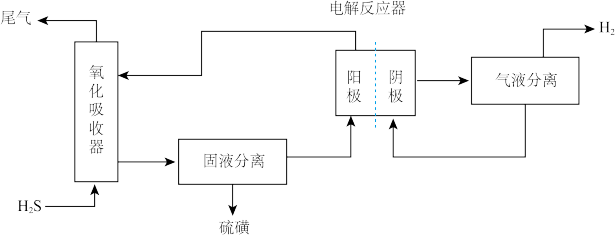
①氧化吸收器中反应的离子方程式为_______ 。
②电解反应器中,阴极的电极反应式为_______ 。
③电解反应器的作用是_______ (写出2点)。
(1)生物脱硫可处理含H2S的烟气,过程中使用的硫杆菌是一种微生物。
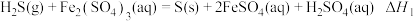

①反应
 的
的 =
=②若反应温度过高,反应速率下降(如图),其原因是

(2)科研工作者利用微波法处理尾气中的H2S并回收H2和S,反应为:
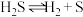 ,一定条件下,H2S的转化率随温度变化的曲线如图。
,一定条件下,H2S的转化率随温度变化的曲线如图。
①H2S分解生成H2和S的反应为
②微波的作用是
(3)利用电化学法也可处理尾气H2S。为避免硫磺沉积在阳极,将氧化吸收和电解制氢过程分开进行,装置如下图所示。氧化吸收器中为Fe2(SO4)3溶液,电解反应器中,以石墨为阳极,以
 为阴极,中间用质子交换膜隔开。
为阴极,中间用质子交换膜隔开。
①氧化吸收器中反应的离子方程式为
②电解反应器中,阴极的电极反应式为
③电解反应器的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、P、Q是原子序数依次增大的短周期主族元素,其中X的一种核素中没有中子,Y的单质和Z的单质是空气的主要成分,Z和Q同主族。做焰色试验时P元素的焰色为黄色。回答下列问题:
(1)X、Y、Z、P、Q五种元素的原子半径从大到小的顺序为_______ (用元素符号表示)。
(2)M是由X、Y元素组成的含有10个电子的分子,M的空间构型为_______ 。
(3) 可用作医药原料、照相乳剂的防腐剂。
可用作医药原料、照相乳剂的防腐剂。 可由
可由 与
与 反应制备,副产物为PZX和M。
反应制备,副产物为PZX和M。
①PZX中含有的化学键类型为_______ , 的电子式为
的电子式为_______ 。
②上述制备 的化学方程式为
的化学方程式为_______ 。
(4)Z和Q的简单气态氢化物中,热稳定性更好的是_______ (填化学式),从化学键的角度解释Z的简单气态氢化物的分解反应为吸热反应的原因:_______ 。
(1)X、Y、Z、P、Q五种元素的原子半径从大到小的顺序为
(2)M是由X、Y元素组成的含有10个电子的分子,M的空间构型为
(3)
 可用作医药原料、照相乳剂的防腐剂。
可用作医药原料、照相乳剂的防腐剂。 可由
可由 与
与 反应制备,副产物为PZX和M。
反应制备,副产物为PZX和M。①PZX中含有的化学键类型为
 的电子式为
的电子式为②上述制备
 的化学方程式为
的化学方程式为(4)Z和Q的简单气态氢化物中,热稳定性更好的是
您最近一年使用:0次
【推荐1】脱除沼气中的H2S具有重要意义,脱除H2S有多种方法。
(1)受热分解法。将H2S和CH4混合气导入热解器,反应分两步进行。
反应Ⅰ:2H2S(g)=2H2(g)+S2(g) ΔH1 =169.8kJ·mol-1
反应Ⅱ:CH4(g)+S2(g)=CS2(g)+2H2(g) ΔH2 =63.7kJ·mol-1
现将H2S和CH4按照2:1体积比投料,并用N2稀释。在常压和不同温度下,反应相同时间后,H2、S2和CS2的体积分数随温度的变化关系如图所示。___________ 。
②1050℃时,H2的体积分数为___________ 。
③在950℃~1150℃范围内,其他条件不变,随着温度的升高,S2(g)的体积分数先增大而后减小,可能是___________ 。
(2)光电催化法。某光电催化法脱除H2S的原理如图所示。___________ 。
②与受热分解法相比,光电催化法的优点是___________ 。
(3)催化重整法。Fe2O3可以用作脱除H2S的催化剂,脱除过程如图所示。___________ 。
②脱除一段时间后,催化剂的活性降低,原因是___________ 。
(1)受热分解法。将H2S和CH4混合气导入热解器,反应分两步进行。
反应Ⅰ:2H2S(g)=2H2(g)+S2(g) ΔH1 =169.8kJ·mol-1
反应Ⅱ:CH4(g)+S2(g)=CS2(g)+2H2(g) ΔH2 =63.7kJ·mol-1
现将H2S和CH4按照2:1体积比投料,并用N2稀释。在常压和不同温度下,反应相同时间后,H2、S2和CS2的体积分数随温度的变化关系如图所示。
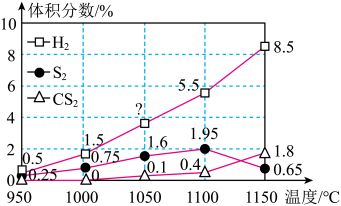
②1050℃时,H2的体积分数为
③在950℃~1150℃范围内,其他条件不变,随着温度的升高,S2(g)的体积分数先增大而后减小,可能是
(2)光电催化法。某光电催化法脱除H2S的原理如图所示。

②与受热分解法相比,光电催化法的优点是
(3)催化重整法。Fe2O3可以用作脱除H2S的催化剂,脱除过程如图所示。
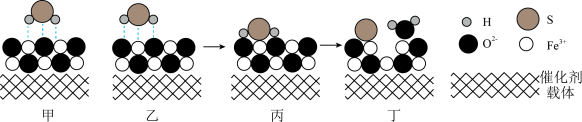
②脱除一段时间后,催化剂的活性降低,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氢气是一种常用的化工原料,如合成氨和尿素[CO(NH2)2]等。
(1)以H2合成CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g)=2NH3(g)ΔH1=-92.4 kJ·mol-1
②NH3(g)+ CO2(g)=
CO2(g)= NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
③NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l)ΔH3=+72.5 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为__________ 。
(2)电解制H2的原理为C(s)+2H2O(l)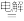 CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
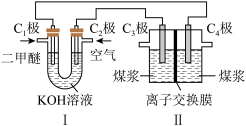
①分别写出电极C1和C3的电极反应式__________________ ;___________________ 。
②离子交换膜可能是________ (填字母)。
a.阳离子交换膜 b.阴离子交换膜 c.质子交换膜
③已知4.6 g二甲醚参与反应,假设装置Ⅰ的能量转化率为100%,C4极收集到11.2L(标准状况)气体,装置Ⅱ的电流效率η=________ 。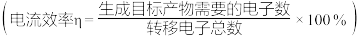
(1)以H2合成CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g)=2NH3(g)ΔH1=-92.4 kJ·mol-1
②NH3(g)+
 CO2(g)=
CO2(g)= NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1③NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l)ΔH3=+72.5 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为
(2)电解制H2的原理为C(s)+2H2O(l)
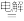 CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
①分别写出电极C1和C3的电极反应式
②离子交换膜可能是
a.阳离子交换膜 b.阴离子交换膜 c.质子交换膜
③已知4.6 g二甲醚参与反应,假设装置Ⅰ的能量转化率为100%,C4极收集到11.2L(标准状况)气体,装置Ⅱ的电流效率η=
您最近一年使用:0次
【推荐3】(1)甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为:CO(g)+2H2(g) CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。
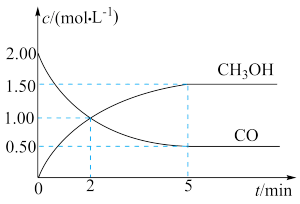
①从反应开始到5min,用一氧化碳表示的平均反应速率v(CO)=____________ 。
②下列说法正确的是____________ (填字母序号)。
A.达到平衡时,H2的转化率为65%
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充入氩气,反应速率减小
D.2min前v(正)>v(逆),2min后v(正)=v(逆)
(2)碳与水蒸气反应制取H2的相关反应如下:
Ⅰ:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △H= - 43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(S) △H= - 178.3kJ/mol
计算反应C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g)的△H=
CaCO3(s)+2H2(g)的△H=__________ kJ/mol;
若K1、K2、K3分别为反应Ⅰ、Ⅱ、Ⅲ的平衡常数,该平衡常数K=__________ (用K1、K2、K3表示)。
②对于可逆反应C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是________ 。(填字母)
A.降低体系的温度 B.压缩容器的体积
C.增加CaO的量 D.选用适当的催化剂
 CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。
①从反应开始到5min,用一氧化碳表示的平均反应速率v(CO)=
②下列说法正确的是
A.达到平衡时,H2的转化率为65%
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充入氩气,反应速率减小
D.2min前v(正)>v(逆),2min后v(正)=v(逆)
(2)碳与水蒸气反应制取H2的相关反应如下:
Ⅰ:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △H= - 43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(S) △H= - 178.3kJ/mol
计算反应C(s)+2H2O(g)+CaO(s)
 CaCO3(s)+2H2(g)的△H=
CaCO3(s)+2H2(g)的△H=若K1、K2、K3分别为反应Ⅰ、Ⅱ、Ⅲ的平衡常数,该平衡常数K=
②对于可逆反应C(s)+2H2O(g)+CaO(s)
 CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是A.降低体系的温度 B.压缩容器的体积
C.增加CaO的量 D.选用适当的催化剂
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
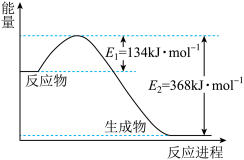
(1)如图是1 mol NO2和1 mol CO反应生成CO2 和NO过程中的能量变化示意图,请写出NO2 和CO反应的热化学方程式__________________________________ 。
(2)在0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:
请回答下列问题:
①试比较K1、K2的大小,K1______ K2(填“>”、“=” 或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是_________ (填序号字母)。
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.3v正(N2)=v逆(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
③400℃时,反应2NH3(g) N2(g) + 3H2(g) 的平衡常数K为
N2(g) + 3H2(g) 的平衡常数K为_________ 。当测得NH3、N2、H2的浓度分别为3 mol • L−1、2 mol • L−1、1 mol • L−1时,则该反应的v正(N2)______ v逆(N2)(填“>”、“=” 或“<”)。
(3)在容积为2 L的密闭容器中,充入一定量CO2和H2合成甲醇(CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-58 kJ·mol−1),在其他条件不变时,温度T1、T2对反应的影响图像如图。
CH3OH(g)+H2O(g) ΔH=-58 kJ·mol−1),在其他条件不变时,温度T1、T2对反应的影响图像如图。
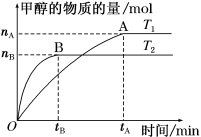
①温度为T1时,从反应到平衡,生成甲醇的平均速率为v(CH3OH)=______ mol·L−1·min−1。
②图示的温度T1______ T2(填“>”、“=” 或“<”)。
(1)如图是1 mol NO2和1 mol CO反应生成CO2 和NO过程中的能量变化示意图,请写出NO2 和CO反应的热化学方程式

(2)在0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
请回答下列问题:
①试比较K1、K2的大小,K1
②下列各项能作为判断该反应达到化学平衡状态的依据是
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.3v正(N2)=v逆(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
③400℃时,反应2NH3(g)
 N2(g) + 3H2(g) 的平衡常数K为
N2(g) + 3H2(g) 的平衡常数K为(3)在容积为2 L的密闭容器中,充入一定量CO2和H2合成甲醇(CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-58 kJ·mol−1),在其他条件不变时,温度T1、T2对反应的影响图像如图。
CH3OH(g)+H2O(g) ΔH=-58 kJ·mol−1),在其他条件不变时,温度T1、T2对反应的影响图像如图。
①温度为T1时,从反应到平衡,生成甲醇的平均速率为v(CH3OH)=
②图示的温度T1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】中国力争在2030年前实现碳达峰,2060年前实现碳中和。为推动实现碳中和的愿景,探索 资源化利用前景广阔。
资源化利用前景广阔。
Ⅰ. 重整反应,可以生成合成气(CO和
重整反应,可以生成合成气(CO和 )。
)。
已知:①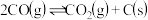
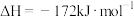
②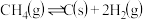
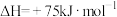
(1)催化重整反应发生的同时,还发生了积碳反应,即反应①和②。实验表明,低温、高压时会有显著积炭产生,说明此条件下积碳主要由反应___________ 产生。(填“①”或“②”)
(2)催化重整反应的热化学方程式为___________ 。
(3)该重整反应也可用于太阳能、核能、高温废热等的储存,储能研究是另一研究热点。反应可以储能的原因是___________ 。
Ⅱ.利用光电催化反应器,实现 资源化的同时产生电能。
资源化的同时产生电能。
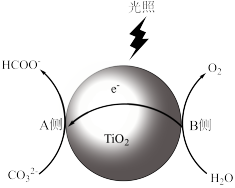
(4)如图所示,以 为催化剂,在光照条件下可将
为催化剂,在光照条件下可将 转化为
转化为 等有机物。生成
等有机物。生成 的过程可描述为
的过程可描述为___________ 。
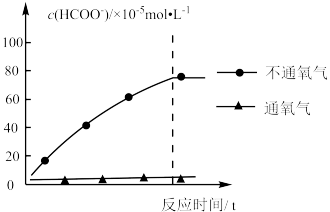
(5)以体积相同的0.25
 溶液为反应物,不同条件对生成的
溶液为反应物,不同条件对生成的 浓度影响如图所示。相同时间内溶液中通入氧气时
浓度影响如图所示。相同时间内溶液中通入氧气时 浓度明显低于不通氧气时,可能的原因是
浓度明显低于不通氧气时,可能的原因是___________ 。
 资源化利用前景广阔。
资源化利用前景广阔。Ⅰ.
 重整反应,可以生成合成气(CO和
重整反应,可以生成合成气(CO和 )。
)。已知:①
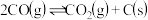
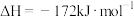
②
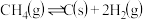
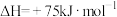
(1)催化重整反应发生的同时,还发生了积碳反应,即反应①和②。实验表明,低温、高压时会有显著积炭产生,说明此条件下积碳主要由反应
(2)催化重整反应的热化学方程式为
(3)该重整反应也可用于太阳能、核能、高温废热等的储存,储能研究是另一研究热点。反应可以储能的原因是
Ⅱ.利用光电催化反应器,实现
 资源化的同时产生电能。
资源化的同时产生电能。(4)如图所示,以
 为催化剂,在光照条件下可将
为催化剂,在光照条件下可将 转化为
转化为 等有机物。生成
等有机物。生成 的过程可描述为
的过程可描述为
(5)以体积相同的0.25

 溶液为反应物,不同条件对生成的
溶液为反应物,不同条件对生成的 浓度影响如图所示。相同时间内溶液中通入氧气时
浓度影响如图所示。相同时间内溶液中通入氧气时 浓度明显低于不通氧气时,可能的原因是
浓度明显低于不通氧气时,可能的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】对某市大气监测,发现首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。对SO2、NOx和PM2.5等进行研究具有重要意义。回答下列问题:
(1)将煤转化为水煤气(主要成为CO和H2),可减少SO2的排放。
已知:2H2(g)+O2(g)=2H2O(g) △H= -484 kJ/mol;2C(s)+O2(g)=2CO(g) △H=-221 kJ/mol。
写出焦炭与水蒸气反应生成水煤气的热化学方程式___________ 。
(2)汽车发动机工作时汽缸内会引发反应N2(g)+O2(g)=2NO(g) △H= +183 kJ/mol。
①1300℃时,1mol 空气(含0.8 mol N2和0.2 molO2,忽略其它气体)在某密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K=___________ 。
②汽车启动后,汽缸内温度越高,单位时间内NO排放量越大,解释原因___________ 。
(3)汽车燃油不完全燃烧时会产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。简述该设想不能实现的依据___________ 。目前,汽车装置尾气催化转化器,可使CO与NO反应转化为两种无毒害气体,从而减少污染。该反应的化学方程式为___________ 。
(4)将PM2.5样本用蒸馏水处理制成试液。测得该试液所含水溶性无机离子的化学组分及其浓度如下表:
根据表中数据计算试液的pH=___________ 。
(1)将煤转化为水煤气(主要成为CO和H2),可减少SO2的排放。
已知:2H2(g)+O2(g)=2H2O(g) △H= -484 kJ/mol;2C(s)+O2(g)=2CO(g) △H=-221 kJ/mol。
写出焦炭与水蒸气反应生成水煤气的热化学方程式
(2)汽车发动机工作时汽缸内会引发反应N2(g)+O2(g)=2NO(g) △H= +183 kJ/mol。
①1300℃时,1mol 空气(含0.8 mol N2和0.2 molO2,忽略其它气体)在某密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K=
②汽车启动后,汽缸内温度越高,单位时间内NO排放量越大,解释原因
(3)汽车燃油不完全燃烧时会产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)。简述该设想不能实现的依据
(4)将PM2.5样本用蒸馏水处理制成试液。测得该试液所含水溶性无机离子的化学组分及其浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度(mol/L) | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
您最近一年使用:0次



