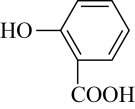
下列说法正确的是
| A.电子的运动状态可从能层、能级、轨道3个方面进行描述 |
| B.原子轨道与电子云都是用来形象描述电子运动状态的 |
C.基态24Cr原子的电子排布式是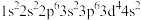 |
| D.BF3、CCl4分子中各原子最外层都能形成8电子结构 |
更新时间:2022-05-03 14:26:13
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列状态的Li原子中,能量最低的是
A.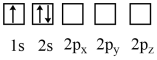 | B.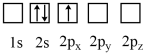 |
C.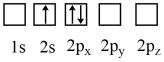 | D.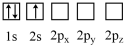 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.2p、3p、4p能级的轨道数依次增多 |
| B.第四周期基态原子末成对电子数为1的元素有4种 |
| C.基态B原子核外电子的运动状态有5种 |
D.ns能级的能量一定高于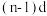 能级的能量 能级的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化合物甲[YW(XV4)2]和化合物乙(ZXV4)常用于游泳池的净水和消毒。V、W、X、Y、Z原子序数依次增大,V、X在元素周期表中同族且相邻,其中V元素在地壳中含量最高;基态W原子有7种空间运动状态不同的电子,基态Y原子的价层电子排布式为4s1,Z位于元素周期表第四周期ds区,基态时有1个单电子。下列说法正确的是
| A.简单离子半径:X>Y | B.简单氢化物稳定性:V<X |
| C.单质的沸点:Z>V>X | D.最高价氧化物对应水化物碱性最强的是W |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下表列出8种短周期元素的部分性质,下列有关叙述正确的是
| 元素 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/10-10m | 0.74 | 1.52 | 1.60 | 1.10 | 0.99 | 0.75 | 1.86 | 0.82 |
| 主要化合价 | -2 | +1 | +2 | +5、-3 | +7、-1 | +5、-3 | +1 | +3 |
| A.①和⑦形成的化合物中只含有离子键 |
| B.⑧的基态原子核外电子排布式为[Ne]3s23p1 |
| C.表格元素中,⑥的最高价氧化物对应水化物的酸性最强 |
| D.表格元素中,④和⑥的基态原子中未成对电子数最多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】对下列实验事实的理论解释不正确的
| 选项 | 实验事实 | 理论解释 |
| A | 环状S8分子结构如图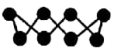 | S原子采取的杂化方式为sp3 |
| B | SO2易溶于水而难溶于CCl4 | SO2和水都是极性分子而CCl4为非极性分子 |
| C | HF分子热稳定性比HCl强 | HF分子间作用力比HCl强 |
| D | Fe2+比Fe3+的稳定性小 | Fe2+和Fe3+的价电子排布式分别为3d6、3d5,Fe3+的3d能级为半充满的稳定结构 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是 ( )
| A.将过量的氨水加入到CuSO4溶液中,最终得到蓝色沉淀 |
| B.电子排布式(22Ti)1s22s22p63s23p10违反了洪特规则 |
| C.由于氢键的作用,H2O的稳定性强于H2S |
| D.H-Cl的键能为431.8 kJ•mol﹣1,H-I的键能为298.7 kJ•mol﹣1,这可以说明HCl分子比HI分子稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.常温常压下,乙烯和丙烯的混合气体共14g,含原子数为3 |
B.1mol苯分子含碳碳双键数目为3 |
C.常温常压下,28g乙烯含σ键数目为6 |
D.1mol羟基所含电子数为10 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于物质的结构或性质的描述及解释都正确的是
| A.[Cu(NH3)4]SO4溶液中加入乙醇,析出晶体,是因为加入乙醇增大了溶剂极性 |
| B.沸点:对羟基苯甲醛>邻羟基苯甲醛,是由于对羟基苯甲醛分子间范德华力更强 |
| C.稳定性:H2OH2S,是由于水分子间存在氢键 |
| D.酸性:三氯乙酸>乙酸,是因为氯原子电负性大,增强了氧氢键的极性 |
您最近一年使用:0次

 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨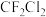 ⑩
⑩
 表示阿伏加德罗常数。下列说法正确的是
表示阿伏加德罗常数。下列说法正确的是 含有π键的数目为
含有π键的数目为
 和
和 的混合气体含有的原子数为
的混合气体含有的原子数为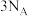
 的分子数为
的分子数为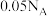
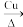 2CH3CHO+2H2O。下列说法正确的是
2CH3CHO+2H2O。下列说法正确的是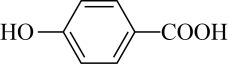 <
<