最近科研人员发现,用[Ni(cyclam)]2+(结构如图a)作电催化剂、二茂铁(结构如图c)作为牺牲电子供体,NH4PF6作为电解质和质子供体,CH3CN作溶剂,可实现有效催化还原CO2。
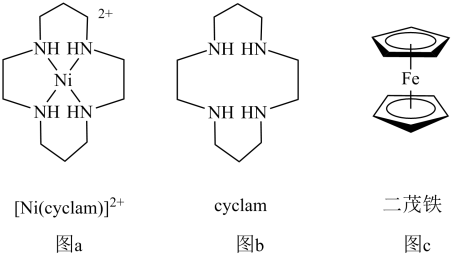
回答下列问题:
(1)基态Ni原子转化为基态Ni2+失去_______ 轨道的电子;基态Fe原子核外电子排布式为_______ 。
(2)NH4PF6中NH 空间构型为
空间构型为_______ ;N、P、F的电负性由大到小的顺序为_______ 。
(3)CH3CN分子中碳原子杂化方式为_______ 。
(4)已知3个及以上原子构成的离子团或分子中,原子有彼此平行的未参与杂化的p轨道电子,连贯重叠在一起构成π型化学键,又称为大π键,可用符号 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯中的大π键可表示为 。二茂铁[(C5H5)2Fe]中五元环的大π键可表示为
。二茂铁[(C5H5)2Fe]中五元环的大π键可表示为_______ 。
(5)[Ni (cyclam)]2+可由某些镍的化合物与cyclam 反应制得。[Ni(cyclam)]2+中,Ni2+的配位数为_______ ;cyclam可溶于水,而环十四烷不溶于水,其原因是_______ 。
(6)某镍、砷晶体结构如图所示。该晶体的密度为_______ g·cm-3(列出计算式即可)。
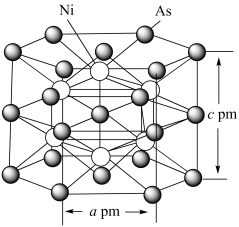

回答下列问题:
(1)基态Ni原子转化为基态Ni2+失去
(2)NH4PF6中NH
 空间构型为
空间构型为(3)CH3CN分子中碳原子杂化方式为
(4)已知3个及以上原子构成的离子团或分子中,原子有彼此平行的未参与杂化的p轨道电子,连贯重叠在一起构成π型化学键,又称为大π键,可用符号
 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯中的大π键可表示为 。二茂铁[(C5H5)2Fe]中五元环的大π键可表示为
。二茂铁[(C5H5)2Fe]中五元环的大π键可表示为(5)[Ni (cyclam)]2+可由某些镍的化合物与cyclam 反应制得。[Ni(cyclam)]2+中,Ni2+的配位数为
(6)某镍、砷晶体结构如图所示。该晶体的密度为

2022·河南开封·模拟预测 查看更多[2]
更新时间:2022-06-10 15:18:39
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】第III A主族元素有着广泛的应用,B可用作特种玻璃,Al可用作火箭和飞机外壳,Ga可用作半导体材料,In可用于电子仪器中,Tl可用于红外技术。回答下列问题:
(1)基态Ga原子的电子排布式为_______ ,有_______ 种不同运动状态的电子。
(2)B能形成很多类似于烃类的物质,比如B2H6,分子中B也形成四根键,但不含B-B键,试画出B2H6的结构式_______ 。此外B与N元素可形成无机苯B3N3H6,它与苯的结构很相似,该分子中N的杂化方式是_______ 。
(3)电解氧化铝需要添加冰晶石Na3AlF6,它的阴离子的空间结构为_______ ,它可通过以下反应制备:Al(OH)3 + 3NaOH + 6HF = Na3AlF6 + 6H2O,该反应涉及的5种元素电负性最大的是_______ 。
(4)AlF3,AlCl3熔点分别为1290 oC和192 oC,熔点呈现如此变化的原因是_______ 。
(5)H3BO3晶体形成层状结构,每一层的结构如下图所示,层与层之间距离为318 pm(大于氢键的长度),硼酸晶体属于_______ 晶体,晶体中含有的作用力有_______ ,在一层硼酸晶体结构中最小的重复单元含有_______ 个H3BO3分子。

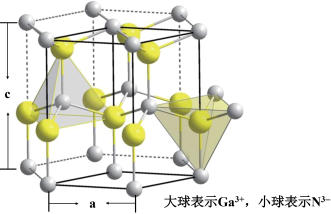
(6)GaN是二元Ⅲ-Ⅴ A族的直接带隙半导体,非常适合制造光电器件,GaN具有六方纤锌矿结构,晶胞示意图如下图所示,该晶胞的边长a = 318 pm,c = 517 pm。该GaN晶体的密度ρ =_______ g·cm-3。(只列计算式,NA表示阿伏加德罗常数)
(1)基态Ga原子的电子排布式为
(2)B能形成很多类似于烃类的物质,比如B2H6,分子中B也形成四根键,但不含B-B键,试画出B2H6的结构式
(3)电解氧化铝需要添加冰晶石Na3AlF6,它的阴离子的空间结构为
(4)AlF3,AlCl3熔点分别为1290 oC和192 oC,熔点呈现如此变化的原因是
(5)H3BO3晶体形成层状结构,每一层的结构如下图所示,层与层之间距离为318 pm(大于氢键的长度),硼酸晶体属于

(6)GaN是二元Ⅲ-Ⅴ A族的直接带隙半导体,非常适合制造光电器件,GaN具有六方纤锌矿结构,晶胞示意图如下图所示,该晶胞的边长a = 318 pm,c = 517 pm。该GaN晶体的密度ρ =

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】稀土正铁氧体RFeO3晶体是一类重要的多功能磁性材料,稳定的RFeO3晶体具有优异的磁光和光磁特性,我国科学家在磁光和光磁调控方面取得一系列重要研究进展。
回答下列问题:
(1)铁元素是构成人体的不可缺少的元素之一,亚铁离子是血红蛋白的重要组成成分。请写出Fe2+的核外电子排布式___________ ;铁的第四电离能I4远大于第三电离能I3的原因是___________ 。
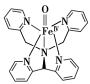
(2)某含铁络合物具有顺磁性,结构如图所示。组成该含铁络合物的第二周期元素中,电负性由大到小的顺序为___________ (用元素符号表示)。该含铁络合物中N原子的杂化方式为___________ ,碳原子价层电子对的空间构型为___________ 。
(3)铁在200 ℃、1×104 kPa压强下和一氧化碳反应,生成五羰基铁Fe(CO)5.Fe(CO)5为黄色液体,沸点103 ℃,Fe(CO)5属于___________ 晶体;铁在氯气中加热,生成三氯化铁,三氯化铁在300 ℃以上升华,气相为二聚体Fe2Cl6.Fe2Cl6中所含的化学键为___________ (填字母序号)。
A.离子键 B.共价键 C.配位键 D.氢键
(4)六方相RFeO3晶胞结构如图所示。R表示Sc与Lu元素,晶胞上下面面心为Sc,顶点为Lu,六方晶胞的高为p nm,正六边形底的边长为q nm。
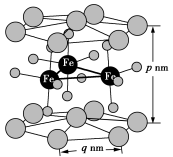
①六方相RFeO3的化学式为___________ 。
②RFeO3晶胞的密度是___________ g·cm−3。
回答下列问题:
(1)铁元素是构成人体的不可缺少的元素之一,亚铁离子是血红蛋白的重要组成成分。请写出Fe2+的核外电子排布式
(2)某含铁络合物具有顺磁性,结构如图所示。组成该含铁络合物的第二周期元素中,电负性由大到小的顺序为

(3)铁在200 ℃、1×104 kPa压强下和一氧化碳反应,生成五羰基铁Fe(CO)5.Fe(CO)5为黄色液体,沸点103 ℃,Fe(CO)5属于
A.离子键 B.共价键 C.配位键 D.氢键
(4)六方相RFeO3晶胞结构如图所示。R表示Sc与Lu元素,晶胞上下面面心为Sc,顶点为Lu,六方晶胞的高为p nm,正六边形底的边长为q nm。

①六方相RFeO3的化学式为
②RFeO3晶胞的密度是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】回答下列问题:
(1)Pt的电子排布式为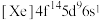 ,则Pt在元素周期表中的位置是
,则Pt在元素周期表中的位置是_______ ,处于_______ 区。
(2) 中阴离子的立体构型名称是
中阴离子的立体构型名称是_______ ,B、N、H的电负性由大到小的顺序为_______ 。
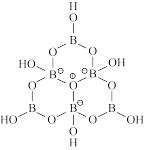
(3)科学家合成了一种含硼阴离子[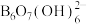 ],其结构如下图所示。其中硼原子的杂化方式为
],其结构如下图所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90,棱长为apm,密度为3 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。

①该晶体的化学式为_______ 。
②金属M原子与硼原子间最短距离为_______ pm。
③金属M的相对原子质量为_______ (列出表达式)。
(1)Pt的电子排布式为
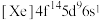 ,则Pt在元素周期表中的位置是
,则Pt在元素周期表中的位置是(2)
 中阴离子的立体构型名称是
中阴离子的立体构型名称是(3)科学家合成了一种含硼阴离子[
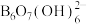 ],其结构如下图所示。其中硼原子的杂化方式为
],其结构如下图所示。其中硼原子的杂化方式为
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子;四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90,棱长为apm,密度为3
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
①该晶体的化学式为
②金属M原子与硼原子间最短距离为
③金属M的相对原子质量为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】有A、B、C、D、E五种元素。其相关信息如下
请回答下列问题:
(1)写出E元素原子基态时的电子排布式__ 。
(2)C元素的第一电离能比氧元素的第一电离能_____ (填“大”或“小”)。
(3)CA3分子中C原子的杂化轨道类型是__ 。
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有_____ (填序号)。
① 配位键 ② 金属键 ③ 极性共价键 ④非极性共价键 ⑤ 离子键 ⑥ 氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_______ (填字母)
a.平面正方形 b.正四面体 c.三角锥形 d. V 形
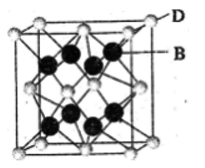
(5)B与D可形成离子化合物,其晶胞结构如下图所示。其中D离子的配位数为____ , 若该晶体的密度为ag/cm3,则B与D间最短距离是______ cm (写出表达式即可)。
| 元素 | 相关信息 |
| A | A原子的1s 轨道上只有l 个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
请回答下列问题:
(1)写出E元素原子基态时的电子排布式
(2)C元素的第一电离能比氧元素的第一电离能
(3)CA3分子中C原子的杂化轨道类型是
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有
① 配位键 ② 金属键 ③ 极性共价键 ④非极性共价键 ⑤ 离子键 ⑥ 氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为
a.平面正方形 b.正四面体 c.三角锥形 d. V 形
(5)B与D可形成离子化合物,其晶胞结构如下图所示。其中D离子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】锌是人体必需的微量元素,[Zn(NH3)4]CO3在生物活性等方面发挥重要的作用。
(1)Zn2+基态核外电子排布式为__ 。
(2)CO32-的空间构型为__ (用文字描述);[Zn(NH3)4]CO3中C、H、O、N四种元素的电负性由小到大的顺序为__ 。
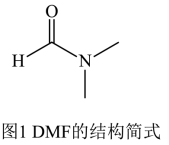
(3)某含锌配合物可用于模拟碳酸酐酶的催化活性,该配合物中含有DMF分子。DMF分子的结构如图1所示。DMF分子中碳原子轨道的杂化类型是__ ,1molDMF分子中含有σ键的数目为__ 。
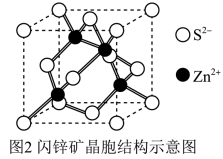
(4)闪锌矿可看作由Zn2+和S2-各自形成的面心立方结构相互穿插而成。其晶胞结构示意图如图2所示,与Zn2+距离相等且最近的Zn2+有__ 个。
(1)Zn2+基态核外电子排布式为
(2)CO32-的空间构型为
(3)某含锌配合物可用于模拟碳酸酐酶的催化活性,该配合物中含有DMF分子。DMF分子的结构如图1所示。DMF分子中碳原子轨道的杂化类型是

(4)闪锌矿可看作由Zn2+和S2-各自形成的面心立方结构相互穿插而成。其晶胞结构示意图如图2所示,与Zn2+距离相等且最近的Zn2+有

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】超分子在生命科学和物理学等领域中具有重要意义。由Mo将2个C60分子、2个p—甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。
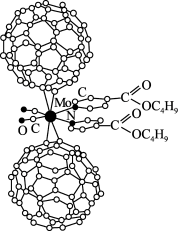
(1)Mo处于第五周期第VIB族,核外电子排布与Cr相似,它的基态价电子排布式是________ ;核外未成对电子数是________ 个。
(2)该超分子中配体CO提供孤电子对的原子是________ (填元素符号),p—甲酸丁酯吡啶配体中C原子的杂化方式有________ 。(已知吡啶可看做苯分子中的一个CH原子团被N取代的化合物)
(3)已知:C60分子中存在碳碳单、双键;C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;C60分子只含有五边形和六边形;多面体的顶点数V、面数F及棱边数E遵循欧拉定理:V+F-E=2。则一个C60分子的结构是由_____ 个五边形和____ 个六边形组成的球体。用文字简述C60跟F2在一定条件下反应所得的物质的组成:__________________ 。
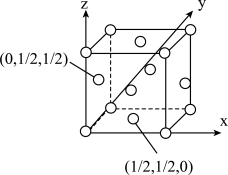
(4)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点的原子坐标均可以为(0,0,0)。钼(Mo)的一种立方晶系的晶体结构中,每个晶胞有2个Mo原子,其中Mo原子坐标是(0,0,0)及( ,
, ,
, )。根据以上信息,推断该晶体的原子堆积方式是
)。根据以上信息,推断该晶体的原子堆积方式是_____________ 。已知该晶体的密度是ρg·cm-3,Mo的摩尔质量是Mg·mol-1,阿伏加 德罗常数是NA,晶体中距离最近的Mo原子核之间的距离为_____ pm。

(1)Mo处于第五周期第VIB族,核外电子排布与Cr相似,它的基态价电子排布式是
(2)该超分子中配体CO提供孤电子对的原子是
(3)已知:C60分子中存在碳碳单、双键;C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;C60分子只含有五边形和六边形;多面体的顶点数V、面数F及棱边数E遵循欧拉定理:V+F-E=2。则一个C60分子的结构是由
(4)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点的原子坐标均可以为(0,0,0)。钼(Mo)的一种立方晶系的晶体结构中,每个晶胞有2个Mo原子,其中Mo原子坐标是(0,0,0)及(
 ,
, ,
, )。根据以上信息,推断该晶体的原子堆积方式是
)。根据以上信息,推断该晶体的原子堆积方式是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】利用 (铁氰化钾)可灵敏检验出溶液中的
(铁氰化钾)可灵敏检验出溶液中的 ,产生特征的蓝色,沉淀
,产生特征的蓝色,沉淀 (滕氏蓝),历史上普作为颜料而被广泛研究。回答下列问题:
(滕氏蓝),历史上普作为颜料而被广泛研究。回答下列问题:
(1)基态 的简化电子排布式为
的简化电子排布式为___________ ,基态 、
、 中未成对电子数之比为
中未成对电子数之比为___________ 。
(2) 中σ键与π键的个数比为___________;铁氰化钾中存在的化学键类型包括___________。
中σ键与π键的个数比为___________;铁氰化钾中存在的化学键类型包括___________。
(3)滕氏蓝晶体的微观结构如图所示。

图1不是滕氏蓝晶体的晶胞单元,理由是图1不是晶体中最小结构的重复单元。图2为滕氏蓝的晶胞结构,晶胞中与1个 等距且最近的
等距且最近的 的数目为
的数目为___________ ;已知 原子的坐标参数为
原子的坐标参数为 ,
, 原子为
原子为 ,则
,则 处
处 的坐标为
的坐标为___________ ;晶胞中 与
与 的核间距为
的核间距为 ,该晶胞密度为
,该晶胞密度为___________  (列出计算式即可,已知
(列出计算式即可,已知 的摩尔质量为
的摩尔质量为 )。
)。
 (铁氰化钾)可灵敏检验出溶液中的
(铁氰化钾)可灵敏检验出溶液中的 ,产生特征的蓝色,沉淀
,产生特征的蓝色,沉淀 (滕氏蓝),历史上普作为颜料而被广泛研究。回答下列问题:
(滕氏蓝),历史上普作为颜料而被广泛研究。回答下列问题:(1)基态
 的简化电子排布式为
的简化电子排布式为 、
、 中未成对电子数之比为
中未成对电子数之比为(2)
 中σ键与π键的个数比为___________;铁氰化钾中存在的化学键类型包括___________。
中σ键与π键的个数比为___________;铁氰化钾中存在的化学键类型包括___________。| A.离子键 | B.非极性键 | C.配位键 | D.金属键 |

图1不是滕氏蓝晶体的晶胞单元,理由是图1不是晶体中最小结构的重复单元。图2为滕氏蓝的晶胞结构,晶胞中与1个
 等距且最近的
等距且最近的 的数目为
的数目为 原子的坐标参数为
原子的坐标参数为 ,
, 原子为
原子为 ,则
,则 处
处 的坐标为
的坐标为 与
与 的核间距为
的核间距为 ,该晶胞密度为
,该晶胞密度为 (列出计算式即可,已知
(列出计算式即可,已知 的摩尔质量为
的摩尔质量为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】氨酸络合剂指含有—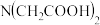 基团的有机化合物,它是一类具有广泛络合性能和强的络合能力的络合剂。
基团的有机化合物,它是一类具有广泛络合性能和强的络合能力的络合剂。
Ⅰ、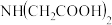 Ⅱ、
Ⅱ、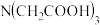 Ⅲ、
Ⅲ、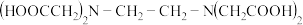
(1)基态氮原子价电子排布式为___________ 。
(2) 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为___________ 。
(3)Ⅰ、Ⅱ、Ⅲ都可以与 形成络合物
形成络合物
①铜元素位于元素周期表第四周期第___________ 族。
②预测___________ (填编号“Ⅰ”、“Ⅱ”、“Ⅲ”)与 形成的络合物最稳定。
形成的络合物最稳定。
(4)下列说法正确的有___________ 。
A.在Ⅰ、Ⅱ、Ⅲ中N原子采取的都是 杂化
杂化
B.在Ⅱ中C元素的电负性最大
C.在Ⅲ中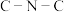 键角是
键角是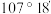
D.在Ⅲ中N元素的第一电离能最大。
E.在Ⅲ中碳氧键的键能均相等
(5)某杂志报道了一种磷化硼纳米颗粒作为高选择性 电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示:
电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示:
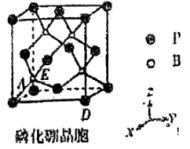
①磷化硼晶体中与硼原子距离最近且相等的硼原子数为___________ 。
②若图中A处磷原子坐标为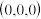 ,D处磷原子坐标为
,D处磷原子坐标为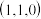 ,则E处的硼原子坐标为
,则E处的硼原子坐标为___________ 。
③已知磷化硼晶胞中A处磷原子与D处磷原子间的距离为a ,则硼原子与最近磷原子的核间距为
,则硼原子与最近磷原子的核间距为___________  。
。
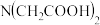 基团的有机化合物,它是一类具有广泛络合性能和强的络合能力的络合剂。
基团的有机化合物,它是一类具有广泛络合性能和强的络合能力的络合剂。Ⅰ、
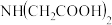 Ⅱ、
Ⅱ、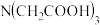 Ⅲ、
Ⅲ、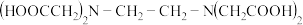
(1)基态氮原子价电子排布式为
(2)
 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为(3)Ⅰ、Ⅱ、Ⅲ都可以与
 形成络合物
形成络合物①铜元素位于元素周期表第四周期第
②预测
 形成的络合物最稳定。
形成的络合物最稳定。(4)下列说法正确的有
A.在Ⅰ、Ⅱ、Ⅲ中N原子采取的都是
 杂化
杂化B.在Ⅱ中C元素的电负性最大
C.在Ⅲ中
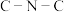 键角是
键角是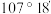
D.在Ⅲ中N元素的第一电离能最大。
E.在Ⅲ中碳氧键的键能均相等
(5)某杂志报道了一种磷化硼纳米颗粒作为高选择性
 电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示:
电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示:
①磷化硼晶体中与硼原子距离最近且相等的硼原子数为
②若图中A处磷原子坐标为
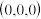 ,D处磷原子坐标为
,D处磷原子坐标为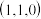 ,则E处的硼原子坐标为
,则E处的硼原子坐标为③已知磷化硼晶胞中A处磷原子与D处磷原子间的距离为a
 ,则硼原子与最近磷原子的核间距为
,则硼原子与最近磷原子的核间距为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
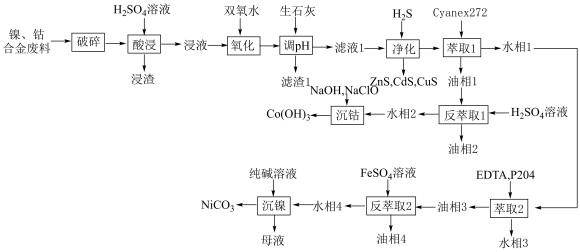
【推荐3】一种以镍钴合金废料(含Co、Ni、Fe、Cu、Al、Zn、Cd及其氧化物)为原料提取Co、Ni的工艺流程如下图所示。
(1)“破碎”和“酸浸”工序也可通过电解法来实现,电解装置中的阳极材料应选择___________ 。相对于“破碎”和“酸浸”,电解法的缺陷为___________ 。
(2)“氧化”的目的是___________ 。
(3)滤渣1的主要成分除 之外,还有
之外,还有___________ (填化学式)。
(4)“沉钴”工序, 转化为
转化为 的离子方程式为
的离子方程式为___________ 。
(5) 、
、 与EDTA均可形成稳定的环状离子,稳定性较强的是
与EDTA均可形成稳定的环状离子,稳定性较强的是___________ (填“ ”或“
”或“ ”)。“反萃取2”中Fe、Ni的存在形式与pH关系如图所示,该工序需控制的最佳pH是
”)。“反萃取2”中Fe、Ni的存在形式与pH关系如图所示,该工序需控制的最佳pH是___________ 。 是制备
是制备 的中间体。
的中间体。 和
和 煅烧均可得到
煅烧均可得到 ,前者得到的
,前者得到的 比表面积更大,其原因是
比表面积更大,其原因是___________ 。
(1)“破碎”和“酸浸”工序也可通过电解法来实现,电解装置中的阳极材料应选择
(2)“氧化”的目的是
(3)滤渣1的主要成分除
 之外,还有
之外,还有(4)“沉钴”工序,
 转化为
转化为 的离子方程式为
的离子方程式为(5)
 、
、 与EDTA均可形成稳定的环状离子,稳定性较强的是
与EDTA均可形成稳定的环状离子,稳定性较强的是 ”或“
”或“ ”)。“反萃取2”中Fe、Ni的存在形式与pH关系如图所示,该工序需控制的最佳pH是
”)。“反萃取2”中Fe、Ni的存在形式与pH关系如图所示,该工序需控制的最佳pH是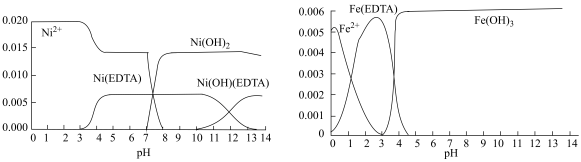
 是制备
是制备 的中间体。
的中间体。 和
和 煅烧均可得到
煅烧均可得到 ,前者得到的
,前者得到的 比表面积更大,其原因是
比表面积更大,其原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】AA705合金(含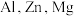 和
和 )几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
(1) 和
和 中阳离子基态核外电子排布式为
中阳离子基态核外电子排布式为_____________________ ,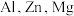 三种元素的第一电离能由大到小为
三种元素的第一电离能由大到小为_____________________ ;
(2)以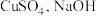 和抗坏血酸为原料,可制备
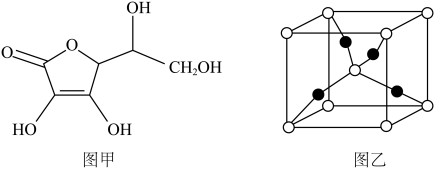
和抗坏血酸为原料,可制备 。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为
。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为_______________ ,推测抗坏血酸在水中的溶解性:_______________ (填“难溶于水”或“易溶于水”),一个 晶胞(见图2)中,
晶胞(见图2)中, 原子的数目为
原子的数目为_______________ ;
(3) 和
和 等配体都能与
等配体都能与 形成配离子。
形成配离子。 含
含______  键,中心离子的配位数为
键,中心离子的配位数为______________ ;
(4)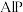 因杀虫效率高、廉价易得而被广泛应用。已知
因杀虫效率高、廉价易得而被广泛应用。已知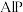 的熔点为2000℃,其晶胞结构如图所示。
的熔点为2000℃,其晶胞结构如图所示。
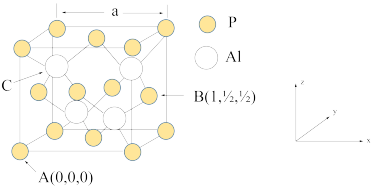
①磷化铝的晶体类型为______________ ,
②A、B点的原子坐标如图所示,则C点的原子坐标为___________ ,
③磷化铝的晶胞参数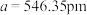 ,其密度为
,其密度为____________  (列出计算式即可,用
(列出计算式即可,用 表示阿伏加 德罗常数的值);
表示阿伏加 德罗常数的值);
(5) 具有对称的立体构型,
具有对称的立体构型, 中的两个
中的两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为________________ 。
 和
和 )几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:(1)
 和
和 中阳离子基态核外电子排布式为
中阳离子基态核外电子排布式为 三种元素的第一电离能由大到小为
三种元素的第一电离能由大到小为(2)以
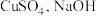 和抗坏血酸为原料,可制备
和抗坏血酸为原料,可制备 。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为
。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为 晶胞(见图2)中,
晶胞(见图2)中, 原子的数目为
原子的数目为
(3)
 和
和 等配体都能与
等配体都能与 形成配离子。
形成配离子。 含
含 键,中心离子的配位数为
键,中心离子的配位数为(4)
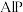 因杀虫效率高、廉价易得而被广泛应用。已知
因杀虫效率高、廉价易得而被广泛应用。已知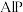 的熔点为2000℃,其晶胞结构如图所示。
的熔点为2000℃,其晶胞结构如图所示。
①磷化铝的晶体类型为
②A、B点的原子坐标如图所示,则C点的原子坐标为
③磷化铝的晶胞参数
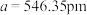 ,其密度为
,其密度为 (列出计算式即可,用
(列出计算式即可,用 表示阿伏加 德罗常数的值);
表示阿伏加 德罗常数的值);(5)
 具有对称的立体构型,
具有对称的立体构型, 中的两个
中的两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】如图为NaCl晶胞结构示意图(晶胞边长为anm)
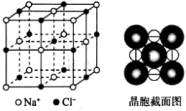
(1)能准确证明其是晶体的方法是___________ 。
(2)晶体中, 位于
位于 所围成的正
所围成的正___________ 面体的体心,该多面体的边长是___________  。
。
(3)晶体中在每个 的周围与它最近且等距离的
的周围与它最近且等距离的 共有
共有___________ 个。
(4) 半径与
半径与 半径的比值是
半径的比值是___________ (保留小数点后三位,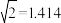 )。
)。
(5)在1413℃时,NaCl晶体转变成氯化钠气体。现有5.85gNaCl晶体,使其气化测得气体体积为1.12L(已换算为标准状况),则此时氯化钠气体的分子式为___________ 。

(1)能准确证明其是晶体的方法是
(2)晶体中,
 位于
位于 所围成的正
所围成的正 。
。(3)晶体中在每个
 的周围与它最近且等距离的
的周围与它最近且等距离的 共有
共有(4)
 半径与
半径与 半径的比值是
半径的比值是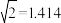 )。
)。(5)在1413℃时,NaCl晶体转变成氯化钠气体。现有5.85gNaCl晶体,使其气化测得气体体积为1.12L(已换算为标准状况),则此时氯化钠气体的分子式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
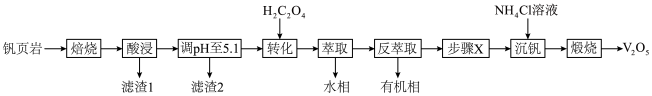
【推荐3】V有“工业味精”之称。工业上提取钒的工艺有多种,一种从钒页岩(一种主要含Si、Fe、Al、V元素的矿石)中提取V的工艺流程如下:
①“酸浸”时有VO 生成;
生成;
② 在有机溶剂中的溶解度大于水,“萃取”时离子的萃取顺序为
在有机溶剂中的溶解度大于水,“萃取”时离子的萃取顺序为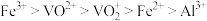 ;
;
③VO 和
和 可以相互转化。
可以相互转化。
回答下列问题:
(1)“焙烧”时可添加适量“盐对”NaCl- 与钒页岩形成混合物,这样做的目的是
与钒页岩形成混合物,这样做的目的是____________________ 。
(2)“滤渣1”除掉的主要杂质元素是_______ (填元素符号)。
(3) 作用是将VO
作用是将VO 转化为
转化为 ,转化的目的是
,转化的目的是_____________ ,发生的离子反应方程式为_____________________ 。
(4)①“沉钒”时,生成 沉淀,“步骤X”应该加入
沉淀,“步骤X”应该加入________ (填“氧化剂”或“还原剂”),写出“沉钒”时的离子反应方程式_______________________ 。
②以“沉钒率”( 沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高于80℃时沉钒率下降的原因是
沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高于80℃时沉钒率下降的原因是_______________ 。 可以溶解在NaOH溶液中,得到
可以溶解在NaOH溶液中,得到 ,
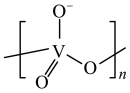
, 在不同的pH下可以得到不同聚合度的多钒酸盐,其阴离子呈如图所示的无限链状结构,其中一种酸式钒酸根离子可以表示为
在不同的pH下可以得到不同聚合度的多钒酸盐,其阴离子呈如图所示的无限链状结构,其中一种酸式钒酸根离子可以表示为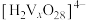 ,其中
,其中
________ 。 的立方晶胞如图所示,则在晶胞中,黑球代表的是
的立方晶胞如图所示,则在晶胞中,黑球代表的是_____ 原子。
①“酸浸”时有VO
 生成;
生成;②
 在有机溶剂中的溶解度大于水,“萃取”时离子的萃取顺序为
在有机溶剂中的溶解度大于水,“萃取”时离子的萃取顺序为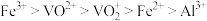 ;
;③VO
 和
和 可以相互转化。
可以相互转化。回答下列问题:
(1)“焙烧”时可添加适量“盐对”NaCl-
 与钒页岩形成混合物,这样做的目的是
与钒页岩形成混合物,这样做的目的是(2)“滤渣1”除掉的主要杂质元素是
(3)
 作用是将VO
作用是将VO 转化为
转化为 ,转化的目的是
,转化的目的是(4)①“沉钒”时,生成
 沉淀,“步骤X”应该加入
沉淀,“步骤X”应该加入②以“沉钒率”(
 沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高于80℃时沉钒率下降的原因是
沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高于80℃时沉钒率下降的原因是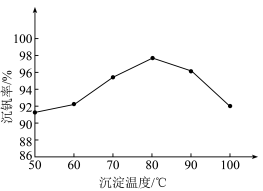
 可以溶解在NaOH溶液中,得到
可以溶解在NaOH溶液中,得到 ,
, 在不同的pH下可以得到不同聚合度的多钒酸盐,其阴离子呈如图所示的无限链状结构,其中一种酸式钒酸根离子可以表示为
在不同的pH下可以得到不同聚合度的多钒酸盐,其阴离子呈如图所示的无限链状结构,其中一种酸式钒酸根离子可以表示为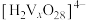 ,其中
,其中
 的立方晶胞如图所示,则在晶胞中,黑球代表的是
的立方晶胞如图所示,则在晶胞中,黑球代表的是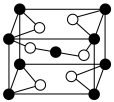
您最近一年使用:0次



