回答下列问题:
(1)对具有下列价电子排布的Ni或As进行光谱实验,用光谱仪一定能摄取到原子发射光谱的是____ (填字母)。
(2)Fe成为阳离子时首先失去____ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为____ 。
(3)羟基磷灰石[Ca(PO4)3OH]是牙齿中的重要矿物质,其中羟基(—OH)中氧原子的杂化方式为___ ,PO 的空间构型为
的空间构型为____ ,该化合物所含元素电负性最大的是____ 。
(4)向胆矾溶液中滴加氨水至过量,最终得到深蓝色的透明溶液,再加入乙醇后析出深蓝色晶体,写出生成深蓝色透明溶液的离子方程式___ 。
(5)H2O与CH3CH2OH可以任意比例互溶,原因是____ 、____ (回答两点)。
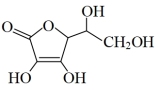
(6)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为____ ,分子中有____ 个手性碳原子。
(1)对具有下列价电子排布的Ni或As进行光谱实验,用光谱仪一定能摄取到原子发射光谱的是
| A.Ni:3d10 | B.As:4s24p 4p 4p 4p 4p |
C.As: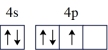 | D.Ni: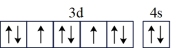 |
(3)羟基磷灰石[Ca(PO4)3OH]是牙齿中的重要矿物质,其中羟基(—OH)中氧原子的杂化方式为
 的空间构型为
的空间构型为(4)向胆矾溶液中滴加氨水至过量,最终得到深蓝色的透明溶液,再加入乙醇后析出深蓝色晶体,写出生成深蓝色透明溶液的离子方程式
(5)H2O与CH3CH2OH可以任意比例互溶,原因是
(6)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

更新时间:2022-05-25 15:30:29
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】镍铜合金是由60%镍、339%铜、7%铁三种金属组成的合金材料。镍铜合金有较好的室温力学性能和高温强度,耐蚀性强,耐磨性好,容易加工,可作为航空发动机的结构材料。根据所学知识,回答下列问题:
(1)铜元素的焰色试验呈绿色,下列三种波长为橙、黄、绿色对应的波长,则绿色对应的辐射波长为___________ (填标号)。
A.577~492nm B.597~577nm C.622~597nm
(2)基态 的价电子排布式为
的价电子排布式为___________ 。
(3)乙酰丙酮中 键与
键与 键数目之比为
键数目之比为___________ 。

(4)Cu与Fe的第二电离能分别为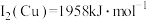 ,
,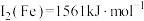 ,
, 大于
大于 的主要原因是
的主要原因是___________ 。
(5)已知 的立方晶胞结构如图所示。
的立方晶胞结构如图所示。

①已知a、b的坐标参数依次为(0,0,0)、 ,则d的坐标参数为
,则d的坐标参数为___________ 。
②晶胞边长为c pm,该晶体的密度为___________  ,(列计算式,设
,(列计算式,设 为阿伏加德罗常数的数值)
为阿伏加德罗常数的数值)
(1)铜元素的焰色试验呈绿色,下列三种波长为橙、黄、绿色对应的波长,则绿色对应的辐射波长为
A.577~492nm B.597~577nm C.622~597nm
(2)基态
 的价电子排布式为
的价电子排布式为(3)乙酰丙酮中
 键与
键与 键数目之比为
键数目之比为
(4)Cu与Fe的第二电离能分别为
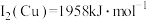 ,
,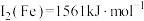 ,
, 大于
大于 的主要原因是
的主要原因是(5)已知
 的立方晶胞结构如图所示。
的立方晶胞结构如图所示。
①已知a、b的坐标参数依次为(0,0,0)、
 ,则d的坐标参数为
,则d的坐标参数为②晶胞边长为c pm,该晶体的密度为
 ,(列计算式,设
,(列计算式,设 为阿伏加德罗常数的数值)
为阿伏加德罗常数的数值)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】锗石是自然界中含有锗元素的一类矿石的统称;锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。回答下列问题:
(1)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠: ;二锗酸钠:
;二锗酸钠: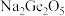 等),也能形成类似于烷烃的锗烷
等),也能形成类似于烷烃的锗烷 。
。
① 中锗原子的杂化方式是
中锗原子的杂化方式是___________ ,外围电子排布式为___________ 。
②碳元素形成的最简单有机物的等电子体是___________ 。
③至今没有发现n大于5的锗烷,根据下表提供的数据分析其中的原因___________ 。
(2)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图所示。___________ 。
(3)硒化锌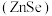 是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是
是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是___________ ;已知晶胞边长为a pm,乙图为甲图的俯视图,若原子坐标A为(0,0,0),B为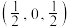 则D原子坐标为
则D原子坐标为___________ 。
(1)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:
 ;二锗酸钠:
;二锗酸钠: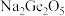 等),也能形成类似于烷烃的锗烷
等),也能形成类似于烷烃的锗烷 。
。①
 中锗原子的杂化方式是
中锗原子的杂化方式是②碳元素形成的最简单有机物的等电子体是
③至今没有发现n大于5的锗烷,根据下表提供的数据分析其中的原因
| 化学键 |  |  |  |  |
键能/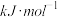 |  |  |  |  |
(2)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图所示。

(3)硒化锌
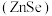 是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是
是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是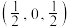 则D原子坐标为
则D原子坐标为
您最近一年使用:0次
【推荐3】第IIB族元素(Zn、Cd、Hg)和第VIA族元素(S、Se、Te)组成的某些二元化合物常用作半导体材料,应用十分广泛。
(1)基态Se原子价电子排布式为____ ,有____ 个未成对电子。
(2)碲酸(H6TeO6)是白色固体,经X射线研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为____ 。
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:
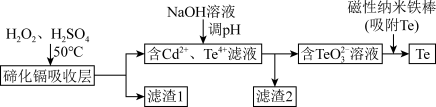
①碲化镉吸收层中的CdTe参与反应的化学方程式为____ ,滤渣1含有的一种单质是____ 。
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=____ 。(已知Ksp[Cd(OH)2]=5.3×10-15)。
(1)基态Se原子价电子排布式为
(2)碲酸(H6TeO6)是白色固体,经X射线研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:

①碲化镉吸收层中的CdTe参与反应的化学方程式为
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、Q、E 五种元素中,X 原子核外的 M 层中只有两对成对电子,Y 原子核外的 L 层电子数是 K 层的两倍,Z 是地壳内含量(质量分数)最高的元素,Q 的核电荷数是X 与 Z 的核电荷数之和,E 在元素周期表的各元素中电负性最大。请回答下列问题:
(1)Y的元素符号为___________ ;
(2)XZ2与YZ2分子的立体结构分别是___________ 和___________ ,相同条件下两者在水中的溶解度较大的是___________ (写分子式),理由是___________ ;
(3)Q元素在元素周期表中属于___________ 区,在形成化合物时它的最高化合价为___________ ;
(4)用氢键表示式写出E的氢化物水溶液中存在的所有氢键___________ 。
(1)Y的元素符号为
(2)XZ2与YZ2分子的立体结构分别是
(3)Q元素在元素周期表中属于
(4)用氢键表示式写出E的氢化物水溶液中存在的所有氢键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】过渡元素铜的配合物在物质制备、尖端技术、医药科学、催化反应、材料化学等领域有着广泛的应用。请回答下列问题:
(1)科学家推测胆矾(CuSO4•5H2O)的结构示意图可简单表示如图:
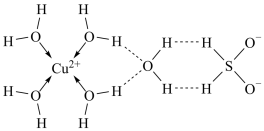
用配合物的形式表示胆矾的化学式为_____ ;SO 的空间结构为
的空间结构为____ ,其中硫原子的杂化轨道类型为____ 。
(2)Cu能与(SCN)2反应生成Cu(SCN)2。1mol(SCN)2中含有的π键数目为____ (设NA为阿伏加德罗常数的值)。
(3)向硫酸铜溶液中加入NaCl固体,溶液由蓝色变为黄绿色,则溶液中铜元素的主要存在形式是_____ (写微粒符号);向上述溶液中滴加浓氨水,先有蓝色沉淀生成,继续滴加浓氨水后,沉淀溶解,溶液变为深蓝色。沉淀溶解的原因是_____ (用离子方程式表示)。
(4)Cu单独与氨水、过氧化氢都不反应,但能与氨水和过氧化氢的混合溶液反应,反应的离子方程式为____ 。
(1)科学家推测胆矾(CuSO4•5H2O)的结构示意图可简单表示如图:

用配合物的形式表示胆矾的化学式为
 的空间结构为
的空间结构为(2)Cu能与(SCN)2反应生成Cu(SCN)2。1mol(SCN)2中含有的π键数目为
(3)向硫酸铜溶液中加入NaCl固体,溶液由蓝色变为黄绿色,则溶液中铜元素的主要存在形式是
(4)Cu单独与氨水、过氧化氢都不反应,但能与氨水和过氧化氢的混合溶液反应,反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】钛(Ti)及其化合物的应用研究是目前前沿科学之一,请回答下列问题:
(1)基态钛原子的电子排布式为_______ 。
(2) 作光催化剂可将甲醛、苯等有害气体转化为
作光催化剂可将甲醛、苯等有害气体转化为 和
和 。上述含碳原子的分子中,碳原子的杂化方式为
。上述含碳原子的分子中,碳原子的杂化方式为 的是
的是_______ (填名称)。
(3)作为过渡元素的Fe、Cu容易形成配位化合物,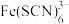 中C、N两种元素的电负性大小关系为
中C、N两种元素的电负性大小关系为_______ 。硫酸铜稀溶液中微粒间不存在的作用力有_______ (填序号)。
A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(4)已知Ba、Mo的氯化物沸点信息如下表所示。二者沸点差异的原因是_______ 。
(5) 分子中H-N-H的键角为107°,在
分子中H-N-H的键角为107°,在 中,H-N-H键角近似109.5°,键角变大的原因是
中,H-N-H键角近似109.5°,键角变大的原因是_______ 。
(6)贵金属磷化物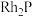 (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为
(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为_______ ,晶体的密度为_______  。(列出计算式即可)。
。(列出计算式即可)。

(1)基态钛原子的电子排布式为
(2)
 作光催化剂可将甲醛、苯等有害气体转化为
作光催化剂可将甲醛、苯等有害气体转化为 和
和 。上述含碳原子的分子中,碳原子的杂化方式为
。上述含碳原子的分子中,碳原子的杂化方式为 的是
的是(3)作为过渡元素的Fe、Cu容易形成配位化合物,
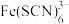 中C、N两种元素的电负性大小关系为
中C、N两种元素的电负性大小关系为A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(4)已知Ba、Mo的氯化物沸点信息如下表所示。二者沸点差异的原因是
| 氯化物 | 沸点 |
 | 1560℃ |
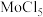 | 268℃ |
(5)
 分子中H-N-H的键角为107°,在
分子中H-N-H的键角为107°,在 中,H-N-H键角近似109.5°,键角变大的原因是
中,H-N-H键角近似109.5°,键角变大的原因是(6)贵金属磷化物
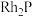 (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为
(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为 。(列出计算式即可)。
。(列出计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铁、铝、铜、钠等金属单质及其化合物具有广泛的用途。
(1)钴位于元素周期表中第____ 族,Cu在元素周期表中属于______ (选填“s”、“p”、“d”或“ds”)区元素,基态Cu的核外电子排布式是_________ 。元素铁与铜的第二电离能分别为:ICu=1958kJ/mol、IFe=1561kJ/mol,ICu>IFe的原因是______________ 。
(2)有机铁肥三硝酸六尿素(H2NCONH2)合铁(Ⅲ),化学式为:[Fe(H2NCONH2)6](NO3)3.
①尿素分子中C原子的杂化方式是_______ 。
②根据价层电子对互斥理论推测 的空间构型为
的空间构型为_________ 。
(3)已知 的结构为
的结构为 ,其中S原子的杂化方式是
,其中S原子的杂化方式是______ 。根据对角线规则,金属Be与铝单质及化合物性质相似,试写出Be与氢氧化钠溶液反应的离子反应方程式__________________
(4)Cu2Cl2•2CO•2H2O是一种配合物,其结构如图所示:

①该配合物中氯原子的杂化方式为_________________________ 。
②该配合物中,CO作配体时配位原子是C而不是O的原因是______________________ 。
③1molCu2Cl2•2CO•2H2O含有的______________ 个σ键。
(5)某种铀氮化物的晶体结构是NaCl型。NaCl的Bom-Haber循环如图所示。已知:元素的一个气态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是__ (填标号)。

a、Cl-Cl键的键能为119.6kJ/mol
b、Na的第一电离能为603.4kJ/mol
c、Cl的第一电子亲和能为348.3kJ/mol
(1)钴位于元素周期表中第
(2)有机铁肥三硝酸六尿素(H2NCONH2)合铁(Ⅲ),化学式为:[Fe(H2NCONH2)6](NO3)3.
①尿素分子中C原子的杂化方式是
②根据价层电子对互斥理论推测
 的空间构型为
的空间构型为(3)已知
 的结构为
的结构为 ,其中S原子的杂化方式是
,其中S原子的杂化方式是(4)Cu2Cl2•2CO•2H2O是一种配合物,其结构如图所示:

①该配合物中氯原子的杂化方式为
②该配合物中,CO作配体时配位原子是C而不是O的原因是
③1molCu2Cl2•2CO•2H2O含有的
(5)某种铀氮化物的晶体结构是NaCl型。NaCl的Bom-Haber循环如图所示。已知:元素的一个气态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是

a、Cl-Cl键的键能为119.6kJ/mol
b、Na的第一电离能为603.4kJ/mol
c、Cl的第一电子亲和能为348.3kJ/mol
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】“氢经济”是当前热门话题,而“高密度安全储氢材料”是制约整个氢能供应链的瓶颈。
(1)氨硼烷是一种有效、安全的固体储氢材料,它是乙烷的等电子体。加热氨硼烷会缓慢释放H2,转变为化合物X,X是乙烯的等电子体。
①氨硼烷的结构式为_______ (必须标明配位键)。
②氮和硼比较,电负性大的元素为_______ (填元素符号)。
③氨硼烷和X分子中硼原子的杂化轨道类型分别为_______ 和_______ 。
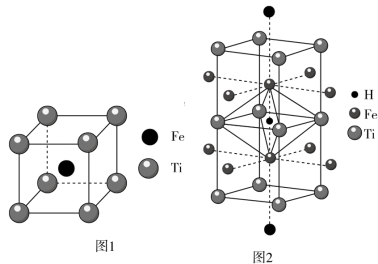
(2)钛铁基储氢合金是由钛、铁两种元素组成的金属间化合物。一种钛铁合金的晶胞如图1所示,晶胞边长为300pm(a=b=c),该合金吸收的氢位于体心立方正八面体的中心,氢被4个钛原子和2个铁原子包围,如图2所示。
①基态钛原子的电子排布式为_______ 。
②钛铁合金的熔点比Ti_______ (填“高”或者“低”)。
③若图2所示的每个体心立方的正八面体空隙均填充1个氢原子,则填充的氢原子位于图1晶胞的_______ ,假设吸收氢后不引起晶胞参数变化,则理论上形成的金属氢化物的密度为_______ g·cm-3(列出计算表达式即可,用NA表示阿伏加德罗常数)。
(1)氨硼烷是一种有效、安全的固体储氢材料,它是乙烷的等电子体。加热氨硼烷会缓慢释放H2,转变为化合物X,X是乙烯的等电子体。
①氨硼烷的结构式为
②氮和硼比较,电负性大的元素为
③氨硼烷和X分子中硼原子的杂化轨道类型分别为
(2)钛铁基储氢合金是由钛、铁两种元素组成的金属间化合物。一种钛铁合金的晶胞如图1所示,晶胞边长为300pm(a=b=c),该合金吸收的氢位于体心立方正八面体的中心,氢被4个钛原子和2个铁原子包围,如图2所示。

①基态钛原子的电子排布式为
②钛铁合金的熔点比Ti
③若图2所示的每个体心立方的正八面体空隙均填充1个氢原子,则填充的氢原子位于图1晶胞的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
【查阅资料】经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。
【设计方案】学习小组设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
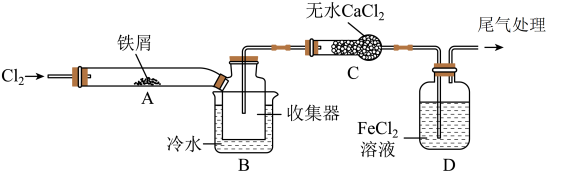
①检验装置的气密性;②通入干燥的Cl2,赶尽装置中的空气;③用酒精灯在铁屑下方加热至反应完成;④……;⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)Fe元素的原子结构示意图为______________ 。FeCl3是___________ 化合物(填“离子”或“共价”)。
(2)装置A中反应的化学方程式为______________ 。
(3)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是____________ 。
(4)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)____________ 。
(5)装置B中冷水浴的作用为____________ ;装置C的名称为____________ ;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂K3[Fe(CN)6]是配位化合物,其配位数为___________ ,配体为__________ 。
(6)该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;FeCl3与H2S反应的离子方程式为________________ 。
【查阅资料】经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。
【设计方案】学习小组设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:

①检验装置的气密性;②通入干燥的Cl2,赶尽装置中的空气;③用酒精灯在铁屑下方加热至反应完成;④……;⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)Fe元素的原子结构示意图为
(2)装置A中反应的化学方程式为
(3)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是
(4)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)
(5)装置B中冷水浴的作用为
(6)该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;FeCl3与H2S反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】有些食物中铁元素含量非常丰富,其中非血红素铁是其存在形式之一,主要是三价铁与蛋白质和羧酸结合成络合物。
(1)Fe3+的电子排布式为______ 。
(2)配合物Fe(CO)5的配位体是___ ;常温下,Fe(CO)5为黄色液体,易溶于非极性溶剂,熔点为251 K,沸点为376K,据此,可判断Fe(CO)5晶体属于____ 晶体(填“离子”、“原子”、“分子”或“金属”)。
(3)金属晶体可看成金属原子在三维空间中堆积而成,单质铁中铁原子采用钾型模式堆积,原子空间利用率为68%,铁原子的配位数为____ 。
(4)乙醛能被氧化剂氧化为乙酸,乙醛中碳原子的轨道杂化类型是____ ;1 mol乙醛分子中含有的σ键的数目为____ 。
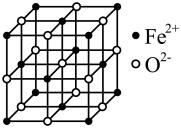
(5)FeO晶体结构如图所示,FeO晶体中Fe2+的配位数为___ 。若该晶胞边长为bcm,则该晶体的密度为___ g·cm-3。
(1)Fe3+的电子排布式为
(2)配合物Fe(CO)5的配位体是
(3)金属晶体可看成金属原子在三维空间中堆积而成,单质铁中铁原子采用钾型模式堆积,原子空间利用率为68%,铁原子的配位数为
(4)乙醛能被氧化剂氧化为乙酸,乙醛中碳原子的轨道杂化类型是
(5)FeO晶体结构如图所示,FeO晶体中Fe2+的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
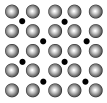
【推荐3】(1)诺贝尔化学奖获得者Gerhard Ertl利用光电子能谱证实:洁净铁(可用于合成氨反应的催化剂)的表面上存在氮原子,图为氮原子在铁的晶面上的单层附着局部示意图(图中小的黑色球代表氮原子,大的灰色球代表铁原子)。则在图示状况下,铁颗粒表面上N/Fe原子数比值的最大值为________________ 。
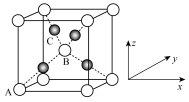
(2)Cu与O形成的某种化合物X,其晶胞结构如下图所示。O在顶点和体心。已知X晶胞中原子坐标参数:A为(0,0,0),B为( ,
, ,
, ),则C原子的坐标参数为
),则C原子的坐标参数为___________ 。
物质结构用到多种模型,请结合模型完成下列问题:
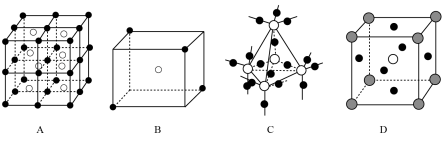
(3)D图是CaTiO3晶胞模型,同一种微粒位置相同,Ca2+位于立方体的体心,则Ti4+位于____ (填顶点或面心)
(4)已知A图是CsCl晶胞模型,体心为Cs+,与其紧邻等距离的Cs+数目有___________ 个。
(5)某分子中原子空间位置关系如B图所示,X位于立方体的顶点,Y位于立方体中心,用X,Y表示的化学式为______________ 。
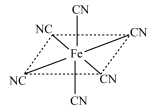
(6)铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其阴离子结构如图。写出上述沉淀溶解过程的离子方程式为___________________ 。

(2)Cu与O形成的某种化合物X,其晶胞结构如下图所示。O在顶点和体心。已知X晶胞中原子坐标参数:A为(0,0,0),B为(
 ,
, ,
, ),则C原子的坐标参数为
),则C原子的坐标参数为
物质结构用到多种模型,请结合模型完成下列问题:

(3)D图是CaTiO3晶胞模型,同一种微粒位置相同,Ca2+位于立方体的体心,则Ti4+位于
(4)已知A图是CsCl晶胞模型,体心为Cs+,与其紧邻等距离的Cs+数目有
(5)某分子中原子空间位置关系如B图所示,X位于立方体的顶点,Y位于立方体中心,用X,Y表示的化学式为
(6)铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其阴离子结构如图。写出上述沉淀溶解过程的离子方程式为

您最近一年使用:0次

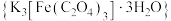 是制备铁触媒上的主要原料。在光照下分解:
是制备铁触媒上的主要原料。在光照下分解: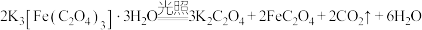 。回答下列问题:
。回答下列问题: 原子的电子排布式为
原子的电子排布式为 与
与 中未成对电子的数目之比为
中未成对电子的数目之比为 键数目之比为
键数目之比为

