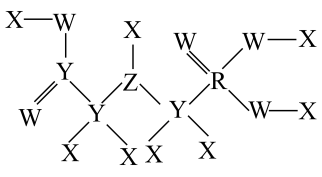
我国科学家意外发现一种罕见无机化合物 (结构如图所示),其中W、X、Y为同一短周期元素,X、Z为短周期同一主族元素且Z的核电荷数是X的2倍,下列说法正确的是
(结构如图所示),其中W、X、Y为同一短周期元素,X、Z为短周期同一主族元素且Z的核电荷数是X的2倍,下列说法正确的是
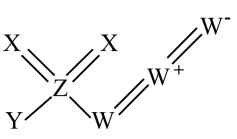
 (结构如图所示),其中W、X、Y为同一短周期元素,X、Z为短周期同一主族元素且Z的核电荷数是X的2倍,下列说法正确的是
(结构如图所示),其中W、X、Y为同一短周期元素,X、Z为短周期同一主族元素且Z的核电荷数是X的2倍,下列说法正确的是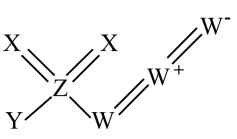
| A.原子半径的大小顺序为Z>Y>K>W |
| B.NaY的水溶液能存放在玻璃试剂瓶中 |
| C.该物质中存在共价键和离子键 |
| D.Z的氧化物的水化物不一定是强酸 |
更新时间:2022-07-06 11:48:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,下列说法正确的是
| A.分别取20.00mL0.1000mol/L的盐酸和醋酸溶液,以酚酞作指示剂,用0.1000mol/LNaOH标准溶液滴定至终点时,两者消耗的NaOH溶液体积相等 |
| B.将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| C.均为0.1mol/L的Na2SO3、Na2CO3、H2SO4溶液中阴离子的浓度依次减小 |
| D.常温下pH=11的碱溶液中水电离产生的c(H+)是纯水电离产生的c(H+)的104倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某化合物的结构为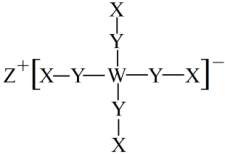 ,其中X、Y、Z、W四种元素分布在三个短周期,原子序数依次增大,且Y、Z、W的简单离子具有相同的电子层结构。下列叙述正确的是
,其中X、Y、Z、W四种元素分布在三个短周期,原子序数依次增大,且Y、Z、W的简单离子具有相同的电子层结构。下列叙述正确的是
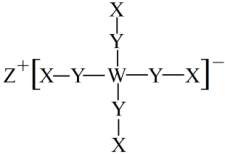 ,其中X、Y、Z、W四种元素分布在三个短周期,原子序数依次增大,且Y、Z、W的简单离子具有相同的电子层结构。下列叙述正确的是
,其中X、Y、Z、W四种元素分布在三个短周期,原子序数依次增大,且Y、Z、W的简单离子具有相同的电子层结构。下列叙述正确的是| A.简单离子半径:W>Z>Y | B.Z的氯化物可促进水的电离 |
| C.最高价氧化物对应水化物的碱性:Z<W | D.ZX和Z2Y所含化学键类型完全相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列相关比较中,正确的是
| A.分解温度:MgCO3>CaCO3> BaCO3 | B.熔点:Na>Mg>Al |
| C.微粒半径:r(Cl-)>r(O2-)>r(Na+) | D.热稳定性:H2O>H2S> HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W为原子序数依次增大的短周期主族元素,X原子核外电子总数与Y原子次外层的电子数相同;Z所在的周期数与族序数相同,W与X同族。下列说法不正确 的是
| A.简单离子的半径:W>X>Y>Z | B.4种元素中Y的金属性最强 |
| C.Z元素对应的盐溶液一定显酸性 | D.W单质的氧化性比X单质的氧化性弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a,c和d的气态氢化物的稳定性c>d,五种元素的原子得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是( )
| A.b、a、e、d、c | B.e、d、a、b、c |
| C.a、b、d、c、e | D.c、d、e、a、b |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、D、E、G、M六种元素位于元素周期表前四周期,原子序数依次增大。其中,元素A的一种核素无中子,B的单质既有分子晶体又有原子晶体,化合物DE2为红棕色气体,G是前四周期中电负性最小的元素,M的原子核外电子数比G多10。
请回答下列问题:
(1)基态G原子的核外电子排布式是_______ ,M在元素周期表中的位置是_______ ,元素B、D、E的第一电离能由大到小的顺序为_______ (用元素符号表示)。
(2)元素A和E组成的阳离子空间构型为_______ ;化合物ABD的结构式为_______ ,其中B原子的杂化方式为_______ 。
(3)D的最高价氧化物对应的水化物甲与气体DA3化合生成离子化合物乙,常温下,若甲、乙两溶液的pH均等于5,则由水电离出的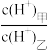 =
=__ ;乙溶液中所含离子的物质的量浓度由大到小的顺序是__ 。
(4)元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子。
①X与Y所形成化合物中X的化合价等于其族序数,Y达到8电子的稳定结构则该化合物的化学式为_______ ;
②E的氢化物(H2E)在乙醇中的溶解度大于H2Y,其原因是_______ 。
③X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为_______ 。
请回答下列问题:
(1)基态G原子的核外电子排布式是
(2)元素A和E组成的阳离子空间构型为
(3)D的最高价氧化物对应的水化物甲与气体DA3化合生成离子化合物乙,常温下,若甲、乙两溶液的pH均等于5,则由水电离出的
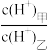 =
=(4)元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子。
①X与Y所形成化合物中X的化合价等于其族序数,Y达到8电子的稳定结构则该化合物的化学式为
②E的氢化物(H2E)在乙醇中的溶解度大于H2Y,其原因是
③X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
您最近一年使用:0次

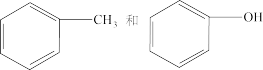
 。下列说法错误的是
。下列说法错误的是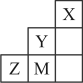
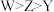

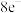 的稳定结构
的稳定结构

