一定条件下用甲烷可以消除氮氧化物(NOx)的污染。
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
下列选项正确的是
已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
下列选项正确的是
| A.CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ΔH=-867 kJ·mol-1 |
| B.若把反应①设计为燃料电池,在碱性条件下负极的电极反应式为:CH4-8e-+8OH-=CO2+6H2O |
| C.反应①在任何温度下都能自发进行 |
| D.在其他条件不变的情况下,增大压强有利于提高氮氧化物的消除率 |
更新时间:2022-04-06 09:05:08
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】为消除NO对环境的污染,可利用NH3在一定条件下与NO反应生成无污染的气体。
已知:① ∆H=+180.50kJ·mol-1
∆H=+180.50kJ·mol-1
②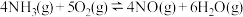 ∆H=-905.48kJ·mol-1
∆H=-905.48kJ·mol-1
则反应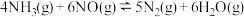 的∆H为
的∆H为
已知:①
 ∆H=+180.50kJ·mol-1
∆H=+180.50kJ·mol-1②
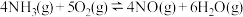 ∆H=-905.48kJ·mol-1
∆H=-905.48kJ·mol-1则反应
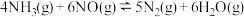 的∆H为
的∆H为| A.+2.98kJ·mol-1 | B.-2.98kJ·mol-1 |
| C.+1807.98kJmol-1 | D.-1807.98kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】CO2催化重整CH4的反应:(Ⅰ)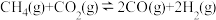 △H1,主要副反应:(Ⅱ)
△H1,主要副反应:(Ⅱ) 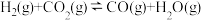 △H2>0,(Ⅲ)
△H2>0,(Ⅲ)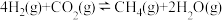 △H3<0。在恒容反应器中CH4和CO2按物质的量之比1:1充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法错误的是
△H3<0。在恒容反应器中CH4和CO2按物质的量之比1:1充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法错误的是

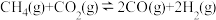 △H1,主要副反应:(Ⅱ)
△H1,主要副反应:(Ⅱ) 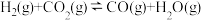 △H2>0,(Ⅲ)
△H2>0,(Ⅲ)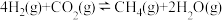 △H3<0。在恒容反应器中CH4和CO2按物质的量之比1:1充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法错误的是
△H3<0。在恒容反应器中CH4和CO2按物质的量之比1:1充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法错误的是
| A.△H1>0 |
| B.若反应Ⅰ、Ⅲ消耗等量的CO2时,转移电子数之比为3:4 |
| C.300~580℃时,H2O的体积分数不断增大,是由于反应(Ⅲ)生成H2O的量大于反应(Ⅱ)消耗的量 |
| D.T℃时,在2.0L容器中加入1molCH4、1molCO2以及催化剂进行重整反应,测得CO2的平衡转化率为50%,则反应(I)的平衡常数小于1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在密闭容器中发生如下反应:mA(g)+nB(g) pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法正确的是( )
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法正确的是( )
 pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法正确的是( )
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法正确的是( )| A.m+n>p | B.平衡向正反应方向移动 |
| C.A的转化率降低 | D.C的体积分数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室模拟工业处理含铬废水,操作及现象如图1所示,反应过程中铬元素的化合价变化如图2,已知:深蓝色溶液中生成了 ,下列说法
,下列说法不正确 的是
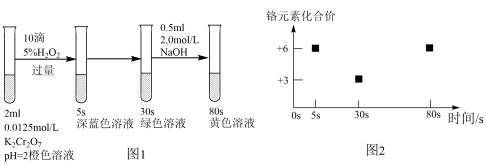
 ,下列说法
,下列说法
A. 过程中, 过程中, 没有发生氧化还原反应 没有发生氧化还原反应 |
B.实验开始至30s,溶液中发生的总反应离子方程式为: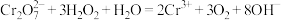 |
C.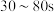 过程中,Cr元素被氧化,可能是溶液中剩余 过程中,Cr元素被氧化,可能是溶液中剩余 的所致 的所致 |
D.80s时,在碱性条件下,溶液中含铬微粒主要为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.已知 则 则 反应的反应热 反应的反应热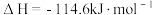 |
| B.能自发进行的化学反应,不一定是ΔH<0,Δ S>0 |
C.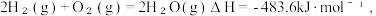 则H₂的燃烧热为 则H₂的燃烧热为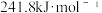 |
| D.用NaOH标准溶液滴定未知浓度的醋酸,可选用甲基橙或酚酞做指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】自由能的变化综合反映了焓变和熵变对自发过程的影响。下列说法正确的是
| A.乙烯聚合为聚乙烯的反应是熵减的过程 |
| B.凡是放热反应都是自发的,凡是吸热反应都是非自发的 |
| C.常温常压下,△H>0且△S<0的反应一定能自发进行 |
| D.对于同一种物质,气态时熵值最小,固态时熵值最大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】利用小粒径零价铁(ZVI)的电化学腐蚀处理三氯乙烯进行水体修复,修复过程如图所示。H+、O2、 等共存物的存在会影响水体修复效果。下列说法错误的是
等共存物的存在会影响水体修复效果。下列说法错误的是

 等共存物的存在会影响水体修复效果。下列说法错误的是
等共存物的存在会影响水体修复效果。下列说法错误的是
| A.反应①在负极发生,反应②③④⑤在正极发生 |
| B.增大单位体积水体中小粒径ZVI的投入量,可加快水体修复速率 |
| C.水体修复过程中,三氯乙烯每脱去3mol Cl,就有3molFe变成Fe2+ |
D.⑤的电极反应式为 + 10H++8e-== + 10H++8e-== +3H2O +3H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一种新型微生物脱盐燃料电池如图所示。利用活性菌的催化作用,在净化两极室污水的同时,淡化脱盐室的盐水,协同产生电流。下列说法错误的是
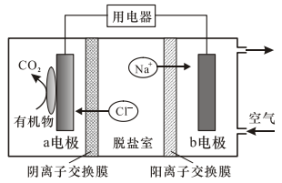

A. 电极为电池负极 电极为电池负极 |
B. 电极的电极反应可能为: 电极的电极反应可能为: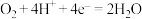 |
C.污水净化过程中, 电极区溶液的pH一定增大 电极区溶液的pH一定增大 |
| D.外电路转移2mol电子,脱盐室质量减少58.5g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】“绿水青山就是金山银山”很好地诠释了我国当前对环境保护的认识。某微生物燃料电池可很好的解决当前河流中的有机废水问题。某污染的河水中含有大量的葡萄糖,通过下面的微生物电池进行处理可达到净水的初级目标。下列有关说法错误的是
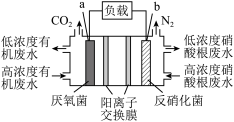

| A.a极是负极 |
| B.b极的电极反应式为:2NO3-+6H2O+10e-=N2+12OH- |
| C.右室溶液中的氢氧根可以进入左室,使左室溶液的pH增大 |
| D.电池工作时,外电路中流过2.4mol电子时,产生标准状况下13.44LCO2 |
您最近一年使用:0次

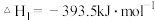 ,
,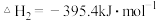 下列说法或表示式正确的是
下列说法或表示式正确的是 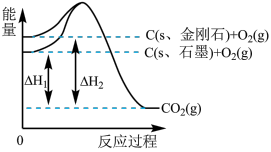
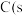 ,石墨
,石墨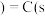 ,金刚石
,金刚石 ,该反应的焓变为负值
,该反应的焓变为负值 石墨的总键能比
石墨的总键能比


