一定温度下,向密闭容器中分别加入足量活性炭和 ,发生反应:
,发生反应: ,在相同时间内测得各容器中
,在相同时间内测得各容器中 的转化率与容器体积的关系如图所示 (
的转化率与容器体积的关系如图所示 (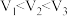 )。下列说法正确的是
)。下列说法正确的是
 ,发生反应:
,发生反应: ,在相同时间内测得各容器中
,在相同时间内测得各容器中 的转化率与容器体积的关系如图所示 (
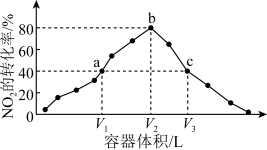
的转化率与容器体积的关系如图所示 (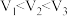 )。下列说法正确的是
)。下列说法正确的是
| A.bc曲线上反应均达到平衡状态 |
B.容器内的压强: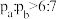 |
| C.a、c两点时气体的颜色相同 |
D.该温度下,a、b、c三点时反应的平衡常数: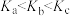 |
22-23高三上·广东·阶段练习 查看更多[7]
黑龙江省鹤岗市第一中学2022-2023学年高三上学期11月月考化学试题广东省深圳市新安中学2022-2023学年高三上学期周末测试(2022.9.18)化学试题(已下线)2022年北京高考真题化学试题变式题(选择题11-14)陕西省咸阳市武功县2022-2023学年高二上学期期中考试化学试题河南省中原名校2022-2023学年高二上学期第二次联考化学试题(已下线)2022年北京高考真题变式题1-14广东省清中、河中、北中、惠中2023届高三上学期8月联合考试化学试题
更新时间:2022-08-27 18:32:19
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在2L恒容密闭容器中,发生反应:2SO2(g)+O2(g) 2SO3(g) ΔH=-198kJ/mol。起始通入2molSO2和1molO2,5min后达到平衡,测得SO3的体积分数为40%。下列说法正确的是
2SO3(g) ΔH=-198kJ/mol。起始通入2molSO2和1molO2,5min后达到平衡,测得SO3的体积分数为40%。下列说法正确的是
 2SO3(g) ΔH=-198kJ/mol。起始通入2molSO2和1molO2,5min后达到平衡,测得SO3的体积分数为40%。下列说法正确的是
2SO3(g) ΔH=-198kJ/mol。起始通入2molSO2和1molO2,5min后达到平衡,测得SO3的体积分数为40%。下列说法正确的是| A.5min内,SO2的平均反应速率为0.1mol/(L·s) |
| B.平衡后再升高温度,则平衡向逆反应方向移动,正反应速率减小 |
| C.5min时,SO2的转化率为25% |
| D.如果充入4molSO2和2molO2,相同条件下达到平衡,反应放出的热量大于198kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g) + 3H2(g)  2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是
 2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
| A.放出热量关系:a < b <92.4 |
| B.三个容器内反应的平衡常数:③>①>② |
| C.达平衡时氨气的体积分数:①>③ |
| D.N2的转化率:②>①>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】接触法制备硫酸中的关键步骤是: 在
在 催化作用下与空气中
催化作用下与空气中 在接触室发生可逆反应,其热化学方程式为:
在接触室发生可逆反应,其热化学方程式为: 。题图表示在有、无催化剂条件下
。题图表示在有、无催化剂条件下 氧化成
氧化成 过程中的能量变化。
过程中的能量变化。 催化时,该反应机理为:
催化时,该反应机理为:
反应①:
反应②:
下列说法正确的是

 在
在 催化作用下与空气中
催化作用下与空气中 在接触室发生可逆反应,其热化学方程式为:
在接触室发生可逆反应,其热化学方程式为: 。题图表示在有、无催化剂条件下
。题图表示在有、无催化剂条件下 氧化成
氧化成 过程中的能量变化。
过程中的能量变化。 催化时,该反应机理为:
催化时,该反应机理为:反应①:

反应②:

下列说法正确的是

A. 催化时,反应②的速率大于反应① 催化时,反应②的速率大于反应① |
B. |
| C.升高温度,正反应速率增大,逆反应速率减小 |
D.增大压强,反应 平衡常数增大 平衡常数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知某化学反应的平衡常数表达式为K= ,在不同的温度下该反应的平衡常数如表所示:
,在不同的温度下该反应的平衡常数如表所示:
下列有关叙述不正确的是
 ,在不同的温度下该反应的平衡常数如表所示:
,在不同的温度下该反应的平衡常数如表所示:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
| A.该反应的化学方程式是:CO(g)+H2O(g)⇌CO2(g)+H2(g) |
| B.上述反应的正反应是放热反应 |
C.若平衡浓度符合下列关系式: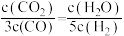 ,则此时的温度是为1000℃ ,则此时的温度是为1000℃ |
| D.在1L的密闭容器中通入CO2和H2各1mol,5min后温度升高到830℃,此时测得CO2为0.4 mol时,则该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
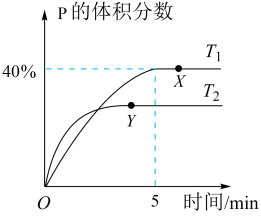
【推荐1】将1 mol M和2 mol N置于体积为2 L的恒容密闭容器中,发生反应:M(s)+2N(g) P(g)+Q(g)ΔH 。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
P(g)+Q(g)ΔH 。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
 P(g)+Q(g)ΔH 。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
P(g)+Q(g)ΔH 。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
| A.若X、Y两点的平衡常数分别为K1、K2,则K1<K2 |
| B.温度为T1时,N的平衡转化率为80%,平衡常数K=4 |
| C.无论温度为T1还是T2,当容器中气体密度或压强不变时,反应达平衡状态 |
| D.降低温度、增大压强、及时分离出产物均有利于提高反应物的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将等物质的量的 X、Y 气体充入某密闭容器中,在一定条件下,发生反应并达到平衡:X(g)+3Y(g) ⇌ 2Z(g) ΔH<0,当改变某个条件并维持新条件直至新的平衡时,表中关于新平衡与原平衡的比较正确的是
| 选项 | 改变条件 | 新平衡与原平衡比较 |
| A | 升高温度 | X的转化率变小 |
| B | 增大压强(减小容器容积) | X的转化率变小 |
| C | 充入一定量Y | Y的转化率增大 |
| D | 使用适当催化剂 | Y的转化率增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,向三个容积不等的恒容密闭容器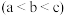 中分别投入
中分别投入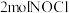 ,发生反应:
,发生反应: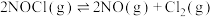 。
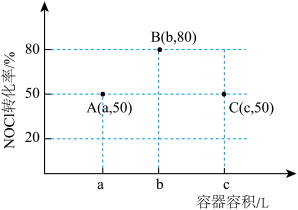
。 后,三个容器中
后,三个容器中 的转化率如图中A、B、C三点。下列叙述正确的是
的转化率如图中A、B、C三点。下列叙述正确的是
 中分别投入
中分别投入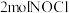 ,发生反应:
,发生反应: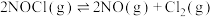 。
。 后,三个容器中
后,三个容器中 的转化率如图中A、B、C三点。下列叙述正确的是
的转化率如图中A、B、C三点。下列叙述正确的是
A.A点延长反应时间,可以提高 的转化率 的转化率 |
| B.A、B两点的压强之比为25∶28 |
| C.容积为cL的容器NOCl的平衡转化率等于80% |
D.容积为aL的容器达到平衡后再投入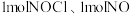 ,平衡不移动 ,平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某反应aA(g)+bB(g) cC(g) ∆H<0,在体积为2L的密闭容器中反应:在I、II、III不同阶段体系中改变某一条件,体系中各物质的量(mol)随时间变化的曲线如图所示。下列说法不正确的是:
cC(g) ∆H<0,在体积为2L的密闭容器中反应:在I、II、III不同阶段体系中改变某一条件,体系中各物质的量(mol)随时间变化的曲线如图所示。下列说法不正确的是:

 cC(g) ∆H<0,在体积为2L的密闭容器中反应:在I、II、III不同阶段体系中改变某一条件,体系中各物质的量(mol)随时间变化的曲线如图所示。下列说法不正确的是:
cC(g) ∆H<0,在体积为2L的密闭容器中反应:在I、II、III不同阶段体系中改变某一条件,体系中各物质的量(mol)随时间变化的曲线如图所示。下列说法不正确的是:
A.该反应的化学反应方程式为:A+3B 2C 2C |
| B.用物质A表示第I阶段20分钟内平均反应速率为:v(A)=0.025mol·L-1·min-1 |
| C.三个阶段反应的平衡常数关系为:KI<KII<KIII |
| D.三个阶段反应的速率为:v(B)I>v(B)II>v(B)III,各段内转化率AI%>AII%>AIII% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2 H2O(g) 2 H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2 H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:

下列说法不正确 的是
 2 H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2 H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
下列说法
| A.实验时的温度T2高于T1 |
| B.2号Cu2O的催化效率比1号Cu2O的催化效率高 |
| C.实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol·Lˉ1·minˉ1 |
| D.等质量纳米级Cu2O比微米级Cu2O催化效率高,这与Cu2O的粒径大小有关 |
您最近一年使用:0次


 (aq),该平衡体系中,I2的物质的量浓度与温度(T)的关系如图所示(曲线上的任何一点都代表平衡状态),下列说法正确的是
(aq),该平衡体系中,I2的物质的量浓度与温度(T)的关系如图所示(曲线上的任何一点都代表平衡状态),下列说法正确的是
 3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:
3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:

