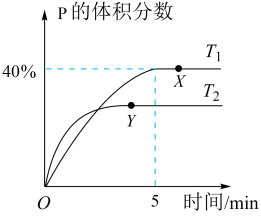
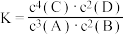将1 mol M和2 mol N置于体积为2 L的恒容密闭容器中,发生反应:M(s)+2N(g) P(g)+Q(g)ΔH 。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
P(g)+Q(g)ΔH 。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
 P(g)+Q(g)ΔH 。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
P(g)+Q(g)ΔH 。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
| A.若X、Y两点的平衡常数分别为K1、K2,则K1<K2 |
| B.温度为T1时,N的平衡转化率为80%,平衡常数K=4 |
| C.无论温度为T1还是T2,当容器中气体密度或压强不变时,反应达平衡状态 |
| D.降低温度、增大压强、及时分离出产物均有利于提高反应物的平衡转化率 |
2020高三·全国·专题练习 查看更多[1]
(已下线)专题讲座(七) 常考速率、平衡图像题解题策略(精练)-2021年高考化学一轮复习讲练测
更新时间:2020-10-30 14:31:13
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】一定条件下,在密闭容器中,进行反应2CO(g)+SO2(g)⇌2CO2(g)+S(s) △H<0,可以同时提高反应速率与CO转化率的措施是
| A.缩小容积增大压强 | B.分离出CO2 |
| C.再充入一定量的CO | D.升高温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】据美国《科学》杂志报道,外太空的某一星球的大气层中,含有大量的CH2=CHOH,该物质常温时为液体,它很容易转化成CH3CHO,化学方程式为CH2=CHOH  CH3CHO ΔH < 0。下列说法中正确的是
CH3CHO ΔH < 0。下列说法中正确的是
 CH3CHO ΔH < 0。下列说法中正确的是
CH3CHO ΔH < 0。下列说法中正确的是| A.该星球表面温度很高 |
| B.该星球表面温度很低 |
| C.低温下稳定性:CH2=CHOH > CH3CHO |
| D.该反应中CH2=CHOH化学键断裂吸收能量大于CH3CHO化学键形成放出能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,在一容积固定的容器中,反应xA(g)+yB(g) zH(g)达到平衡后,A、B、H的物质的量分别为amol、bmol和hmol。已知x+y=2z,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是( )
zH(g)达到平衡后,A、B、H的物质的量分别为amol、bmol和hmol。已知x+y=2z,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是( )
 zH(g)达到平衡后,A、B、H的物质的量分别为amol、bmol和hmol。已知x+y=2z,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是( )
zH(g)达到平衡后,A、B、H的物质的量分别为amol、bmol和hmol。已知x+y=2z,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是( )| A.平衡不移动 | B.混合气体的密度不变 |
| C.B的体积分数减少 | D.amol/L<c(A)<2amol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】关于一定条件下的化学平衡CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH<0,下列说法正确的是
| A.恒温恒压,充入Ar,反应速率不变,CO的体积分数不变 |
| B.恒温恒容,充入H2,v(正)增大,CO2转化率增大 |
| C.加压,v(正),v(逆)不变,平衡不移动 |
| D.升温,v(正)不变,v(逆)增大,平衡左移,CO2转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列选项中的原因或结论与现象不对应的是
| 选项 | 现象 | 原因或结论 |
| A | 在 中加入 中加入 ,能加速 ,能加速 的分解速率 的分解速率 |  降低了反应所需的活化能 降低了反应所需的活化能 |
| B | 将盛有 气体的密闭容器浸泡在热水中,容器内气体颜色变深 气体的密闭容器浸泡在热水中,容器内气体颜色变深 |  ,平衡向生成 ,平衡向生成 方向移动 方向移动 |
| C | 向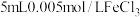 溶液中加入 溶液中加入 溶液,溶液呈红色,再滴加几滴 溶液,溶液呈红色,再滴加几滴 溶液,溶液颜色变浅 溶液,溶液颜色变浅 | 增大生成物浓度,平衡向逆反应方向移动 |
| D | 在密闭容器中有反应: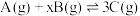 ,达到平衡时测得 ,达到平衡时测得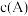 为 为 ,将容器容积扩大到原来的2倍,测得 ,将容器容积扩大到原来的2倍,测得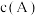 为 为 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】利用反应 △H<0,可减少汽车尾气对大气的污染。该反应的速率方程可表示为
△H<0,可减少汽车尾气对大气的污染。该反应的速率方程可表示为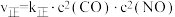 、
、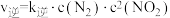 ,其中
,其中 、
、 分别为正、逆反应的速率常数(与温度有关),lgk与
分别为正、逆反应的速率常数(与温度有关),lgk与 的关系如图所示:
的关系如图所示:

下列说法正确的是
 △H<0,可减少汽车尾气对大气的污染。该反应的速率方程可表示为
△H<0,可减少汽车尾气对大气的污染。该反应的速率方程可表示为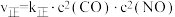 、
、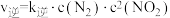 ,其中
,其中 、
、 分别为正、逆反应的速率常数(与温度有关),lgk与
分别为正、逆反应的速率常数(与温度有关),lgk与 的关系如图所示:
的关系如图所示:
下列说法正确的是
| A.升高温度,v正减小、v逆增大 | B.曲线②代表lgk正 |
| C.该反应易在高温下自发进行 | D. ℃-1时,该反应的平衡常数K为10 ℃-1时,该反应的平衡常数K为10 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定体积的密闭容器中进行反应:CO2(g)+H2(g) CO(g)+H2O(g),平衡常数K和温度t的关系如表,下列说不正确的是
CO(g)+H2O(g),平衡常数K和温度t的关系如表,下列说不正确的是
 CO(g)+H2O(g),平衡常数K和温度t的关系如表,下列说不正确的是
CO(g)+H2O(g),平衡常数K和温度t的关系如表,下列说不正确的是| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A.该反应的△H>0 |
| B.当v正(H2)=v正(H2O)时,该反应达到化学平衡状态 |
| C.平衡浓度符合c(CO2)c(H2)=c(CO)c(H2O),此时温度为830℃ |
| D.1200℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2mol·L-1、2mol·L-1、4mol·L-1、4 mol·L-1,则此时平衡向逆反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据化学反应速率和化学平衡理论,联系生产实际,你认为下列说法不正确 的是
| A.化学反应速率理论可指导怎样在一定时间内快出产品 |
| B.勒夏特列原理可指导怎样使用有限原料多出产品 |
| C.催化剂的使用是提高原料转化率的有效方法 |
| D.正确利用化学反应速率和化学反应限度理论,可以提高化工生产的综合经济效益 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】由γ-羟基丁酸生成γ-丁内酯的反应为HOCH2CH2CH2COOH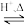
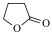 +H2O。在25℃下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:
+H2O。在25℃下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:
则下列说法不正确的是
 +H2O。在25℃下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:
+H2O。在25℃下,γ-羟基丁酸水溶液的初始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如图所示:| t/min | 21 | 50 | 80 | 100 | 120 | 160 | 220 | ∞ |
| c/ mol·L-1 | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
| A.在50~80 min内,以γ-丁内酯的浓度变化表示的反应速率为7×10-4 mol·L-1·min-1 |
| B.25℃时该反应的平衡常数K=2.5 |
| C.120 min时γ-羟基丁酸的转化率为50% |
| D.为提高γ-羟基丁酸的平衡转化率,除适当控制反应温度外,还可采用的措施是及时分离出γ-丁内酯 |
您最近一年使用:0次

 ”,压缩反应容器体积,颜色变深
”,压缩反应容器体积,颜色变深


 ,反应一段时间后达到平衡状态,测得生成1.6 mol C。下列说法正确的是
,反应一段时间后达到平衡状态,测得生成1.6 mol C。下列说法正确的是