将0.2 mol/L的NH4NO3溶液与0.1 mol/L的NaOH溶液等体积混合,下列有关混合溶液中微粒的浓度关系正确的是
A.c(NH )=c(Na+)>c(OH-)>c(NH3·H2O) )=c(Na+)>c(OH-)>c(NH3·H2O) | B.c(NH )=c(Na+)>c(NH3·H2O)>c(OH-) )=c(Na+)>c(NH3·H2O)>c(OH-) |
C.c(Na+)>c(NH )>c(NH3·H2O)>c(OH-) )>c(NH3·H2O)>c(OH-) | D.c(NH )+c(Na+)+c(H+)=c(OH-)+c(NO )+c(Na+)+c(H+)=c(OH-)+c(NO ) ) |
21-22高二上·陕西西安·期末 查看更多[4]
陕西省西安市西航一中2021-2022学年高二上学期期末考试化学试题(已下线)3.3.1 盐类的水解-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)
更新时间:2022-09-02 00:15:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列比较中正确的是
| A.相同浓度的溶液:①(NH4)2S溶液②Na2S溶液③H2S溶液中c(S2-):③>①>② |
| B.相同pH的溶液:①NaClO溶液②NaHCO3溶液③CH3COONa溶液中c(Na+):①>②>③ |
| C.同种溶液:①0.1mol·L-1FeCl3溶液②0.01mol·L-1FeCl3溶液③0.001mol·L-1FeCl3溶液中pH:③>②>① |
| D.相同浓度的溶液:①氨水、②NaOH溶液、③Ba(OH)2溶液中c(H+):②>①>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列实验不能证明一元酸HR为弱酸的是( )
| A.室温下,NaR溶液的pH大于7 |
| B.HR溶液加入少量NaR固体,溶解后溶液的pH变大 |
| C.加热NaR溶液时,溶液的pH变小 |
| D.70 ℃时,0.01 mol·L-1的HR溶液pH=2.8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,用HCl气体调节0.1mol/L氨水的pH,系统中微粒浓度的对数值(lgc)与pH的关系如图1所示,反应物的物质的量之比[t= ]与pH的关系如图2所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
]与pH的关系如图2所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
 ]与pH的关系如图2所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
]与pH的关系如图2所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的是
| A.P1所示溶液:c(Cl-)=0.05mol/L |
| B.25℃时,NH3·H2O的电离平衡常数为10-9.25 |
C.P3所示溶液:c( )+c(NH3·H2O)=c(Cl-)+c(H+) )+c(NH3·H2O)=c(Cl-)+c(H+) |
D.P2所示溶液:c( )>100c(NH3·H2O) )>100c(NH3·H2O) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25 ℃时,下列有关电解质溶液的说法不正确的是
A.将CH3COONa溶液从20 ℃升温至30 ℃,溶液中 增大 增大 |
| B.分别向1 mL pH=3的盐酸和pH=3的CH3COOH溶液中加入少量CH3COONa固体,两溶液pH均增大 |
| C.浓度均为0.1 mol·L-1的下列溶液,pH由大到小的排列顺序为NaOH>Na2CO3> (NH4)2SO4>NaHSO4 |
| D.0.2 mol·L-1 HCOOH与0.1 mol·L-1 NaOH等体积混合后的溶液中:c(HCOO-)+2c(OH-)=c(HCOOH)+2c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
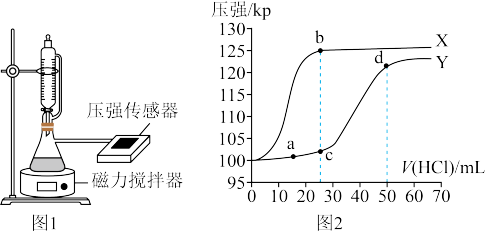
【推荐3】常温下,用如图1所示装置,分别向 溶液和
溶液和 溶液中逐滴滴加
溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的是
的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的是
 溶液和
溶液和 溶液中逐滴滴加
溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的是
的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的是
A.X曲线为 溶液的滴定曲线 溶液的滴定曲线 |
| B.b点溶液的pH大于c点溶液的pH |
C.c点的溶液中: |
| D.a、d两点水的电离程度:a>d |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 时,浓度均为
时,浓度均为 的HA溶液和BOH溶液的pH分别是1和11。下列说法中正确的是
的HA溶液和BOH溶液的pH分别是1和11。下列说法中正确的是
 时,浓度均为
时,浓度均为 的HA溶液和BOH溶液的pH分别是1和11。下列说法中正确的是
的HA溶液和BOH溶液的pH分别是1和11。下列说法中正确的是A.BOH的电离方程式为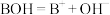 |
B.将一定体积的上述两种溶液混合后得到中性溶液,则 |
C.在 溶液中: 溶液中: |
D.若将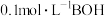 溶液稀释至 溶液稀释至 ,则溶液的 ,则溶液的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
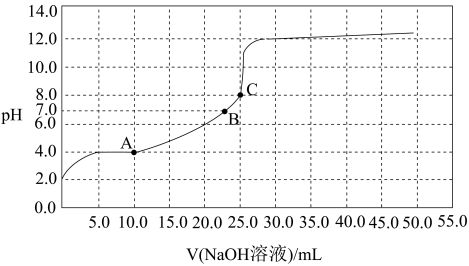
【推荐2】常温时,用0.10mol/L NaOH溶液滴定25.00mL 0.10molL某一元酸HX的溶液,滴定过程中pH变化曲线如图所示,下列判断不正确的是
| A.HX为一元弱酸 |
| B.V(NaOH 溶液)=12.50mL时,c(X-)>c(Na+ )>c(H+)>c(OH-) |
| C.溶液pH=7时,HX和NaOH恰好完全反应 |
| D.V(NaOH溶液)=25.00mL时,c(Na+)= c(X-)+c(HX) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】甲胺(CH3NH2)是一种应用广泛的一元弱碱,其电离方程式为:CH3NH2+H2O CH3NH3++OH-常温下,向20.0mL0.10mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是( )
CH3NH3++OH-常温下,向20.0mL0.10mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是( )

 CH3NH3++OH-常温下,向20.0mL0.10mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是( )
CH3NH3++OH-常温下,向20.0mL0.10mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是( )
| A.b点对应加入盐酸的体积V<20.00mL |
| B.常温下,甲胺的电离常数为Kb,则Kb=10-3.4 |
| C.b点可能存在关系:c(Cl-)>c(CH3NH3+)>c(H+)>cOH-) |
| D.V=20.00mL时,溶液中水电离的c(H+)>10-7mol/L |
您最近一年使用:0次





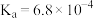

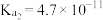


 不与盐酸溶液反应
不与盐酸溶液反应


