不同催化剂作用下NH3还原NOx的机理与效果是研究烟气(含NOx、O2、N2等)脱硝的热点。
(1)NH3还原NO的主反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g)。
已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-1269kJ·mol-1
上述主反应的△H=____ 。
(2)在某钒催化剂中添加一定量Cu2O可加快NO的脱除效率,其可能机理如图1所示(*表示物种吸附在催化剂表面,部分物种未画出)。

①X、Y处V元素化合价为+4或+5价。X处V元素化合价为____ 。
②NO转化为N2的机理可描述为____ 。
③烟气中若含有SO2,会生成NH4HSO4堵塞催化剂孔道。生成NH4HSO4的化学方程式为____ 。
(3)将模拟烟气(一定比例NOx、NH3、O2和N2)以一定流速通过装有Fe/Zr催化剂的反应管,测得NOx转化率随温度变化的曲线如图2所示。
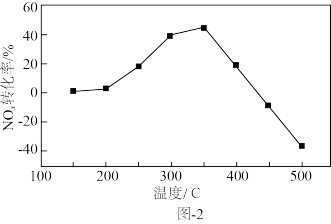
①温度低于350℃时,NOx转化率随温度升高而增大,其可能原因是_____ 。
②温度高于450℃时,NOx转化率已降低为负值,其可能原因是____ 。
(1)NH3还原NO的主反应为4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g)。
已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-1269kJ·mol-1
上述主反应的△H=
(2)在某钒催化剂中添加一定量Cu2O可加快NO的脱除效率,其可能机理如图1所示(*表示物种吸附在催化剂表面,部分物种未画出)。

①X、Y处V元素化合价为+4或+5价。X处V元素化合价为
②NO转化为N2的机理可描述为
③烟气中若含有SO2,会生成NH4HSO4堵塞催化剂孔道。生成NH4HSO4的化学方程式为
(3)将模拟烟气(一定比例NOx、NH3、O2和N2)以一定流速通过装有Fe/Zr催化剂的反应管,测得NOx转化率随温度变化的曲线如图2所示。

①温度低于350℃时,NOx转化率随温度升高而增大,其可能原因是
②温度高于450℃时,NOx转化率已降低为负值,其可能原因是
更新时间:2022-10-08 11:49:38
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】氯及其化合物在生活和生产中应用广泛。
(1)已知:900 K时,4HCl(g)+O2(g) 2Cl2(g)+2H2O(g),反应自发。
2Cl2(g)+2H2O(g),反应自发。
①该反应是放热还是吸热,判断并说明理由___________________________ 。
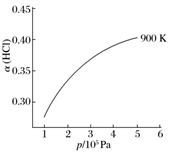
②900 K时,体积比为4∶1的HCl和O2在恒温恒容的密闭容器中发生反应,HCl的平衡转化率α(HCl)随压强(p)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在1.5×105~4.5 ×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。
×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。_____________________
(2)已知:Cl2(g)+2NaOH(aq)===NaCl(aq)+NaClO(aq)+H2O(l) ΔHl=-102 kJ·mol-1
3Cl2(g)+6NaOH(aq)===5NaCl(aq)+NaClO3(aq)+3H2O(l) ΔH2=-422 kJ·mol-1
①写出在溶液中NaClO分解生成NaClO3的热化学方程式:________________________________ 。
②用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3),此时ClO-的浓度为c0 mol·L-1;加热时NaClO转化为NaClO3,测得t时刻溶液中ClO-浓度为ct mol·L-1,写出该时刻溶液中Cl-浓度的表达式:c(Cl-)=________________ (用c0、ct表示)mol·L-1。
③有研究表明,生成NaClO3的反应分两步进行:
Ⅰ.2ClO-===ClO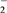 + Cl-
+ Cl-
Ⅱ.ClO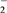 +ClO-===ClO
+ClO-===ClO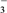 +Cl-
+Cl-
常温下,反应Ⅱ能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:______________________________________________________ 。
(1)已知:900 K时,4HCl(g)+O2(g)
 2Cl2(g)+2H2O(g),反应自发。
2Cl2(g)+2H2O(g),反应自发。①该反应是放热还是吸热,判断并说明理由
②900 K时,体积比为4∶1的HCl和O2在恒温恒容的密闭容器中发生反应,HCl的平衡转化率α(HCl)随压强(p)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在1.5×105~4.5
 ×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。
×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。
(2)已知:Cl2(g)+2NaOH(aq)===NaCl(aq)+NaClO(aq)+H2O(l) ΔHl=-102 kJ·mol-1
3Cl2(g)+6NaOH(aq)===5NaCl(aq)+NaClO3(aq)+3H2O(l) ΔH2=-422 kJ·mol-1
①写出在溶液中NaClO分解生成NaClO3的热化学方程式:
②用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3),此时ClO-的浓度为c0 mol·L-1;加热时NaClO转化为NaClO3,测得t时刻溶液中ClO-浓度为ct mol·L-1,写出该时刻溶液中Cl-浓度的表达式:c(Cl-)=
③有研究表明,生成NaClO3的反应分两步进行:
Ⅰ.2ClO-===ClO
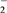 + Cl-
+ Cl-Ⅱ.ClO
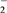 +ClO-===ClO
+ClO-===ClO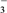 +Cl-
+Cl-常温下,反应Ⅱ能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】氮的氧化物是造成大气污染的主要物质。研究它们的反应机理,对于消除环境污染有重要意义。
(1)已知:4NH3(g)+5O2(g)=4NO(g) +6H2O(g) △H1=-907.0 kJ/mol
4NH3(g) +3O2(g)=2N2(g)+6H2O(g)△H2=-1269.0 kJ/mol
若4NH3(g) +6NO(g) 5N2(g) +6H2O(g)的正反应活化能为E正kJ/mol,则其逆反应活化能为
5N2(g) +6H2O(g)的正反应活化能为E正kJ/mol,则其逆反应活化能为___________ kJ/mol(用含E正的代数式表示)。
(2)在一定条件下,向某2 L密闭容器中分别投入一定量的NH3、NO发生反应:4NH3(g) +6NO(g) 5N2(g) +6H2O(g),其他条件相同时,在甲、乙两种催化剂的作用下,NO的转化率与温度的关系如图所示。
5N2(g) +6H2O(g),其他条件相同时,在甲、乙两种催化剂的作用下,NO的转化率与温度的关系如图所示。
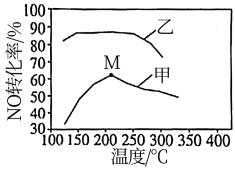
①工业上应选择催化剂___________ (填“甲”或“乙”)。
②M点是否为对应温度下NO的平衡转化率,判断理由是___________ 。温度高于210℃时,NO转化率降低的可能原因是___________ 。
(3)已知:NO2(g) +SO2(g) NO(g)+SO3(g)△H<0.向密闭容器中充入等体积的NO2和SO2,测得平衡状态时压强对数1gp(NO2)和lgp(SO3)的关系如下图所示。
NO(g)+SO3(g)△H<0.向密闭容器中充入等体积的NO2和SO2,测得平衡状态时压强对数1gp(NO2)和lgp(SO3)的关系如下图所示。
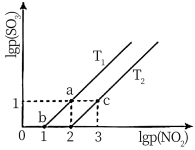
①ab两点体系总压强pa与pb的比值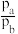 =
=___________ ;同一温度下图象呈线性变化的理由是___________ 。
②温度为T2时化学平衡常数Kp=___________ ,T1___________ T2(填“>”、“<”或“=”)。
(1)已知:4NH3(g)+5O2(g)=4NO(g) +6H2O(g) △H1=-907.0 kJ/mol
4NH3(g) +3O2(g)=2N2(g)+6H2O(g)△H2=-1269.0 kJ/mol
若4NH3(g) +6NO(g)
 5N2(g) +6H2O(g)的正反应活化能为E正kJ/mol,则其逆反应活化能为
5N2(g) +6H2O(g)的正反应活化能为E正kJ/mol,则其逆反应活化能为(2)在一定条件下,向某2 L密闭容器中分别投入一定量的NH3、NO发生反应:4NH3(g) +6NO(g)
 5N2(g) +6H2O(g),其他条件相同时,在甲、乙两种催化剂的作用下,NO的转化率与温度的关系如图所示。
5N2(g) +6H2O(g),其他条件相同时,在甲、乙两种催化剂的作用下,NO的转化率与温度的关系如图所示。
①工业上应选择催化剂
②M点是否为对应温度下NO的平衡转化率,判断理由是
(3)已知:NO2(g) +SO2(g)
 NO(g)+SO3(g)△H<0.向密闭容器中充入等体积的NO2和SO2,测得平衡状态时压强对数1gp(NO2)和lgp(SO3)的关系如下图所示。
NO(g)+SO3(g)△H<0.向密闭容器中充入等体积的NO2和SO2,测得平衡状态时压强对数1gp(NO2)和lgp(SO3)的关系如下图所示。
①ab两点体系总压强pa与pb的比值
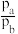 =
=②温度为T2时化学平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】氢能是最具应用前景的绿色能源,下列反应是目前大规模制取氢气的方法之一: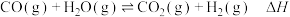
回答下列问题:
已知:①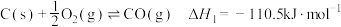 ;
;
②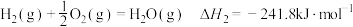 ;
;
③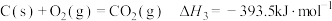 。
。
(1)
___________ 。
(2)实验发现,830℃时(其他条件相同),相同时间内,向上述体系中投入一定量的 可以提高
可以提高 的百分含量。做对比实验,结果如图所示:
的百分含量。做对比实验,结果如图所示:

分析无 、投入微米
、投入微米 、投入纳米
、投入纳米 ,
, 百分含量不同的原因是
百分含量不同的原因是___________ 。
(3)在 时,将
时,将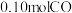 与
与 充入
充入 的恒容密闭容器中,反应达到平衡时,
的恒容密闭容器中,反应达到平衡时, 的物质的量分数
的物质的量分数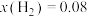 。
。
① 的平衡转化率
的平衡转化率
___________ %; 时,反应平衡常数
时,反应平衡常数
___________ (保留2位有效数字)。
②由 时上述实验数据计算得到
时上述实验数据计算得到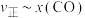 和
和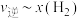 的关系如图1所示。若升高温度,反应重新达到平衡,则
的关系如图1所示。若升高温度,反应重新达到平衡,则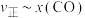 相应的点变为
相应的点变为___________ 、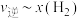 相应的点变为
相应的点变为___________ (填图中字母)。
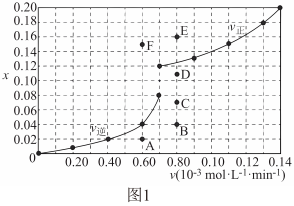
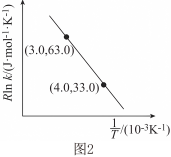
(4)反应 的Arrhenius经验公式的实验数据如图2中曲线所示,已知经验公式为
的Arrhenius经验公式的实验数据如图2中曲线所示,已知经验公式为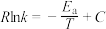 (其中
(其中 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 为常数)。该反应的活化能
为常数)。该反应的活化能
___________  。
。
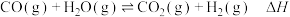
回答下列问题:
已知:①
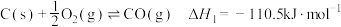 ;
;②
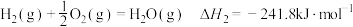 ;
;③
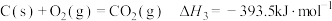 。
。(1)

(2)实验发现,830℃时(其他条件相同),相同时间内,向上述体系中投入一定量的
 可以提高
可以提高 的百分含量。做对比实验,结果如图所示:
的百分含量。做对比实验,结果如图所示:
分析无
 、投入微米
、投入微米 、投入纳米
、投入纳米 ,
, 百分含量不同的原因是
百分含量不同的原因是(3)在
 时,将
时,将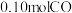 与
与 充入
充入 的恒容密闭容器中,反应达到平衡时,
的恒容密闭容器中,反应达到平衡时, 的物质的量分数
的物质的量分数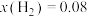 。
。①
 的平衡转化率
的平衡转化率
 时,反应平衡常数
时,反应平衡常数
②由
 时上述实验数据计算得到
时上述实验数据计算得到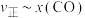 和
和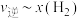 的关系如图1所示。若升高温度,反应重新达到平衡,则
的关系如图1所示。若升高温度,反应重新达到平衡,则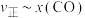 相应的点变为
相应的点变为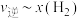 相应的点变为
相应的点变为
(4)反应
 的Arrhenius经验公式的实验数据如图2中曲线所示,已知经验公式为
的Arrhenius经验公式的实验数据如图2中曲线所示,已知经验公式为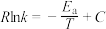 (其中
(其中 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 为常数)。该反应的活化能
为常数)。该反应的活化能
 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】磷精矿湿法制备磷酸的一种工艺流程如下:

已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)上述流程中能加快反应速率的措施有___ 。
(2)磷精矿粉酸浸时发生反应:2Ca5(PO4)3(OH)+3H2O+10H2SO4 10CaSO4·0.5H2O+6H3PO4
10CaSO4·0.5H2O+6H3PO4
①该反应体现出酸性关系:H3PO4___ H2SO4(填“>”或“<”)。
②结合元素周期律解释①中结论:P和S电子层数相同,___ 。
(3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。写出生成HF的化学方程式:__ 。
(4)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:___ 。

(5)脱硫时,CaCO3稍过量,充分反应后仍有SO42-残留,加入BaCO3可进一步提高硫的脱除率,其离子方程式是__ 。

已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)上述流程中能加快反应速率的措施有
(2)磷精矿粉酸浸时发生反应:2Ca5(PO4)3(OH)+3H2O+10H2SO4
 10CaSO4·0.5H2O+6H3PO4
10CaSO4·0.5H2O+6H3PO4①该反应体现出酸性关系:H3PO4
②结合元素周期律解释①中结论:P和S电子层数相同,
(3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。写出生成HF的化学方程式:
(4)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:

(5)脱硫时,CaCO3稍过量,充分反应后仍有SO42-残留,加入BaCO3可进一步提高硫的脱除率,其离子方程式是
您最近一年使用:0次
【推荐2】二氧化碳是用途非常广泛的基础化工原料,回答下列问题:
(1)工业上可以用 来生产燃料甲醇。
来生产燃料甲醇。
已知: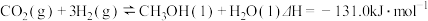 ;
;

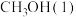 的燃烧热
的燃烧热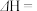
_________ 。
(2)在催化剂作用下, 和
和 可以直接转化为乙酸:
可以直接转化为乙酸: 。在不同温度下乙酸的生成速率变化如图所示。
。在不同温度下乙酸的生成速率变化如图所示。

①温度在 范围时,乙酸的生成速率减慢的主要原因是
范围时,乙酸的生成速率减慢的主要原因是___________ ,当温度在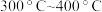 范围时,影响乙酸生成速率的主要因素是
范围时,影响乙酸生成速率的主要因素是__________ 。
②欲使乙酸的平衡产率提高,应采取的措施是__________ (填标号)。
A.升高温度 B.降低温度 C.增大压强 D.加入合适的催化剂
(3)高温下, 与足量的碳在密闭容器中实现反应:
与足量的碳在密闭容器中实现反应:
①向容积为1L的恒容器中加入0.2mol ,在不同温度下达到平衡时
,在不同温度下达到平衡时 的物质的量浓度
的物质的量浓度 随温度的变化如图所示。
随温度的变化如图所示。

某温度下,若向该平衡体系中再通入0.2mol ,达到新平衡后,体系中CO的百分含量
,达到新平衡后,体系中CO的百分含量________ (填“变大”“变小”或“不变”)。若升高温度,再次达到平衡,气体的平均摩尔质量_______ (填“变大”“变小”或“不变”或“无法确定”)
②向压强为p MPa、体积可变的恒压容器中充入一定量 ,
, 时反应达到平衡,CO的体积分数为40%,则
时反应达到平衡,CO的体积分数为40%,则 的转化率为
的转化率为_________ 。
(4)反应 的正、逆反应速率可表示为:
的正、逆反应速率可表示为: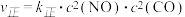 ,
,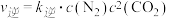 ;k正、k逆分别为正、逆反应速率常数,c为物质的量浓度,一定温度下,在体积为1L的容器加入2mol NO和2mol CO发生上述反应,测得CO和
;k正、k逆分别为正、逆反应速率常数,c为物质的量浓度,一定温度下,在体积为1L的容器加入2mol NO和2mol CO发生上述反应,测得CO和 物质的量浓度随时间的变化如下图所示,则a点时,v正:v逆=
物质的量浓度随时间的变化如下图所示,则a点时,v正:v逆=__________

(1)工业上可以用
 来生产燃料甲醇。
来生产燃料甲醇。已知:
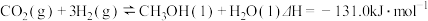 ;
;
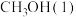 的燃烧热
的燃烧热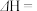
(2)在催化剂作用下,
 和
和 可以直接转化为乙酸:
可以直接转化为乙酸: 。在不同温度下乙酸的生成速率变化如图所示。
。在不同温度下乙酸的生成速率变化如图所示。
①温度在
 范围时,乙酸的生成速率减慢的主要原因是
范围时,乙酸的生成速率减慢的主要原因是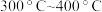 范围时,影响乙酸生成速率的主要因素是
范围时,影响乙酸生成速率的主要因素是②欲使乙酸的平衡产率提高,应采取的措施是
A.升高温度 B.降低温度 C.增大压强 D.加入合适的催化剂
(3)高温下,
 与足量的碳在密闭容器中实现反应:
与足量的碳在密闭容器中实现反应:
①向容积为1L的恒容器中加入0.2mol
 ,在不同温度下达到平衡时
,在不同温度下达到平衡时 的物质的量浓度
的物质的量浓度 随温度的变化如图所示。
随温度的变化如图所示。
某温度下,若向该平衡体系中再通入0.2mol
 ,达到新平衡后,体系中CO的百分含量
,达到新平衡后,体系中CO的百分含量②向压强为p MPa、体积可变的恒压容器中充入一定量
 ,
, 时反应达到平衡,CO的体积分数为40%,则
时反应达到平衡,CO的体积分数为40%,则 的转化率为
的转化率为(4)反应
 的正、逆反应速率可表示为:
的正、逆反应速率可表示为: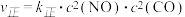 ,
,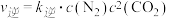 ;k正、k逆分别为正、逆反应速率常数,c为物质的量浓度,一定温度下,在体积为1L的容器加入2mol NO和2mol CO发生上述反应,测得CO和
;k正、k逆分别为正、逆反应速率常数,c为物质的量浓度,一定温度下,在体积为1L的容器加入2mol NO和2mol CO发生上述反应,测得CO和 物质的量浓度随时间的变化如下图所示,则a点时,v正:v逆=
物质的量浓度随时间的变化如下图所示,则a点时,v正:v逆=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】某研究性学习组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
(1)通过实验A、B,可探究出_______ 的改变对反应速率的影响,其中V1=_____ ,T1=_____ ,通过实验_______ 可探究出温度变化对化学反应速率的影响。
(2)若t1<8,则由实验A、B可以得出的结论是______________________________ ;利用实验B中数据计算,用KMnO4的浓度变化表示的反应速率为____________ 。
(3)该反应中有无色无味气体产生且锰被还原为Mn2+,写出相应反应的离子方程式_________________________ 。
(4)该小组的一位同学通过查阅资料发现:反应一段时间后该反应速率会加快,造成此种变化的原因是反应体系中的某种粒子对KMnO4与H2C2O4之间的反应有某种特殊的作用,则该作用是_______________ ,相应的粒子最有可能是(填符号)_______ 。
| 实验序号 | 实验温度 | KMnO4溶液 | H2C2O4溶液 | H2O | 溶液褪色时间 | ||
| V(mL) | C(mol/L) | V(mL) | C(mol/L) | V(mL) | t(s) | ||
| A | 293K | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313K | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)若t1<8,则由实验A、B可以得出的结论是
(3)该反应中有无色无味气体产生且锰被还原为Mn2+,写出相应反应的离子方程式
(4)该小组的一位同学通过查阅资料发现:反应一段时间后该反应速率会加快,造成此种变化的原因是反应体系中的某种粒子对KMnO4与H2C2O4之间的反应有某种特殊的作用,则该作用是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】CH4(其中C为—4价)既是一种重要的能源,也是一种重要的化工原料。
(1)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图甲所示,通入a气体的一极的电极反应式为_______ 。通入2.24L(已换算为标准状况)a气体时,通过质子交换膜转移的H+数目为_______ (设NA为阿伏加德罗常数的值)。

(2)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图乙所示,则该反应的最佳温度应控制在_______ ℃左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其反应的离子方程式为_______ 。
③CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2、CO2和H2O,若标准状况下8.96LCH4可处理22.4LNOx,则x值为_______ 。
(1)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图甲所示,通入a气体的一极的电极反应式为

(2)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图乙所示,则该反应的最佳温度应控制在
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其反应的离子方程式为
③CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2、CO2和H2O,若标准状况下8.96LCH4可处理22.4LNOx,则x值为
您最近一年使用:0次
【推荐2】环氧乙烷(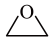 ,别称EO)是重要的杀菌剂和工业合成原料。回答下列问题:
,别称EO)是重要的杀菌剂和工业合成原料。回答下列问题:
(一)乙烯直接氧化法:
反应I:CH2=CH2(g)+ O2(g)→
O2(g)→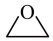 (g) ΔH1
(g) ΔH1
反应II:CH2=CH2(g)+3O2(g)→2CO2(g)+2H2O(g) ΔH2
(1)乙烯与O2在a、b两种催化剂作用下发生反应,催化剂的催化活性(用EO%衡量)及生成EO的选择性(用EO选择性%表示)与温度(T)的变化曲线如图一所示。

①依据图给信息,选择制备环氧乙烷的适宜条件为_____ 。
②M点后曲线下降的原因为_____ 。
③下列说法正确的有_____ (填标号)。
A.催化剂的选择性越高,其达到最高反应活性所需的温度越高
B.不同催化剂达到最高活性时的温度不同
C.催化剂的催化活性与温度成正比
(2)设K 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。反应I、II对应的-lnK
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。反应I、II对应的-lnK 随
随 (温度的倒数)的变化如图二所示。
(温度的倒数)的变化如图二所示。
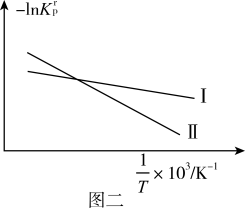
ΔH2_____ 0(填“>”或“<”)。
(二)电化学合成法
(3)科学家利用CO2、水合成环氧乙烷,有利于实现碳中和。总反应为:2CO2+2H2O→ +2.5O2,该过程在两个独立的电解槽中实现,装置如图三所示,在电解槽2中利用氯离子介导制备环氧乙烷,内部结构如图四所示。
+2.5O2,该过程在两个独立的电解槽中实现,装置如图三所示,在电解槽2中利用氯离子介导制备环氧乙烷,内部结构如图四所示。
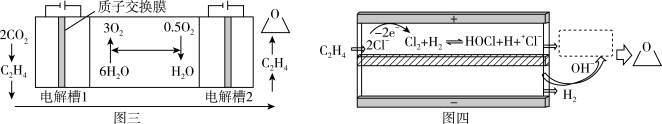
①电解槽1中阴极的电极反应式为_____ 。
②图四虚线框中发生多个反应,有中间产物HOCH2CH2Cl生成,最终生成环氧乙烷,其反应过程可描述为_____ 。
 ,别称EO)是重要的杀菌剂和工业合成原料。回答下列问题:
,别称EO)是重要的杀菌剂和工业合成原料。回答下列问题:(一)乙烯直接氧化法:
反应I:CH2=CH2(g)+
 O2(g)→
O2(g)→ (g) ΔH1
(g) ΔH1反应II:CH2=CH2(g)+3O2(g)→2CO2(g)+2H2O(g) ΔH2
(1)乙烯与O2在a、b两种催化剂作用下发生反应,催化剂的催化活性(用EO%衡量)及生成EO的选择性(用EO选择性%表示)与温度(T)的变化曲线如图一所示。

①依据图给信息,选择制备环氧乙烷的适宜条件为
②M点后曲线下降的原因为
③下列说法正确的有
A.催化剂的选择性越高,其达到最高反应活性所需的温度越高
B.不同催化剂达到最高活性时的温度不同
C.催化剂的催化活性与温度成正比
(2)设K
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。反应I、II对应的-lnK
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。反应I、II对应的-lnK 随
随 (温度的倒数)的变化如图二所示。
(温度的倒数)的变化如图二所示。
ΔH2
(二)电化学合成法
(3)科学家利用CO2、水合成环氧乙烷,有利于实现碳中和。总反应为:2CO2+2H2O→
 +2.5O2,该过程在两个独立的电解槽中实现,装置如图三所示,在电解槽2中利用氯离子介导制备环氧乙烷,内部结构如图四所示。
+2.5O2,该过程在两个独立的电解槽中实现,装置如图三所示,在电解槽2中利用氯离子介导制备环氧乙烷,内部结构如图四所示。
①电解槽1中阴极的电极反应式为
②图四虚线框中发生多个反应,有中间产物HOCH2CH2Cl生成,最终生成环氧乙烷,其反应过程可描述为
您最近一年使用:0次
【推荐3】研究脱除烟气中的 、
、 是环境保护、促进社会可持续发展的重要课题。
是环境保护、促进社会可持续发展的重要课题。
(1)烟气中的 可在催化剂作用下用
可在催化剂作用下用 还原。
还原。
①已知:



有氧条件下, 与
与 反应生成
反应生成 ,相关热化学方程式为
,相关热化学方程式为

___________  。
。
②其他条件相同,以一定流速分别向含催化剂A和B的反应管中通入一定比例 、
、 、
、 和
和 的模拟烟气,测得
的模拟烟气,测得 的去除率与温度的关系如图所示。使用催化剂B,当温度高于360℃,
的去除率与温度的关系如图所示。使用催化剂B,当温度高于360℃, 的去除率下降的原因是
的去除率下降的原因是___________ 。

(2) 在一定条件下能有效去除烟气中的
在一定条件下能有效去除烟气中的 、
、 ,可能的反应机理如图所示,该过程可描述为
,可能的反应机理如图所示,该过程可描述为___________ 。

(3)尿素[ ]溶液可吸收含
]溶液可吸收含 、
、 烟气中的
烟气中的 ,其反应为
,其反应为 。若吸收烟气时同时通入少量
。若吸收烟气时同时通入少量 ,可同时实现脱硫、脱硝。
,可同时实现脱硫、脱硝。
①脱硝的反应分为两步。第一步: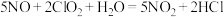 。第二步:
。第二步: 和
和 反应生成
反应生成 和
和 。第二步的化学反应方程式为
。第二步的化学反应方程式为___________ 。
②将含 、
、 烟气以一定的流速通过10%的
烟气以一定的流速通过10%的 溶液,其他条件相同,不通
溶液,其他条件相同,不通 和通少量
和通少量 时
时 的去除率如图所示。通少量
的去除率如图所示。通少量 时
时 的去除率较低的原因是
的去除率较低的原因是___________ 。

 、
、 是环境保护、促进社会可持续发展的重要课题。
是环境保护、促进社会可持续发展的重要课题。(1)烟气中的
 可在催化剂作用下用
可在催化剂作用下用 还原。
还原。①已知:




有氧条件下,
 与
与 反应生成
反应生成 ,相关热化学方程式为
,相关热化学方程式为

 。
。②其他条件相同,以一定流速分别向含催化剂A和B的反应管中通入一定比例
 、
、 、
、 和
和 的模拟烟气,测得
的模拟烟气,测得 的去除率与温度的关系如图所示。使用催化剂B,当温度高于360℃,
的去除率与温度的关系如图所示。使用催化剂B,当温度高于360℃, 的去除率下降的原因是
的去除率下降的原因是
(2)
 在一定条件下能有效去除烟气中的
在一定条件下能有效去除烟气中的 、
、 ,可能的反应机理如图所示,该过程可描述为
,可能的反应机理如图所示,该过程可描述为
(3)尿素[
 ]溶液可吸收含
]溶液可吸收含 、
、 烟气中的
烟气中的 ,其反应为
,其反应为 。若吸收烟气时同时通入少量
。若吸收烟气时同时通入少量 ,可同时实现脱硫、脱硝。
,可同时实现脱硫、脱硝。①脱硝的反应分为两步。第一步:
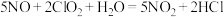 。第二步:
。第二步: 和
和 反应生成
反应生成 和
和 。第二步的化学反应方程式为
。第二步的化学反应方程式为②将含
 、
、 烟气以一定的流速通过10%的
烟气以一定的流速通过10%的 溶液,其他条件相同,不通
溶液,其他条件相同,不通 和通少量
和通少量 时
时 的去除率如图所示。通少量
的去除率如图所示。通少量 时
时 的去除率较低的原因是
的去除率较低的原因是
您最近一年使用:0次



