硅电池、锂离子电池都是现代高性能电池的代表,高性能的电极材料与物质结构密切相关。
(1)LiFePO4因具有良好的结构稳定性而成为新一代正极材料,这与 的结构密切相关,
的结构密切相关, 的空间结构为
的空间结构为_______ 。P、O、S的电负性从大到小的顺序为_______ 。
(2)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸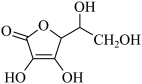 常被用作碳包覆的碳源,其易溶于水的原因是
常被用作碳包覆的碳源,其易溶于水的原因是_______ ,抗坏血酸中碳原子的杂化方式为_______ ,1 mol抗坏血酸中手性碳原子的数目为_______ 。
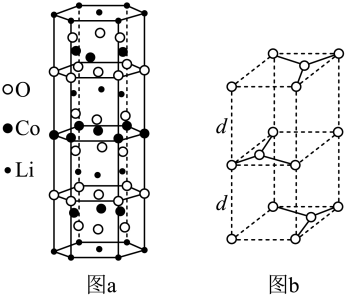
(3)目前最常用的电极材料有锂钴复合氧化物和石墨。_______ ,Co3+的价层电子排布式为_______ 。
②石墨晶胞(图b)层间距为d pm,C−C键长为a pm,石墨晶体的密度为ρ g·cm−3,列式表示阿伏加德罗常数为_______ mol−l。
(4)硅酸盐中Si元素一般显+4价,如下图所示是一种无限长单键的多聚硅酸根离子的结构,其中“ ”表示Si原子,“o”表示氧原子,则该长链硅酸根离子的通式为
”表示Si原子,“o”表示氧原子,则该长链硅酸根离子的通式为_______ 。
(1)LiFePO4因具有良好的结构稳定性而成为新一代正极材料,这与
 的结构密切相关,
的结构密切相关, 的空间结构为
的空间结构为(2)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸
 常被用作碳包覆的碳源,其易溶于水的原因是
常被用作碳包覆的碳源,其易溶于水的原因是(3)目前最常用的电极材料有锂钴复合氧化物和石墨。
②石墨晶胞(图b)层间距为d pm,C−C键长为a pm,石墨晶体的密度为ρ g·cm−3,列式表示阿伏加德罗常数为
(4)硅酸盐中Si元素一般显+4价,如下图所示是一种无限长单键的多聚硅酸根离子的结构,其中“
 ”表示Si原子,“o”表示氧原子,则该长链硅酸根离子的通式为
”表示Si原子,“o”表示氧原子,则该长链硅酸根离子的通式为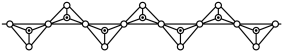
更新时间:2022-09-23 10:52:25
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
【推荐1】铁及其化合物在生活中有广泛应用。
(1)Fe3+基态价电子排布式为_______ 。
(2)实验室用KSCN溶液、苯酚检验Fe3+。
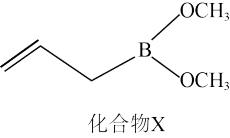
①1mol化合物X分子(结构如图)中含有σ键的数目为_______ 。
②类卤素离子SCN-可用于Fe2+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是_______ 。
(3)氮化铁晶体的晶胞结构如图1所示。该晶体化合物的化学式为_______ 。

图1
(4)某铁的化合物结构简式如图2所示。
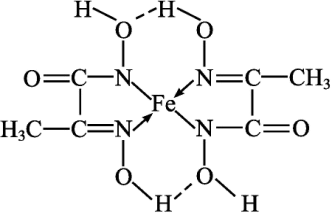
图2
①上述化合物中所含有的非金属元素的电负性由小到大的顺序为_______ (用元素符号表示)。
②上述化合物中碳原子的杂化方式为_______ 。
(1)Fe3+基态价电子排布式为
(2)实验室用KSCN溶液、苯酚检验Fe3+。
①1mol化合物X分子(结构如图)中含有σ键的数目为

②类卤素离子SCN-可用于Fe2+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是
(3)氮化铁晶体的晶胞结构如图1所示。该晶体化合物的化学式为

图1
(4)某铁的化合物结构简式如图2所示。

图2
①上述化合物中所含有的非金属元素的电负性由小到大的顺序为
②上述化合物中碳原子的杂化方式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表列出了前20号元素中某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是___________ (填元素符号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e 稳定结构的物质可能是___________ (写分子式,只答一条即可)。元素⑨和⑩形成的化合物的化学式为___________ ;元素①的原子价电子排布式是___________ 。
(3)①、⑥、⑦、⑩四种元素的电负性,由强到弱的顺序是___________ (填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是___________ (填名称),可以验证你的结论的是下列中的___________ (填序号)。
A.气态氢化物的稳定性 B.单质分子中的键能
C.两元素的电负性 D.最高价含氧酸的酸性
| 性质元素 | 原子半径(1019m) | 最高价态 | 最低价态 |
| ① | 1.02 | +6 | 2 |
| ② | 2.27 | +1 | — |
| ③ | 0.74 | — | 2 |
| ④ | 1.43 | +3 | — |
| ⑤ | 0.77 | +4 | 4 |
| ⑥ | 1.10 | +5 | 3 |
| ⑦ | 0.99 | +7 | 1 |
| ⑧ | 1.86 | +1 | — |
| ⑨ | 0.75 | +5 | 3 |
| ⑩ | 1.17 | +4 | 4 |
(1)以上10种元素中,第一电离能最小的是
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e 稳定结构的物质可能是
(3)①、⑥、⑦、⑩四种元素的电负性,由强到弱的顺序是
(4)③和⑨两元素比较,非金属性较弱的是
A.气态氢化物的稳定性 B.单质分子中的键能
C.两元素的电负性 D.最高价含氧酸的酸性
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】点击化学(click chemistry)是一种能够让分子的构建模块快速、高效地结合在一起的化学反应。科学工作者可以利用基础模块搭建出变化无穷的造型,就如同玩乐高玩具一般。叠氨化物和块经合成抗真菌药物三唑是点击化学的重要应用,反应示例如下:
(1) 的核外电子排布式为
的核外电子排布式为_______ 。
(2)C、N、Cu的电负性由大到小的顺序为_______ 。
(3)分子乙中存在5中心6电子的大 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是_______ (填对应原子的序号)。
(4)分子中碳碳三键的活泼性:甲_______ 丙(填“>”“=”“<”),理由是_______ (从分子的结构角度分析)。
(5)丁形成的晶体中不存在的微粒间作用力有_______ 。
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中, 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。 的配位数为
的配位数为_______ 。
②由 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为_______ 。
 +CH3CH2N3
+CH3CH2N3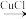

 +CH3CH2N3→
+CH3CH2N3→
(1)
 的核外电子排布式为
的核外电子排布式为(2)C、N、Cu的电负性由大到小的顺序为
(3)分子乙中存在5中心6电子的大
 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是(4)分子中碳碳三键的活泼性:甲
(5)丁形成的晶体中不存在的微粒间作用力有
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中,
 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。
 的配位数为
的配位数为②由
 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】硅及其化合物在生活、生产和科技等方面应用广泛。工业制备高纯硅的主要过程如下:
石英砂(主要成分 )
)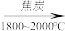 粗硅
粗硅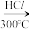

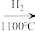 高纯硅
高纯硅
(1) 位于元素周期表第
位于元素周期表第_____ 周期,第_____ 族。
(2)由硅原子核形成的三种微粒,电子排布式分别为:a.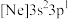 、b.
、b.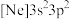 、c.
、c.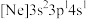 ,有关这些微粒的叙述,正确的是_____(填标号)。
,有关这些微粒的叙述,正确的是_____(填标号)。
(3)石英砂与焦炭反应制备粗硅的化学方程式为_____ 。粗硅与 反应过程中会有副产物
反应过程中会有副产物 生成,
生成, 中
中 的杂化轨道类型为
的杂化轨道类型为_____ 。 的键角
的键角_____ (填“大于”、“小于”或“等于”) 的键角。
的键角。
(4) 以空间结构为
以空间结构为_____ 。 和
和 会剧烈反应,写出该反应的化学方程式
会剧烈反应,写出该反应的化学方程式_____ (已知:电负性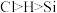 )。
)。
石英砂(主要成分
 )
)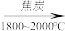 粗硅
粗硅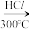

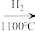 高纯硅
高纯硅(1)
 位于元素周期表第
位于元素周期表第(2)由硅原子核形成的三种微粒,电子排布式分别为:a.
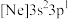 、b.
、b.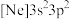 、c.
、c.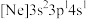 ,有关这些微粒的叙述,正确的是_____(填标号)。
,有关这些微粒的叙述,正确的是_____(填标号)。A.微粒半径: |
| B.电子排布属于基态原子(或离子)的是:a、b |
C.电离一个电子所需最低能量: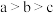 |
D.得电子能力: |
 反应过程中会有副产物
反应过程中会有副产物 生成,
生成, 中
中 的杂化轨道类型为
的杂化轨道类型为 的键角
的键角 的键角。
的键角。(4)
 以空间结构为
以空间结构为 和
和 会剧烈反应,写出该反应的化学方程式
会剧烈反应,写出该反应的化学方程式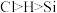 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】明代科学家宋应星在《天工开物》中写道:“凡玉入中国,贵者尽出于田葱岭”。和田玉的主要化学成分是含水的钙镁硅酸盐。回答下列问题:
(1)元素镁能形成很多简单微粒,下面是镁原子形成的微粒的电子排布式,其中再电离出一个电子所需能量最大的是______ (填标号),当从C状态变到B状态,形成的是______ 光谱(选填“发射”或“吸收”)。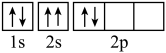 ,该电子排布图违背了
,该电子排布图违背了______ 。
(3)元素钙、镁和氯三种元素形成的最高价氧化物的水化物中,碱性最强的是______ (填化学式,下同),酸性最强的是______ 。
(4) 中中心原子Si的杂化类型是
中中心原子Si的杂化类型是______ ,离子空间结构为______ 。
(5)在 中不存在的化学键类型有
中不存在的化学键类型有______ 。
A.非极性共价键 B.极性共价键 C. 键 D.
键 D. 键
键
碳酸( )的酸性比硅酸(
)的酸性比硅酸( )
)______ (填“强”或“弱”),用离子方程式证明______ 。
(6)羧基( )能电离出
)能电离出 ,使溶液呈现酸性,已知
,使溶液呈现酸性,已知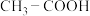 的酸性小于
的酸性小于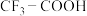 ,则推电子能力较强的是
,则推电子能力较强的是______ (填“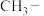 ”或“
”或“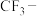 ”)
”)
(1)元素镁能形成很多简单微粒,下面是镁原子形成的微粒的电子排布式,其中再电离出一个电子所需能量最大的是
A. 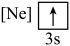 B.
B.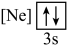 C.
C. 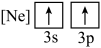 D.
D.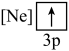
 ,该电子排布图违背了
,该电子排布图违背了(3)元素钙、镁和氯三种元素形成的最高价氧化物的水化物中,碱性最强的是
(4)
 中中心原子Si的杂化类型是
中中心原子Si的杂化类型是(5)在
 中不存在的化学键类型有
中不存在的化学键类型有A.非极性共价键 B.极性共价键 C.
 键 D.
键 D. 键
键碳酸(
 )的酸性比硅酸(
)的酸性比硅酸( )
)(6)羧基(
 )能电离出
)能电离出 ,使溶液呈现酸性,已知
,使溶液呈现酸性,已知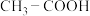 的酸性小于
的酸性小于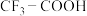 ,则推电子能力较强的是
,则推电子能力较强的是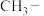 ”或“
”或“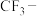 ”)
”)
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大,Z基态原子核外有三个未成对电子,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形,Q的各级电离能如下表,W与R是同族元素。
回答下列有关问题:
(1)W原子的价电子排布图 为_______________________________ 。
(2)化合物X 2W2的电子式______________ ,化合物XYZ的结构式________________ 。
(3)RW3分子中的键角___________ ,RW32-分子的立体构型是_______________ 形。
(4)YW2中的化学键类型为_________ 共价键(填“极性”或“非极性”),根据等电子原理,指出与YW互为等电子体且含有Z原子的微粒有________ (要求写一种即可)。
| Q | I1 | I2 | I3 | I4 | I5 | … |
| 电离能(kJ/mol) | 496 | 4562 | 6912 | 9543 | 13353 | … |
(1)W原子的
(2)化合物X 2W2的电子式
(3)RW3分子中的键角
(4)YW2中的化学键类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】2020年12月17日,“嫦娥五号”首次成功实现地外天体采样返回,标志着我国航天向前迈出了一大步。其制作材料中包含了Al、Cr、Cu、C、N、O、Si等多种元素。回答下列问题:
(1)上述元素中基态原子未成对电子数与Cu相同的有___ 。
(2)[Cr(NO2)(NH3)5]Cl2中Cr3+的配位数为___ 。配位体原子给出电子能力越强,则配位体与中心离子形成的配位键越强,配合物越稳定,NO 作为配体时提供孤电子对的原子是
作为配体时提供孤电子对的原子是___ 。粒子中的大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则NO
),则NO 的大π键可表示为
的大π键可表示为___ 。
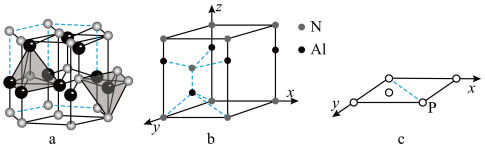
(3)氮化铝晶体是第三代半导体材料的典型代表之一,属于六方晶系,结构如图a所示,其晶体类型为___ ,其晶胞结构如图b所示,Al原子位于氮原子形成的___ 空隙(填“四面体”或“八面体”)。
(1)上述元素中基态原子未成对电子数与Cu相同的有
(2)[Cr(NO2)(NH3)5]Cl2中Cr3+的配位数为
 作为配体时提供孤电子对的原子是
作为配体时提供孤电子对的原子是 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则NO
),则NO 的大π键可表示为
的大π键可表示为
(3)氮化铝晶体是第三代半导体材料的典型代表之一,属于六方晶系,结构如图a所示,其晶体类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】锂—磷酸氧铜电池正极的活性物质是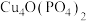 ,可通过下列反应制备:
,可通过下列反应制备: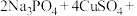
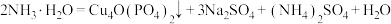 。
。
(1)写出基态 的电子排布式:
的电子排布式:_______________ 。
(2)P、S元素第一电离能大小关系为_______________ ,原因是_______________ 。
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为_______________ ,基态碳原子核外电子有_______________ 种运动状态。 ,生成配合物
,生成配合物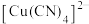 ,则
,则 该配合物含有
该配合物含有 键的数目为
键的数目为_______________ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为_______________ ,铜的原子半径为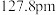 ,
, 表示阿伏加德罗常数的值,晶体铜的密度为
表示阿伏加德罗常数的值,晶体铜的密度为_______________  (列出计算式即可)。
(列出计算式即可)。
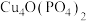 ,可通过下列反应制备:
,可通过下列反应制备: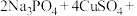
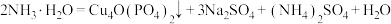 。
。(1)写出基态
 的电子排布式:
的电子排布式:(2)P、S元素第一电离能大小关系为
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为
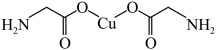
 ,生成配合物
,生成配合物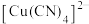 ,则
,则 该配合物含有
该配合物含有 键的数目为
键的数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为
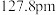 ,
, 表示阿伏加德罗常数的值,晶体铜的密度为
表示阿伏加德罗常数的值,晶体铜的密度为 (列出计算式即可)。
(列出计算式即可)。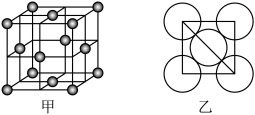
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】氧族元素的单质及其化合物是一类重要物质,请回答下列问题。
⑴基态硒(Se)原子的价层电子排布式为____________ 。
⑵OCN-中所含三种元素的电负性从大到小的顺序为________ (用元素符号表示,下同);第一电离能从大到小的顺序为________ 。已知等电子体具有相同的空间构型,则OCN-的空间构型为_______ 。
⑶H2O2分子中氧原子的轨道杂化类型是__________ ;H2O的沸点明显高于H2Se的沸点( 42℃),其主要原因是
42℃),其主要原因是_______________ 。
⑷硒化锌的晶胞结构如图所示,则硒化锌的化学式为_________ ,其中Zn(黑球)的配位数为______ 。

⑴基态硒(Se)原子的价层电子排布式为
⑵OCN-中所含三种元素的电负性从大到小的顺序为
⑶H2O2分子中氧原子的轨道杂化类型是
 42℃),其主要原因是
42℃),其主要原因是⑷硒化锌的晶胞结构如图所示,则硒化锌的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1) 的价电子排布图为:
的价电子排布图为:__ ;基态磷原子有___ 种空间运动状态不同的电子。
(2)Li、O、P三种元素的电负性由大到小的顺序是:__ 。
(3)写出一种与 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:__ ,该分子的中心原子的价层电子对数等于__ 。
(4)已知无水硫酸铜为白色粉末,溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间作用力有:__ 。
A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(5)N和P是同主族元素,但是 分子中的键角大于
分子中的键角大于 分子中的键角,原因是:
分子中的键角,原因是:___ 。
(6) 为离子晶体,具有反萤石结构,晶胞如下图所示。则
为离子晶体,具有反萤石结构,晶胞如下图所示。则 配位数为:
配位数为:__ ,若晶胞参数为bnm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为__  (列出计算式即可)。
(列出计算式即可)。

(1)
 的价电子排布图为:
的价电子排布图为:(2)Li、O、P三种元素的电负性由大到小的顺序是:
(3)写出一种与
 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(4)已知无水硫酸铜为白色粉末,溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间作用力有:
A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(5)N和P是同主族元素,但是
 分子中的键角大于
分子中的键角大于 分子中的键角,原因是:
分子中的键角,原因是:(6)
 为离子晶体,具有反萤石结构,晶胞如下图所示。则
为离子晶体,具有反萤石结构,晶胞如下图所示。则 配位数为:
配位数为: ,则
,则 的密度为
的密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】钛的化合物在化工、医药、材料等领域具有广泛应用。回答下列问题:
(1)基态Ti原子的未成对电子数是______ ,基态Ti原子4s轨道上的一个电子激发到 4p轨道上形成激发态,写出该激发态价层电子排布式______ 。
(2)钛卤化物的熔点和沸点如下表所示,TiCl4、TiBr4、TiI4 熔沸点依次升高的原因是______ ;TiF4熔点反常的原因是______ 。
Ti可形成配合物[Ti(urea)6](ClO4)3, urea表示尿素,其结构如图所示:

(3)配合物中Ti化合价为______ 。
(4)尿素中C原子的杂化轨道类型为______ 。
(5) ClO 的立体构型为
的立体构型为______ 。
(6)如图为具有较高催化活性材料金红石的晶胞结构,其化学式为______ 。

(1)基态Ti原子的未成对电子数是
(2)钛卤化物的熔点和沸点如下表所示,TiCl4、TiBr4、TiI4 熔沸点依次升高的原因是
TiF4 | TiCl4 | TiBr4 | TiI4 | |
熔点/℃ | 377 | -24 | 38 | 150 |
沸点/℃ | —— | 136 | 230 | 377 |

(3)配合物中Ti化合价为
(4)尿素中C原子的杂化轨道类型为
(5) ClO
 的立体构型为
的立体构型为(6)如图为具有较高催化活性材料金红石的晶胞结构,其化学式为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】X、Y、Z、W四种元素的部分信息如下表所示。
回答下列问题:
(1)X、Y、Z三种元素电负性由大到小的顺序为___________ (用具体的元素符号填写)。
(2)化合物 、
、 、
、 (气态或液态时)中,中心原子的轨道类型不是
(气态或液态时)中,中心原子的轨道类型不是 杂化的是
杂化的是___________ (填化学式,下同),分子构型是正四面体的是___________ , 属于
属于___________ (极性分子、非极性分子)。
(3)已知 的熔点:306℃,沸点:319℃,则
的熔点:306℃,沸点:319℃,则 的晶体类型为
的晶体类型为___________ 。
(4)在金属材料中添加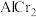 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
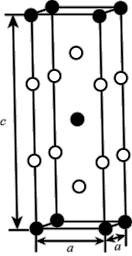
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。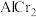 具有体心四方结构,如图所示。处于顶角位置的是
具有体心四方结构,如图所示。处于顶角位置的是___________ 原子。设Cr和Al原子半径分别为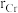 和
和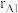 ,则金属原子空间占有率为
,则金属原子空间占有率为___________ %(列出计算表达式)。
| 元素 | X | Y | Z | W |
| 相关信息 | 短周期元素,最高化合价为+7价 | 基态原子中,电子占据的最高能层符号为M,最高能级上只有两个自旋方向相同的电子 | Z元素的价电子构型为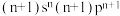 | W元素正三价离子的3d轨道为半充满状态 |
回答下列问题:
(1)X、Y、Z三种元素电负性由大到小的顺序为
(2)化合物
 、
、 、
、 (气态或液态时)中,中心原子的轨道类型不是
(气态或液态时)中,中心原子的轨道类型不是 杂化的是
杂化的是 属于
属于(3)已知
 的熔点:306℃,沸点:319℃,则
的熔点:306℃,沸点:319℃,则 的晶体类型为
的晶体类型为(4)在金属材料中添加
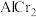 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。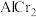 具有体心四方结构,如图所示。处于顶角位置的是
具有体心四方结构,如图所示。处于顶角位置的是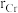 和
和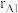 ,则金属原子空间占有率为
,则金属原子空间占有率为
您最近一年使用:0次



