下列物质中:① ②
② ③
③ ④盐酸 ⑤
④盐酸 ⑤ ⑥
⑥
(1)属于弱电解质的是____ (填序号,下同),属于强电解质且其水溶液呈碱性的是_____ 。
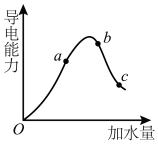
(2)在氨水中存在电离平衡: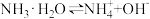 。将上述六种物质分别配成
。将上述六种物质分别配成 的溶液,向稀氨水中分别滴加少量六种溶液,能使氨水的电离平衡逆向移动且
的溶液,向稀氨水中分别滴加少量六种溶液,能使氨水的电离平衡逆向移动且 增大的是
增大的是_______ (填序号),此时
_______ (填“增大”“减小”或“不变”,下同),
_______ 。
(3)等体积、pH相同的盐酸和醋酸分别与 的
的 溶液恰好完全反应,消耗
溶液恰好完全反应,消耗 体积较大的是
体积较大的是_______ (填“ ”或“
”或“ ”),反应后溶液pH较大的是
”),反应后溶液pH较大的是_______ (填“ ”或“
”或“ ”)。
”)。
(4)已知次氯酸 的电离平衡常数为
的电离平衡常数为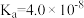 ,向
,向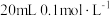 的
的 溶液中滴加少量硫酸,再加水稀释至
溶液中滴加少量硫酸,再加水稀释至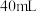 ,此时测得
,此时测得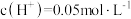 ,则溶液中
,则溶液中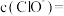
_______  。
。
(5)已知亚硫酸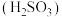 的电离平衡常数为
的电离平衡常数为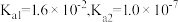 ;碳酸
;碳酸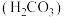 的电离平衡常数为
的电离平衡常数为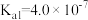 ,
,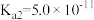 ,足量的
,足量的 溶液和
溶液和 溶液发生反应的主要离子方程式为
溶液发生反应的主要离子方程式为_______ 。
 ②
② ③
③ ④盐酸 ⑤
④盐酸 ⑤ ⑥
⑥
(1)属于弱电解质的是
(2)在氨水中存在电离平衡:
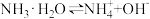 。将上述六种物质分别配成
。将上述六种物质分别配成 的溶液,向稀氨水中分别滴加少量六种溶液,能使氨水的电离平衡逆向移动且
的溶液,向稀氨水中分别滴加少量六种溶液,能使氨水的电离平衡逆向移动且 增大的是
增大的是

(3)等体积、pH相同的盐酸和醋酸分别与
 的
的 溶液恰好完全反应,消耗
溶液恰好完全反应,消耗 体积较大的是
体积较大的是 ”或“
”或“ ”),反应后溶液pH较大的是
”),反应后溶液pH较大的是 ”或“
”或“ ”)。
”)。(4)已知次氯酸
 的电离平衡常数为
的电离平衡常数为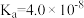 ,向
,向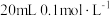 的
的 溶液中滴加少量硫酸,再加水稀释至
溶液中滴加少量硫酸,再加水稀释至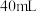 ,此时测得
,此时测得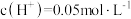 ,则溶液中
,则溶液中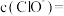
 。
。(5)已知亚硫酸
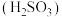 的电离平衡常数为
的电离平衡常数为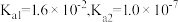 ;碳酸
;碳酸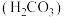 的电离平衡常数为
的电离平衡常数为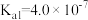 ,
,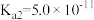 ,足量的
,足量的 溶液和
溶液和 溶液发生反应的主要离子方程式为
溶液发生反应的主要离子方程式为
更新时间:2022-11-05 09:38:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.现有下列物质:①酒精、② 溶液、③稀硫酸、④
溶液、③稀硫酸、④ 、⑤
、⑤ 固体、⑥铁、⑦小苏打、⑧淀粉溶液
固体、⑥铁、⑦小苏打、⑧淀粉溶液
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)②⑧两种分散系的本质区别是___________ 。
(3)为除去 溶液中的⑦,选用试剂为
溶液中的⑦,选用试剂为___________ (化学式),其中离子方程式为___________ 。
II.已知 能发生如下反应:
能发生如下反应: ,生成的
,生成的 可以使淀粉变蓝。
可以使淀粉变蓝。
(4)用双线桥标出该反应的电子转移方向和数目___________ 。
(5)HI在该反应中表现的性质是___________ ,反应中被还原的元素是___________ 。
III.某离子反应涉及到 、
、 、
、 、
、 、
、 、
、 等微粒,其中
等微粒,其中 、
、 的粒子数随时间变化的曲线如图所示。
的粒子数随时间变化的曲线如图所示。

(6)请写出该反应的离子方程式:___________ 。
 溶液、③稀硫酸、④
溶液、③稀硫酸、④ 、⑤
、⑤ 固体、⑥铁、⑦小苏打、⑧淀粉溶液
固体、⑥铁、⑦小苏打、⑧淀粉溶液(1)属于电解质的是
(2)②⑧两种分散系的本质区别是
(3)为除去
 溶液中的⑦,选用试剂为
溶液中的⑦,选用试剂为II.已知
 能发生如下反应:
能发生如下反应: ,生成的
,生成的 可以使淀粉变蓝。
可以使淀粉变蓝。(4)用双线桥标出该反应的电子转移方向和数目
(5)HI在该反应中表现的性质是
III.某离子反应涉及到
 、
、 、
、 、
、 、
、 、
、 等微粒,其中
等微粒,其中 、
、 的粒子数随时间变化的曲线如图所示。
的粒子数随时间变化的曲线如图所示。
(6)请写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】物质的分类、转化、化学计量在化学中占有重要地位。现有下列9种物质:①Cu②淀粉溶液③ ④
④ ⑤
⑤ ⑥
⑥ ⑦纯醋酸⑧
⑦纯醋酸⑧ 溶液⑨熔融的
溶液⑨熔融的 。根据所学知识回答下列问题:
。根据所学知识回答下列问题:
(1)以上能发生丁达尔效应的是___________ 。(填写序号,下同)
(2)属于强电解质的是___________ 。
(3)标准状况下,相同体积的④ 和⑤
和⑤ 原子个数之比为
原子个数之比为___________ 。
(4) 某硝酸盐
某硝酸盐 中含有
中含有 ,则该硝酸盐的摩尔质量为
,则该硝酸盐的摩尔质量为___________ 。
(5)实验室需要配制 的稀硫酸
的稀硫酸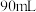 ,需量取质量分数为98%、密度为
,需量取质量分数为98%、密度为 的浓硫酸
的浓硫酸___________ mL,配制过程中所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器有___________ 。
 ④
④ ⑤
⑤ ⑥
⑥ ⑦纯醋酸⑧
⑦纯醋酸⑧ 溶液⑨熔融的
溶液⑨熔融的 。根据所学知识回答下列问题:
。根据所学知识回答下列问题:(1)以上能发生丁达尔效应的是
(2)属于强电解质的是
(3)标准状况下,相同体积的④
 和⑤
和⑤ 原子个数之比为
原子个数之比为(4)
 某硝酸盐
某硝酸盐 中含有
中含有 ,则该硝酸盐的摩尔质量为
,则该硝酸盐的摩尔质量为(5)实验室需要配制
 的稀硫酸
的稀硫酸 ,需量取质量分数为98%、密度为
,需量取质量分数为98%、密度为 的浓硫酸
的浓硫酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】H2C2O4为二元弱酸。回答下列问题:
(1)20℃时,配制一组c(H2C2O4)+c(HC2O4-)+ c(C2O42-)=0.100 mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如下图所示。
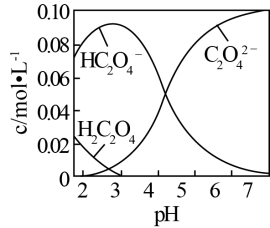
①H2C2O4的电离方程式为___________ 。
②为获得尽可能纯的NaHC2O4,pH应控制在_______ 左右。
③NaHC2O4溶液呈酸性,其原因为_________________ 。
④pH=6时,溶液中含碳微粒浓度大小关系为_______________ 。
(2)常温下,草酸、碳酸的电离平衡常数如下:
①常温下,0.1 mol·L-1 Na2CO3溶液的pH____ 0.1 mol·L-1 Na2C2O4溶液的pH。(填“>”、“<”或“=”)
② pH=4的H2C2O4溶液中c(C2O42-):c(HC2O4-)=_________ 。
(1)20℃时,配制一组c(H2C2O4)+c(HC2O4-)+ c(C2O42-)=0.100 mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如下图所示。

①H2C2O4的电离方程式为
②为获得尽可能纯的NaHC2O4,pH应控制在
③NaHC2O4溶液呈酸性,其原因为
④pH=6时,溶液中含碳微粒浓度大小关系为
(2)常温下,草酸、碳酸的电离平衡常数如下:
| 化学式 | H2CO3 | H2C2O4 |
| 平衡常数 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=5.6×10-2 Ka2=5.4×10-5 |
①常温下,0.1 mol·L-1 Na2CO3溶液的pH
② pH=4的H2C2O4溶液中c(C2O42-):c(HC2O4-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氰化氢是剧毒物质,含有氰的废水对环境的污染和人体的危害非常严重。
(1)氢氰酸(HCN)的电子式为______ 。
(2)用电解的方法可以除去含有CN-、Cl-废水中的CN-,其原理是控制溶液pH为9-10,利用阳极产生的ClO-将CN-氧化为两种无污染的气体。
①阳极的电极反应式:_________ 。
②除去CN-的离子方程式为:_________ 。
(3)已知25℃时,HCN的电离常数Ka=4.9×10-10,则25℃时0.1mol/L 的HCN溶液中c(H+)=_____ mol/L。NaCN溶液中加入盐酸至恰好完全反应,溶液中所有离子浓度的关系为___________ 。
(1)氢氰酸(HCN)的电子式为
(2)用电解的方法可以除去含有CN-、Cl-废水中的CN-,其原理是控制溶液pH为9-10,利用阳极产生的ClO-将CN-氧化为两种无污染的气体。
①阳极的电极反应式:
②除去CN-的离子方程式为:
(3)已知25℃时,HCN的电离常数Ka=4.9×10-10,则25℃时0.1mol/L 的HCN溶液中c(H+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某一元弱酸(用HA表示)在水中的电离方程式是HA H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向___________ (填“正”或“逆”)反应方向移动。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向___________ (填“正”或“逆”)反应方向移动,溶液中c(A-)将___________ (填“增大”“减小”或“不变”,下同),溶液中c(OH-)将___________ 。
(3)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c( )=c(Cl-),则溶液显
)=c(Cl-),则溶液显___________ 性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=___________
(4)①现有室温下pH均为5的 溶液和
溶液和 溶液。两种溶液中,
溶液。两种溶液中,
___________ 。
② 和
和 两种溶液中,由水电离出的
两种溶液中,由水电离出的 分别为
分别为___________ 、___________ 。
 H++A-,回答下列问题:
H++A-,回答下列问题:(1)向溶液中加入适量NaA固体,以上平衡将向
(2)若向溶液中加入适量NaCl溶液,以上平衡将向
(3)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c(
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(4)①现有室温下pH均为5的
 溶液和
溶液和 溶液。两种溶液中,
溶液。两种溶液中,
②
 和
和 两种溶液中,由水电离出的
两种溶液中,由水电离出的 分别为
分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】常温下,几种酸的电离平衡常数如下:
回答下列问题:
(1)物质的量浓度均为0.1 mol·L-1的①NaClO溶液②Na2CO3溶液③NaHCO3溶液④Na2SO3溶液,pH值由大到小的顺序是_____________________ 。(填序号)
(2))用离子方程式表示NaClO溶液呈碱性的原因________________ 。
(3)0.1mol/L的氯化铵溶液中各离子 物质的量浓度由大到小的顺序是_________________ ,只改变下列一个条件,能使c(NH4+)与c(Cl-)比值变大的是___________ (填标号)
A.加入固体硫酸铵 B.通入少量氯化氢
C.降低溶液温度 D.加入少量固体氢氧化钠
(4)假设25 ℃时,0.1mol/L氯化铵溶液由水电离出的氢离子浓度为1×10-6mol/L,则在该温度下此溶液中氨水的电离平衡常数:Kb(NH3·H2O)=________ 。
| 酸 | 电离方程式 | 电离平衡常数K |
| HClO | HClO H++ClO- H++ClO- | 3.0×10-8 |
| H2CO3 | H2CO3 H++ HCO3- H++ HCO3-HCO3-  H++ CO32- H++ CO32- | K1=4.4×10-7 K2=5.6×10-11 |
| H2SO3 | H2SO3 H++HSO3- H++HSO3-HSO3-  H++ SO32- H++ SO32- | K1=1.54×10-2 K2= 1.02×10-7 |
回答下列问题:
(1)物质的量浓度均为0.1 mol·L-1的①NaClO溶液②Na2CO3溶液③NaHCO3溶液④Na2SO3溶液,pH值由大到小的顺序是
(2))用离子方程式表示NaClO溶液呈碱性的原因
(3)0.1mol/L的氯化铵溶液中各
A.加入固体硫酸铵 B.通入少量氯化氢
C.降低溶液温度 D.加入少量固体氢氧化钠
(4)假设25 ℃时,0.1mol/L氯化铵溶液由水电离出的氢离子浓度为1×10-6mol/L,则在该温度下此溶液中氨水的电离平衡常数:Kb(NH3·H2O)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空:
(1)25℃,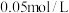 硫酸溶液中,酸电离出的
硫酸溶液中,酸电离出的 约为水电离出的
约为水电离出的 的
的______ 倍。
(2)25℃时,将 的稀硫酸
的稀硫酸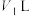 与
与 的苛性钠溶液
的苛性钠溶液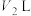 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则
___________ 。
(3)常温下,向 的乙酸溶液中加入少量蒸馏水稀释,则溶液中
的乙酸溶液中加入少量蒸馏水稀释,则溶液中 的数目将
的数目将________ , 将
将_________ (填“变大”、“变小”或“不变”)。
(4)室温时,碳酸的电离常数为 、
、 ,则当某溶液
,则当某溶液 时,
时,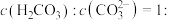
___________ ;已知次氯酸的电离平衡常数 和碳酸的电离平衡常数关系为
和碳酸的电离平衡常数关系为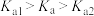 ,请写出向
,请写出向 溶液中通入少量
溶液中通入少量 的离子反应方程式
的离子反应方程式___________ 。
(5) 俗称大苏打,在与稀硫酸溶液混合时会产生沉淀及易溶于水的气体,该反应可用来探究化学反应速率的影响因素,请写出该化学反应方程式
俗称大苏打,在与稀硫酸溶液混合时会产生沉淀及易溶于水的气体,该反应可用来探究化学反应速率的影响因素,请写出该化学反应方程式___________ 。
(1)25℃,
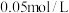 硫酸溶液中,酸电离出的
硫酸溶液中,酸电离出的 约为水电离出的
约为水电离出的 的
的(2)25℃时,将
 的稀硫酸
的稀硫酸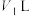 与
与 的苛性钠溶液
的苛性钠溶液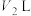 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则
(3)常温下,向
 的乙酸溶液中加入少量蒸馏水稀释,则溶液中
的乙酸溶液中加入少量蒸馏水稀释,则溶液中 的数目将
的数目将 将
将(4)室温时,碳酸的电离常数为
 、
、 ,则当某溶液
,则当某溶液 时,
时,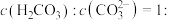
 和碳酸的电离平衡常数关系为
和碳酸的电离平衡常数关系为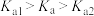 ,请写出向
,请写出向 溶液中通入少量
溶液中通入少量 的离子反应方程式
的离子反应方程式(5)
 俗称大苏打,在与稀硫酸溶液混合时会产生沉淀及易溶于水的气体,该反应可用来探究化学反应速率的影响因素,请写出该化学反应方程式
俗称大苏打,在与稀硫酸溶液混合时会产生沉淀及易溶于水的气体,该反应可用来探究化学反应速率的影响因素,请写出该化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知:25℃时,Ka(CH3COOH)=1.75×10-5,Ka(HClO)=2.95×10-8,Ka1(H2CO3)=4.30×10-7、Ka2(H2CO3)=5.61×10-11,Ka1(H2SO3)=1.54×10-2、Ka2(H2SO3)=1.02×10-7。回答下列问题:
(1)写出碳酸的第一步电离平衡常数表达式Ka1(H2CO3)=___________ 。
(2)在相同条件下,等pH的CH3COONa、NaClO、Na2CO3和Na2SO34种溶液中溶质浓度由大到小的顺序为___________ 。等物质的量浓度的Na2CO3和NaHCO3的混合溶液中各离子浓度由大到小的顺序为___________ 。
(3)若保持温度不变,在醋酸溶液中通入少量HCl,下列的量会变小的是___________ (填字母)。
a.c(CH3COO-) b.c(H+) c.
(4)下列离子方程式中书写错误的是___________ (填字母)。
a.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-= +2HClO
+2HClO
b.少量SO2通入Ca(ClO)2溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
c.少量Cl2通入Na2CO3溶液中:Cl2+2 +H2O=Cl-+2
+H2O=Cl-+2 +ClO-
+ClO-
(1)写出碳酸的第一步电离平衡常数表达式Ka1(H2CO3)=
(2)在相同条件下,等pH的CH3COONa、NaClO、Na2CO3和Na2SO34种溶液中溶质浓度由大到小的顺序为
(3)若保持温度不变,在醋酸溶液中通入少量HCl,下列的量会变小的是
a.c(CH3COO-) b.c(H+) c.

(4)下列离子方程式中书写错误的是
a.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-=
 +2HClO
+2HClOb.少量SO2通入Ca(ClO)2溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
c.少量Cl2通入Na2CO3溶液中:Cl2+2
 +H2O=Cl-+2
+H2O=Cl-+2 +ClO-
+ClO-
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】25℃时,草酸( )的
)的 ,
,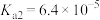 ;
; 的
的 ,
, 。回答下列问题:
。回答下列问题:
(1)写出 的第二步电离方程式
的第二步电离方程式___________ 。
(2)相同浓度的 、
、 、
、 、
、 四种溶液中碱性最弱的物质是
四种溶液中碱性最弱的物质是________ 溶液。用 的NaOH溶液滴定
的NaOH溶液滴定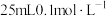 草酸溶液的滴定曲线如图所示。
草酸溶液的滴定曲线如图所示。
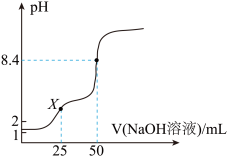
①X点溶液显___________ (填“酸性”“中性”或“碱性”),若向该溶液中滴加少量 ,反应的离子方程式为
,反应的离子方程式为___________ , 值
值___________ (填“增大”或“减小”)。
②滴定过程中所得混合溶液中 时,
时,
___________ 。
(3)反应 的平衡常数K的数量级为
的平衡常数K的数量级为___________ 。
 )的
)的 ,
,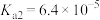 ;
; 的
的 ,
, 。回答下列问题:
。回答下列问题:(1)写出
 的第二步电离方程式
的第二步电离方程式(2)相同浓度的
 、
、 、
、 、
、 四种溶液中碱性最弱的物质是
四种溶液中碱性最弱的物质是 的NaOH溶液滴定
的NaOH溶液滴定 草酸溶液的滴定曲线如图所示。
草酸溶液的滴定曲线如图所示。
①X点溶液显
 ,反应的离子方程式为
,反应的离子方程式为 值
值②滴定过程中所得混合溶液中
 时,
时,
(3)反应
 的平衡常数K的数量级为
的平衡常数K的数量级为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题。
(1)若纯水在100℃时 ,该温度下
,该温度下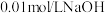 溶液的
溶液的
___________ 。
(2)25℃时,向水中加入少量碳酸钠固体,得到 为11的溶液,碳酸钠水解的离子方程式为
为11的溶液,碳酸钠水解的离子方程式为___________ ,由水电离出的
___________  。
。
(3)体积均为 、
、 均为2的盐酸与一元酸
均为2的盐酸与一元酸 ,加水稀释过程中
,加水稀释过程中 与溶液体积的关系如图所示,则
与溶液体积的关系如图所示,则 是
是___________ (填“强酸”或“弱酸”),理由是___________ 。

(4)电离平衡常数是衡量弱电解质电离强弱的物理量。已知:
①25℃时,等浓度的 溶液、
溶液、 溶液和
溶液和 溶液,其溶液的
溶液,其溶液的 由大到小的顺序为
由大到小的顺序为___________ 。
②25℃时,在 的醋酸溶液中由醋酸电离出的
的醋酸溶液中由醋酸电离出的 约是由水电离出的
约是由水电离出的 的
的_____ 倍。
(1)若纯水在100℃时
 ,该温度下
,该温度下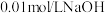 溶液的
溶液的
(2)25℃时,向水中加入少量碳酸钠固体,得到
 为11的溶液,碳酸钠水解的离子方程式为
为11的溶液,碳酸钠水解的离子方程式为
 。
。(3)体积均为
 、
、 均为2的盐酸与一元酸
均为2的盐酸与一元酸 ,加水稀释过程中
,加水稀释过程中 与溶液体积的关系如图所示,则
与溶液体积的关系如图所示,则 是
是
(4)电离平衡常数是衡量弱电解质电离强弱的物理量。已知:
| 化学式 | 电离常数( ) ) |
 | 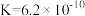 |
 | 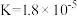 |
 | 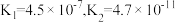 |
 溶液、
溶液、 溶液和
溶液和 溶液,其溶液的
溶液,其溶液的 由大到小的顺序为
由大到小的顺序为②25℃时,在
 的醋酸溶液中由醋酸电离出的
的醋酸溶液中由醋酸电离出的 约是由水电离出的
约是由水电离出的 的
的
您最近一年使用:0次