碳元素在自然界中分布很广,是存在形式最复杂的元素。实验室可用邻二氮菲(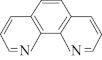 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
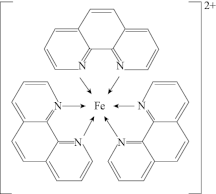
回答下列问题:
(1)基态Fe原子的价层电子排布式为_______ 。
(2)红色配合物中非金属元素的电负性从大到小的顺序为_______ 。
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为_______ 、_______ 。
(4)红色配合物的中心原子的配位数为_______ 。
(5)红色配合物中不存在的作用力有_______ 。
A.σ键 B.π键 C.离子键 D.氢键 E.配位键
(6)科学家合成了硬度超过金刚石的 晶体,该晶体的硬度比金刚石大的原因是:
晶体,该晶体的硬度比金刚石大的原因是:_______ 。C、N、O三种元素第一电离能从大到小的顺序为:_______ (用元素符号回答)。
 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
回答下列问题:
(1)基态Fe原子的价层电子排布式为
(2)红色配合物中非金属元素的电负性从大到小的顺序为
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为
(4)红色配合物的中心原子的配位数为
(5)红色配合物中不存在的作用力有
A.σ键 B.π键 C.离子键 D.氢键 E.配位键
(6)科学家合成了硬度超过金刚石的
 晶体,该晶体的硬度比金刚石大的原因是:
晶体,该晶体的硬度比金刚石大的原因是:
更新时间:2022-11-17 08:24:55
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数相等。已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学程式是___________________________________
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:___________________________________
(3)在一定条件下,甲与O2反应的化学方程式是_______________________
(4)丁的元素符号是_________ ,它的核外电子排布式为 _______________________
(5)丁的氧化物的晶体结构与_________________ 的晶体结构相似。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学程式是
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:
(3)在一定条件下,甲与O2反应的化学方程式是
(4)丁的元素符号是
(5)丁的氧化物的晶体结构与
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac。请回答下列问题:
(1)C、N、O的电负性由大到小的顺序为________ 。
(2)写出Cu的核外电子排布式________ 。
(3)化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为________ 。
(4)在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为________ ;1mol尿素分子中,σ 键的数目为________ 。
(1)C、N、O的电负性由大到小的顺序为
(2)写出Cu的核外电子排布式
(3)化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为
(4)在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】2022年北京冬奥会实现了100%的绿电供应,充分利用了电动汽车和氢燃料汽车等先进技术,基本实现了碳中和,下面是几种储氢材料,回答下面问题:
(1) 是一种白色粉末,与水发生反应:
是一种白色粉末,与水发生反应: ↑。
↑。
①上述反应中含有离子键的化合物是___________ (填化学式)。
②写出基态 原子最高能层符号
原子最高能层符号___________ ,最高能级符号___________ 。基态O原子最高能级含有___________ 个电子。
(2) 和
和 也是很好的储氢材料。
也是很好的储氢材料。
①基态 原子核外电子的空间运动状态(原子轨道)有
原子核外电子的空间运动状态(原子轨道)有___________ 种。
②基态 原子的电子排布式
原子的电子排布式___________ ,基态 原子的价层电子排布式
原子的价层电子排布式___________ , 和
和 都处于元素周期表的
都处于元素周期表的___________ 区。
(3)金属氨络合物储氢材料 和
和 是研究的热点。
是研究的热点。
①基态S原子最高能级上最多有___________ 个电子顺时针旋转。
②氮元素与氧元素的第一电离能较高的是___________ (填元素符号)。
③Cl-和S2-的还原性比较,还原性较强的是___________ (填离子符号)。
(1)
 是一种白色粉末,与水发生反应:
是一种白色粉末,与水发生反应: ↑。
↑。①上述反应中含有离子键的化合物是
②写出基态
 原子最高能层符号
原子最高能层符号(2)
 和
和 也是很好的储氢材料。
也是很好的储氢材料。①基态
 原子核外电子的空间运动状态(原子轨道)有
原子核外电子的空间运动状态(原子轨道)有②基态
 原子的电子排布式
原子的电子排布式 原子的价层电子排布式
原子的价层电子排布式 和
和 都处于元素周期表的
都处于元素周期表的(3)金属氨络合物储氢材料
 和
和 是研究的热点。
是研究的热点。①基态S原子最高能级上最多有
②氮元素与氧元素的第一电离能较高的是
③Cl-和S2-的还原性比较,还原性较强的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为_______ 。
(2) 的沸点低于
的沸点低于 ,其原因是
,其原因是_______ 。
(3)关于I~III三种反应物,下列说法正确的有_______ 。
A.I中仅有 键
键
B.I中的 键为非极性共价键
键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______ 。
(5)硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为_______ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。_______ 。
②设X的最简式的式量为 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为_______  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: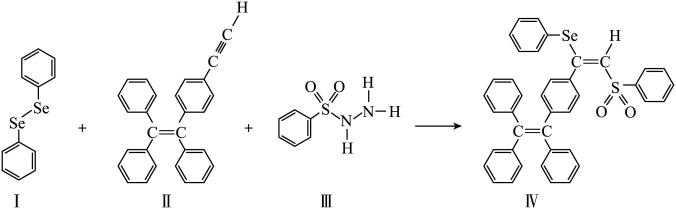
 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为(2)
 的沸点低于
的沸点低于 ,其原因是
,其原因是(3)关于I~III三种反应物,下列说法正确的有
A.I中仅有
 键
键B.I中的
 键为非极性共价键
键为非极性共价键C.II易溶于水
D.II中原子的杂化轨道类型只有
 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有
(5)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
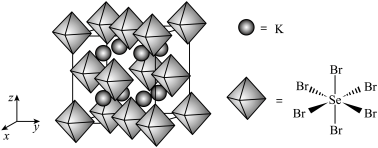
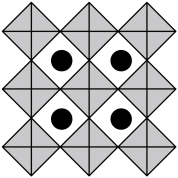
②设X的最简式的式量为
 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
【推荐2】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大,A元素的价层电子排布式为 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)D、C两种元素形成的化合物的电子式为___________ 。
(2)A、B、C三种元素的电负性由小到大的顺序为___________ (用元素符号表示)。
(3)C元素的电子排布图为___________ 。
(4)E元素位于元素周期表的第___________ 族,形成的离子中较稳定的离子的价层电子排布式是___________ 。
(5)F元素位于元素周期表的___________ 区,B元素原子核外占据最高能级的电子云轮廓图是___________ 形。
(6)G可能的性质有___________(填字母)。
 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)D、C两种元素形成的化合物的电子式为
(2)A、B、C三种元素的电负性由小到大的顺序为
(3)C元素的电子排布图为
(4)E元素位于元素周期表的第
(5)F元素位于元素周期表的
(6)G可能的性质有___________(填字母)。
| A.其最高价氧化物对应水化物是弱酸 | B.其第一电离能小于磷小于硒 |
| C.其原子半径大于锗 | D.氢化物的稳定性G大于A |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】北京化工大学杨占旭教授合成了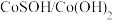 复合催化剂,其在低温条件下能催化水分解制氢,有利于拯救能源危机和缓解环境恶化,其工作原理如图所示。
复合催化剂,其在低温条件下能催化水分解制氢,有利于拯救能源危机和缓解环境恶化,其工作原理如图所示。
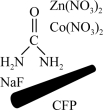
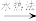
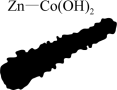

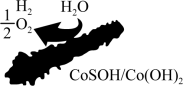
回答下列问题:
(1)基态Co原子的电子排布式为___________ ,其能量最高的能级是___________
(2)Cu的第三电离能比Zn的小,其原因是___________ ;C、N、O、F的电负性由大到小的顺序为___________ 。
(3)尿素可看作是氨基甲酰胺,有一定的弱碱性,其与 、
、 等作用时,生成难溶于水的盐:
等作用时,生成难溶于水的盐: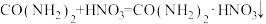 。
。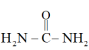 中碳原子的杂化方式是
中碳原子的杂化方式是___________ ,该分子中含有___________ 个σ键。
(4) 的键角
的键角___________ (填“大于”或“小于”) 的键角,其原因为
的键角,其原因为___________ 。
(5)金属锌的晶胞结构如图所示。

①Zn原子的配位数为___________ ;
②该晶体的密度为___________ g/cm3 (列出算式)。
 复合催化剂,其在低温条件下能催化水分解制氢,有利于拯救能源危机和缓解环境恶化,其工作原理如图所示。
复合催化剂,其在低温条件下能催化水分解制氢,有利于拯救能源危机和缓解环境恶化,其工作原理如图所示。



回答下列问题:
(1)基态Co原子的电子排布式为
(2)Cu的第三电离能比Zn的小,其原因是
(3)尿素可看作是氨基甲酰胺,有一定的弱碱性,其与
 、
、 等作用时,生成难溶于水的盐:
等作用时,生成难溶于水的盐: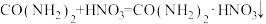 。
。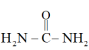 中碳原子的杂化方式是
中碳原子的杂化方式是(4)
 的键角
的键角 的键角,其原因为
的键角,其原因为(5)金属锌的晶胞结构如图所示。

①Zn原子的配位数为
②该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】A.[物质结构与性质]
Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为____ 。
(2) 的空间构型为
的空间构型为____ (用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为____ (填元素符号)。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为____ ;推测抗坏血酸在水中的溶解性:____ (填“难溶于水”或“易溶于水”)。
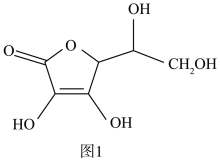
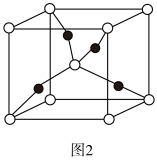
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为____ 。
Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为
(2)
 的空间构型为
的空间构型为(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为


(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】碳及其化合物有许多用途。回答下列问题:
⑴碳元素有12C、13C和14C等核素。下列对12C基态原子结构的表示方法中,对电子运动状态描述最详尽的是_______ (填标号)。
A.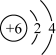 B.
B.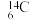
C.1s22s22p2 D.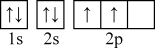
基态13C原子核外有________ 种不同空间运动状态的电子。
⑵K3[Fe(CN)6]晶体中Fe3+与CN-之间的化学键的类型为________ ,该化学键能够形成的原因是________ 。
⑶有机物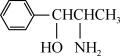 是
是________ (填“极性”或“非极性”)分子;该有机物中存在sp3杂化的原子,其对应元素的第一电离能由大到小的顺序为________ 。
⑷乙二胺(H2NCH2CH2NH2)和三甲胺[N(CH3)3]均属于胺,两者相对分子质量接近,但乙二胺比三甲胺的沸点高得多,原因是________ 。
⑸碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和金属阳离子半径:
随着金属阳离子半径的增大,碳酸盐的热分解温度逐步升高,原因是________ 。
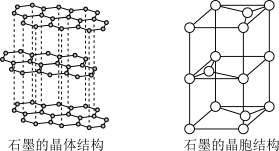
⑹石墨的晶体结构和晶胞结构如图所示。已知石墨的密度为ρg∙cm-3,C—C键长为γ cm,阿伏加 德罗常数的值为NA,则石墨晶体的层间距为________ cm。
⑴碳元素有12C、13C和14C等核素。下列对12C基态原子结构的表示方法中,对电子运动状态描述最详尽的是
A.
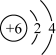 B.
B.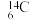
C.1s22s22p2 D.

基态13C原子核外有
⑵K3[Fe(CN)6]晶体中Fe3+与CN-之间的化学键的类型为
⑶有机物
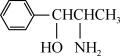 是
是⑷乙二胺(H2NCH2CH2NH2)和三甲胺[N(CH3)3]均属于胺,两者相对分子质量接近,但乙二胺比三甲胺的沸点高得多,原因是
⑸碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和金属阳离子半径:
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 金属阳离子半径/pm | 66 | 99 | 112 | 135 |
随着金属阳离子半径的增大,碳酸盐的热分解温度逐步升高,原因是
⑹石墨的晶体结构和晶胞结构如图所示。已知石墨的密度为ρg∙cm-3,C—C键长为γ cm,阿伏加 德罗常数的值为NA,则石墨晶体的层间距为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】当今社会,各国治理污染的压力都很大,如何变废为宝,合理利用资源,是摆在科学家面前的课题。科学家设计在催化剂表面利用 还原氮的氧化物的一种反应机理如图所示。
还原氮的氧化物的一种反应机理如图所示。
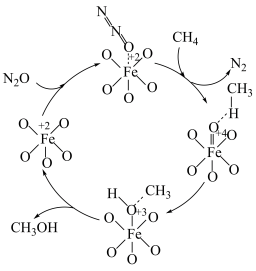
回答下列问题:
(1)基态Fe原子与基态 离子中未成对的电子数之比为
离子中未成对的电子数之比为__________ 。
(2)第二周期第一电离能比N大的主族元素为__________ (填化学式)。上述历程中涉及反应的非金属电负性由大到小的顺序为__________ (填化学式)。
(3)硝酸根离子的空间构型为__________ ,其中N的杂化轨道类型为__________ 。
(4) 中化学键类型有
中化学键类型有______ (填选项字母),甲醇易溶于水的原因是__________ 。
A.非极性共价键 B.氢键 C. 键 D.极性共价键
键 D.极性共价键
(5)铁的晶胞类型有多种,其中图甲中与一个铁原子等距离且最近的铁原子有_______ 个,图乙所示晶胞的密度为__________  (用含有a、
(用含有a、 的代数式表示)。
的代数式表示)。

 还原氮的氧化物的一种反应机理如图所示。
还原氮的氧化物的一种反应机理如图所示。
回答下列问题:
(1)基态Fe原子与基态
 离子中未成对的电子数之比为
离子中未成对的电子数之比为(2)第二周期第一电离能比N大的主族元素为
(3)硝酸根离子的空间构型为
(4)
 中化学键类型有
中化学键类型有A.非极性共价键 B.氢键 C.
 键 D.极性共价键
键 D.极性共价键(5)铁的晶胞类型有多种,其中图甲中与一个铁原子等距离且最近的铁原子有
 (用含有a、
(用含有a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
【推荐1】金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:
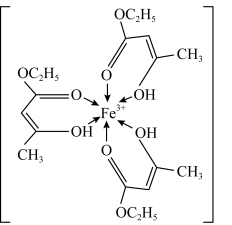
①基态铁离子的核外电子填充在___________ 个原子轨道中;
②此配离子中碳原子的杂化轨道类型为___________ ;
③此配离子中含有的化学键类型为___________ 。
A.离子键 B.金属键 C.共价键 D.配位键 E.σ键 F.π键
(2) 与钴盐形成的配离子
与钴盐形成的配离子 可用于检验
可用于检验 的存在。
的存在。 离子的VSEPR模型名称为
离子的VSEPR模型名称为___________ 。
(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物 和
和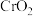 ,其中适合作录音带磁粉原料的是
,其中适合作录音带磁粉原料的是___________ 。
(4)锰的一种配合物的化学式为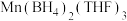 。已知:原子个数和价电子总数分别对应相等的分子、离子或基团称为等电子体。请写出两种与
。已知:原子个数和价电子总数分别对应相等的分子、离子或基团称为等电子体。请写出两种与 互为等电子体的微粒
互为等电子体的微粒___________ (请写出一个分子和一个离子)。
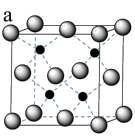
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为___________ ,已知晶胞密度为ρg/cm ,用
,用 表示阿伏加德罗常数的值,则晶胞的边长为
表示阿伏加德罗常数的值,则晶胞的边长为___________ cm(列计算式)。
(1)三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

①基态铁离子的核外电子填充在
②此配离子中碳原子的杂化轨道类型为
③此配离子中含有的化学键类型为
A.离子键 B.金属键 C.共价键 D.配位键 E.σ键 F.π键
(2)
 与钴盐形成的配离子
与钴盐形成的配离子 可用于检验
可用于检验 的存在。
的存在。 离子的VSEPR模型名称为
离子的VSEPR模型名称为(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物
 和
和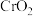 ,其中适合作录音带磁粉原料的是
,其中适合作录音带磁粉原料的是(4)锰的一种配合物的化学式为
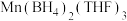 。已知:原子个数和价电子总数分别对应相等的分子、离子或基团称为等电子体。请写出两种与
。已知:原子个数和价电子总数分别对应相等的分子、离子或基团称为等电子体。请写出两种与 互为等电子体的微粒
互为等电子体的微粒(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为
 ,用
,用 表示阿伏加德罗常数的值,则晶胞的边长为
表示阿伏加德罗常数的值,则晶胞的边长为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】铁、钴及其化合物在生活、生产中用途广泛。请回答下列问题:
(1)基态Fe2+的核外电子排布式为_______ ;第四周期元素中,基态原子未成对电子数与Co相等的有_______ (填元素符号)。
(2)CoCl3在氨水中能形成多种配合物。取1molCoCl3·4NH3,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为_______ 。
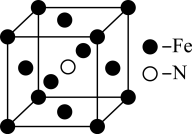
(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为_______ 。
(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,设NA为阿伏加德罗常数的值,钴蓝晶体的密度为_______ g/cm3(列计算式)。

(1)基态Fe2+的核外电子排布式为
(2)CoCl3在氨水中能形成多种配合物。取1molCoCl3·4NH3,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为
(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为

(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,设NA为阿伏加德罗常数的值,钴蓝晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。回答下列问题:
(1)镍元素在周期表中的位置为___________ ,基态镍原子未成对电子数为___________ 。
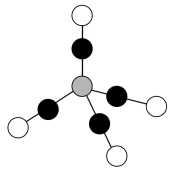
(2)区分晶体和非晶体最可靠的科学方法为___________ ;配合物Ni(CO)4熔点−19.3℃,沸点42.1℃,难溶于水,易溶于有机溶剂,结构见下图,则固态Ni(CO)4属于___________ 晶体,1mol Ni(CO)4含有___________ mol配位键。
(3)NiO的晶体结构类型与NaCl相似,离子半径如下表所示:NiO晶胞中Ni2+的配位数为____ ,NiO的熔点比NaCl高的原因是______ 。
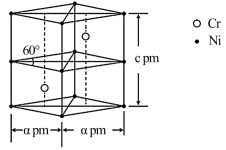
(4)某铬镍合金晶胞如图所示,Cr、Ni原子个数比为__ ,该晶胞中Cr、Ni原子最近距离为__ pm(用含a、c的代数式表示)。
(1)镍元素在周期表中的位置为
(2)区分晶体和非晶体最可靠的科学方法为

(3)NiO的晶体结构类型与NaCl相似,离子半径如下表所示:NiO晶胞中Ni2+的配位数为
| Na+ | 102pm | Cl- | 181pm |
| Ni2+ | 69pm | O2− | 140pm |

您最近一年使用:0次



