反应mX(g) nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中,物质Y的体积分数随压强变化的曲线如图所示。下列说法正确的是
nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中,物质Y的体积分数随压强变化的曲线如图所示。下列说法正确的是
 nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中,物质Y的体积分数随压强变化的曲线如图所示。下列说法正确的是
nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中,物质Y的体积分数随压强变化的曲线如图所示。下列说法正确的是
| A.该反应的ΔH<0 |
| B.m>n+p |
| C.A、C两点化学平衡常数:KA<KC |
| D.B、C两点的反应速率v(B)<v(C) |
更新时间:2022-11-26 16:42:52
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】焦炉煤气(主要成分:CH4、CO2、H2、CO)在炭催化下,使CH4与CO2重整生成H2和CO。其主要反应为
反应I:

反应II:

反应III:

反应IV:

在1×105Pa、将焦炉煤气以一定流速通过装有炭催化剂的反应管,CH4、CO、H2的相对体积和CO2的转化率随温度变化的曲线如图所示。 、
、
相对体积
下列说法不正确的是
反应I:


反应II:


反应III:


反应IV:


在1×105Pa、将焦炉煤气以一定流速通过装有炭催化剂的反应管,CH4、CO、H2的相对体积和CO2的转化率随温度变化的曲线如图所示。

 、
、相对体积

下列说法不正确的是
| A.温度低于900℃,反应I基本不发生 |
| B.850℃~900℃时,主要发生反应Ⅳ |
| C.增大焦炉煤气流速一定能提高CO的相对体积 |
| D.工业生产上需要研发低温下CH4转化率高的催化剂 |
您最近一年使用:0次
【推荐2】恒容条件下,1molSiHCl3发生如下反应:2SiHCl3(g)⇌SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)·x(SiCl4),k正、k逆分别为正、逆反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
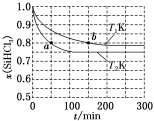

| A.该反应为放热反应,v正,a<v逆,b |
| B.化学平衡状态时,2v消耗(SiHCl3)=v消耗(SiCl4) |
C.当反应进行到a点时, = =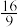 |
| D.T2K时,平衡体系中再充入1molSiHCl3,平衡正向移动,x(SiH2Cl2)增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在一定温度下的密闭容器中,加入1 mol CO和1 mol H2O发生反应:CO(g)+H2O(g) CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的
 CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的| A.在该温度下平衡常数K=1 | B.平衡常数与反应温度无关 |
| C.CO的转化率为50% | D.其他条件不变,改变压强平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在容积为 的恒容密闭容器中充入
的恒容密闭容器中充入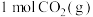 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应: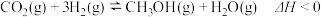 。反应进行
。反应进行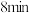 时达到平衡状态,测得
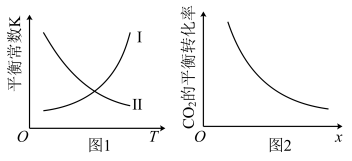
时达到平衡状态,测得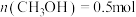 。该反应的平衡常数K与温度T的关系如图1所示,
。该反应的平衡常数K与温度T的关系如图1所示, 的平衡转化率如图2所示,下列说法错误的是
的平衡转化率如图2所示,下列说法错误的是
 的恒容密闭容器中充入
的恒容密闭容器中充入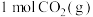 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应: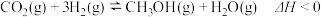 。反应进行
。反应进行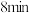 时达到平衡状态,测得
时达到平衡状态,测得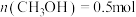 。该反应的平衡常数K与温度T的关系如图1所示,
。该反应的平衡常数K与温度T的关系如图1所示, 的平衡转化率如图2所示,下列说法错误的是
的平衡转化率如图2所示,下列说法错误的是
| A.在图1中,曲线Ⅱ表示该反应的平衡常数K与温度T的关系 |
B.该温度下,平衡常数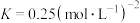 |
C.在其他条件不变的情况下,图2中x可表示温度、压强或 和 和 的投料比 的投料比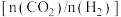 |
D.用二氧化碳合成甲醇体现了 减排理念 减排理念 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
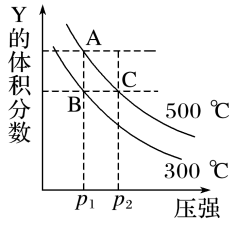
【推荐1】可逆反应mA(s)+nB(g) pC(g)在一定条件下达到平衡后,改变压强,B的体积分数φ (B)与压强的关系如图所示,下列有关叙述正确的是
pC(g)在一定条件下达到平衡后,改变压强,B的体积分数φ (B)与压强的关系如图所示,下列有关叙述正确的是
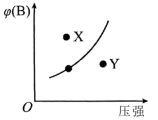
 pC(g)在一定条件下达到平衡后,改变压强,B的体积分数φ (B)与压强的关系如图所示,下列有关叙述正确的是
pC(g)在一定条件下达到平衡后,改变压强,B的体积分数φ (B)与压强的关系如图所示,下列有关叙述正确的是
| A.m+n<p |
| B.加入物质A,B的转化率增大,A的转化率减小 |
| C.X点时,v(正)>v(逆) |
| D.X点比Y点的平衡常数大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
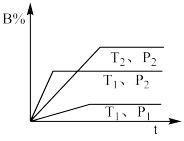
【推荐2】在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g)⇌xC(g),符合如图所示的关系(C%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )
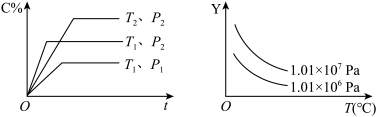

| A.反应物A的百分含量 | B.平衡混合气体中物质B的百分含量 |
| C.平衡混合气体的密度 | D.平衡混合气体的平均摩尔质量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在2 L的恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g) + O2(g) 2SO3(g),下列有关说法正确的是( )
2SO3(g),下列有关说法正确的是( )
 2SO3(g),下列有关说法正确的是( )
2SO3(g),下列有关说法正确的是( )A.由图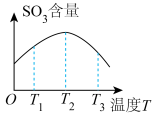 可知:该反应的△H<0 可知:该反应的△H<0 |
B.在图 中的t1时充入少量氩气,容器内压强增大,平衡右移 中的t1时充入少量氩气,容器内压强增大,平衡右移 |
C.图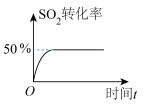 所示条件下,平衡常数为2 所示条件下,平衡常数为2 |
D.图 中的y可以表示平衡常数或混合气体平均摩尔质量 中的y可以表示平衡常数或混合气体平均摩尔质量 |
您最近一年使用:0次