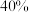在一定温度下的密闭容器中,加入1 mol CO和1 mol H2O发生反应:CO(g)+H2O(g) CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的
 CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的| A.在该温度下平衡常数K=1 | B.平衡常数与反应温度无关 |
| C.CO的转化率为50% | D.其他条件不变,改变压强平衡不移动 |
11-12高三上·辽宁·期中 查看更多[9]
江苏省徐州市睢宁县第一中学2021-2022学年高二下学期第一次月考化学试题陕西省咸阳市泾干中学2021-2022学年高二上学期第二次月考化学试题北京市延庆区2019-2020学年高二下学期期末考试化学试题湖南省娄底市第四中学2018-2019学年高二上学期10月月考化学试题浙江省诸暨市牌头中学2017-2018学年高一下学期期中考试(A)化学试题(已下线)2012届辽宁省辽南协作体高三上学期期中考试化学试卷2016-2017学年河南省师大附中高二上期中化学试卷(已下线)2013-2014河南师大附中第一学期期中考试高二化学试卷(已下线)2011-2012学年陕西省师大附中高一下学期期末考试化学试卷
更新时间:2016-11-14 16:38:45
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某恒定温度下,在一个2L的密闭容器中充入A气体,B气体,测得其浓度分别为2mol/L和1mol/L,且发生如下反应:3A(g)+2B(g) 4C(?)+2D(?)已知“?”代表C、D状态未确定;2min后达到平衡,测得生成1.6molC,且反应前后压强比为5:4,则下列说法中正确的是
4C(?)+2D(?)已知“?”代表C、D状态未确定;2min后达到平衡,测得生成1.6molC,且反应前后压强比为5:4,则下列说法中正确的是
①该反应用C表示反应速率为1.2mol/(L•min)
②此时B的转化率为35%
③增大该体系压强,平衡向右移动,但化学平衡常数不变
④增加C的量,A、B转化率不变
 4C(?)+2D(?)已知“?”代表C、D状态未确定;2min后达到平衡,测得生成1.6molC,且反应前后压强比为5:4,则下列说法中正确的是
4C(?)+2D(?)已知“?”代表C、D状态未确定;2min后达到平衡,测得生成1.6molC,且反应前后压强比为5:4,则下列说法中正确的是①该反应用C表示反应速率为1.2mol/(L•min)
②此时B的转化率为35%
③增大该体系压强,平衡向右移动,但化学平衡常数不变
④增加C的量,A、B转化率不变
| A.①② | B.②③ | C.①④ | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列因素一定能引起化学平衡移动的是
| A.化学反应速率发生变化 | B.反应体系达到平衡后,改变压强 |
| C.反应体系的温度发生变化 | D.反应物或生成物的浓度发生变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知FeCl3溶液与KSCN溶液混合后发生反应FeCl3+3KSCN Fe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是
Fe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是
 Fe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是
Fe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是| A.向溶液中加入少许KC1固体,溶液颜色变浅 |
| B.升高温度,平衡一定发生移动 |
| C.加入少许KC1固体或者加入少许FeCl3固体平衡常数均发生变化,且变化方向相反 |
| D.平衡常数表达式为K=c[Fe(SCN)3]·c3(KCl)/[c(FeCl3)·c3(KSCN)] |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】甲醇是容易输送的清洁燃料,可以单独与汽油混合作为汽车燃料,应用前景广阔。恒容密闭容器内发生反应如下:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。如图研究温度对甲醇产率的影响如图,下列说法不正确的是
CH3OH(g)+H2O(g)。如图研究温度对甲醇产率的影响如图,下列说法不正确的是

 CH3OH(g)+H2O(g)。如图研究温度对甲醇产率的影响如图,下列说法不正确的是
CH3OH(g)+H2O(g)。如图研究温度对甲醇产率的影响如图,下列说法不正确的是
| A.平衡后体系内加入CO2 ,平衡正向移动,H2转化率增大 |
| B.正反应放热 |
| C.缩小体积,增大压强,CH3OH的体积分数增大 |
| D.使用催化剂,平衡常数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】SiHCl3被应用于制造多晶硅及硅烷偶联剂等领域。50℃时将nmolSiHCl3置于密闭容器中发生如下反应: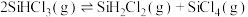 ,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是
,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是
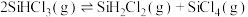 ,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是
,SiHCl3的转化率随时间变化的曲线如下图所示。下列说法正确的是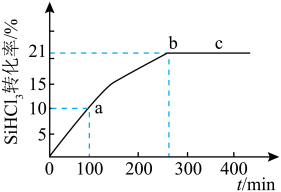
| A.SiH2Cl2和SiCl4均为由极性键构成的非极性分子 |
B.0~100min内,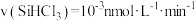 |
C.50℃时该反应的平衡常数 |
| D.b-c段平均速率大于a-b段平均速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,在三个体积均为1L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g)。下列说法正确的是
CH3OCH3(g)+H2O(g)。下列说法正确的是
 CH3OCH3(g)+H2O(g)。下列说法正确的是
CH3OCH3(g)+H2O(g)。下列说法正确的是| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| ① | 387 | 0.20 | 0.080 | 0.080 |
| ② | 387 | 0.40 | ||
| ③ | 207 | 0.20 | 0.090 | 0.090 |
| A.该反应的正反应为放热反应 |
| B.达到平衡时,容器①中的CH3OH体积分数比容器②中的小 |
| C.若容器①中反应达到平衡时增大压强,则各物质浓度保持不变 |
| D.若起始向容器①中充入CH3OH0.10mol、CH3OCH30.10mol、H2O0.10mol,则反应将向正反应方向进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】800℃时,可逆反应CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数K=1。800℃时,测得某一时刻密闭容器中各组分的物质的量如表,下列说法正确的是
CO2(g)+H2(g)的平衡常数K=1。800℃时,测得某一时刻密闭容器中各组分的物质的量如表,下列说法正确的是
 CO2(g)+H2(g)的平衡常数K=1。800℃时,测得某一时刻密闭容器中各组分的物质的量如表,下列说法正确的是
CO2(g)+H2(g)的平衡常数K=1。800℃时,测得某一时刻密闭容器中各组分的物质的量如表,下列说法正确的是| 物质 | CO | H2O | CO2 | H2 |
| 物质的量(mol) | 0.02 | 0.03 | 0.025 | 0.025 |
| A.此时,反应已达到平衡状态 |
| B.因为没有容器体积,无法判断反应进行的方向 |
| C.若维持温度不变,一段时间后,H2O的体积分数增加 |
| D.若维持温度不变,一段时间后,正反应速率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g)⇌COS(g)+H2O(g)△H=﹣Q kJ•mol﹣1 (Q>0)。在温度为T1时,将0.10molCO2与0.40mol H2S充入2.5L 的空钢瓶中,经过4min反应达到平衡,平衡时H2O(g)的物质的量分数为 2%,则下列说法不正确的是
| A.0~4 min内用H2S表示该反应的速率为0.001 mol•L﹣1•min﹣1 |
| B.CO2的平衡转化率α=2.5% |
| C.上述条件下反应达到平衡时放出的热量为0.01Q kJ |
| D.其他条件不变,若该反应在温度为T2 条件下进行,达到平衡所需时间小于4 min,则 T1<T2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是

 CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
| A.该反应的ΔH<0 |
| B.在500℃条件下达平衡时CO 的转化率为60% |
| C.平衡常数K1(3000C)<K2(5000C) |
| D.图2中达化学平衡的点为c、d、e |
您最近一年使用:0次

 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是 在
在 溶液中存在下列平衡:
溶液中存在下列平衡: ,某
,某 混合溶液中,
混合溶液中, 的物质的量浓度
的物质的量浓度 与温度T的关系如图所示(曲线上任何一点都表示平衡状态),下列说法正确的是
与温度T的关系如图所示(曲线上任何一点都表示平衡状态),下列说法正确的是
 的
的
 大
大 ,反应的平衡常数分别为
,反应的平衡常数分别为 ,则
,则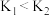
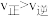
 和
和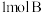 充入容积为
充入容积为 的密闭容器中,发生
的密闭容器中,发生 反应。
反应。 末测得此时容器中
末测得此时容器中 和
和 的浓度分别为
的浓度分别为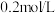 和
和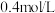 。下列叙述正确的是
。下列叙述正确的是
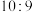
 内
内 和
和 的转化率均为
的转化率均为