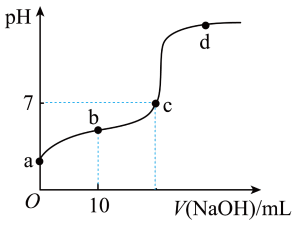
25℃时,向20mL0.1mol/L 溶液中逐滴加入0.1mo/L NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化关系如图所示。下列说法错误的是
溶液中逐滴加入0.1mo/L NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化关系如图所示。下列说法错误的是
 溶液中逐滴加入0.1mo/L NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化关系如图所示。下列说法错误的是
溶液中逐滴加入0.1mo/L NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化关系如图所示。下列说法错误的是
| A.a点的pH>1 |
| B.c点时,V(NaOH)=20mL |
C.反应过程中 的值逐渐减小 的值逐渐减小 |
| D.a、b、c点溶液中,水的电离程度逐渐增大 |
更新时间:2022-11-12 18:56:31
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】下列各溶液中,微粒的物质的量浓度关系正确的是
| A.0.1 mol·L-1 Na2CO3溶液:c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3) |
| B.0.1 mol·L-1 NH4Cl溶液:c(NH4+)=c(Cl-) |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+) > c(CH3COO-) > c(H+) > c(OH-) |
| D.常温下,将pH=2的盐酸和pH=12的氨水等体积混合后:c(NH4+) > c(Cl-) > c(OH-) > c(H+) |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】常温下有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的HCl溶液;③pH=11的氨水;④pH=11的NaOH溶液。下列说法正确的是
| A.①与②中c(H+)相同 |
| B.①与④混合,所得混合液的pH等于7 |
| C.②和③混合,所得混合溶液的pH大于7 |
| D.③与④分别用等浓度的盐酸中和,消耗盐酸的体积相等 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.室温下, 的 的 溶液中H+的数目为 溶液中H+的数目为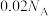 |
| B.室温下,1L pH=13的NaOH溶液中,由水电离的OH-数目为10-13 NA |
| C.1L 0.1mol/LFe2(SO4)3溶液中,Fe3+的数目为0.2NA |
| D.1L 1mol/L的NH4NO3溶液中含有的N原子数目为2NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列选项中的实验操作、现象与结论完全一致的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用玻璃棒蘸取次氯酸钠溶液,点在pH试纸上 | 试纸最终显蓝色 | 次氯酸钠溶液显碱性 |
| B | 用pH试纸分别测定0.1 mol·L-1的Na2CO3溶液和0.1 mol·L-1的NaHCO3溶液的pH | Na2CO3溶液的pH约为10,NaHCO3 溶液的pH约为8 | 结合H+能力:CO >HCO >HCO |
| C | 用坩埚钳夹住一小块用砂纸打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点低 |
| D | 将NaAlO2溶液加入NaHCO3溶液中 | 有白色沉淀生成 | A1O 结合H+能力比CO 结合H+能力比CO 强 强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】根据下列实验操作和现象所得到的结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向2mL0.1mol·L−1的FeCl3溶液中加入4mL0.1mol·L−1的KI溶液,充分反应后,分别取少量溶液于两支试管中,向其中一支试管中滴加几滴淀粉溶液,溶液变蓝,另一支试管中滴加几滴KSCN溶液,溶液变红 | KI与FeCl3的反应是可逆反应 |
| B | 室温下,向0.1mol·L−1HCl溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升 | 镁与盐酸反应放热 |
| C | 向盛有2mL0.1mol·L-1的硝酸银溶液的试管中滴加2滴0.1mol·L-1的氯化钠溶液,生成白色沉淀,再滴加2滴 0.1mol·L-1的碘化钾溶液,有黄色沉淀生成 | Ksp(AgI)<Ksp(AgCl) |
| D | 用pH试纸测得:CH3COONa溶液的pH约为9,NaHCO3溶液的pH约为10 | CH3COOH电离出H+的能力比H2CO3强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 的
的 的氨水;④
的氨水;④ 溶液;⑤
溶液;⑤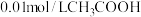 溶液。下列判断不正确的是
溶液。下列判断不正确的是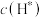 :①=②=③=④
:①=②=③=④ 的量④最多
的量④最多



