(1)下列N元素的电子排布式表示的状态中,失去一个电子所需能量最低的为
A.1s22s22p 2p 2p 2p 2p | B.1s22s22p 2p 2p 3s1 3s1 |
C.1s22s22p 2p 2p | D.1s22s22p 3s1 3s1 |
(3)向含少量CuSO4的水溶液中逐滴滴入氨水,生成蓝色沉淀,继续滴加氨水至过量,沉淀溶解,得到深蓝色溶液,写出沉淀溶解的离子方程式:
(4)一种铜金合金具有储氢功能,其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子的配位数为

(5)Cu元素与Br元素形成的化合物的晶胞结构亦如图(白球代表Br,黑球代表Cu),该晶胞沿z轴(图)在平面的投影图中,Cu原子构成的几何图形是

相似题推荐

 ]形成氢氧化物沉淀的pH范围如下:
]形成氢氧化物沉淀的pH范围如下:| 金属离子 |  |  |  |  |  |  |  |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)
 的价电子排布式为
的价电子排布式为(2)提高“溶浸”速率,可采取的措施是
(3)“氧化”中添加适量的
 的作用是
的作用是(4)“调pH”除铁和铝,溶液的pH范围应调节为
(5)“除杂2”的目的是生成
 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高, 沉淀不完全,原因是
沉淀不完全,原因是(6)电解酸化的硫酸锰溶液可制取二氧化锰,写出电解时阳极的电极反应式
 及其化合物在生产生活方面都有重要的用途.回答下列问题:
及其化合物在生产生活方面都有重要的用途.回答下列问题:(1)基态铁原子的核外电子排布式为:
 比
比 更稳定的原因是:
更稳定的原因是:(2)
 中铁元素的配位数是
中铁元素的配位数是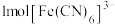 中含有的
中含有的 键的数目为
键的数目为 中C原子的杂化方式为
中C原子的杂化方式为(3)铁和氨在
 可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式: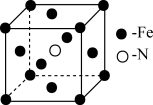
(4)血红素铁用作铁强化剂,其吸收率比一般铁剂高3倍,图中画出
 与N原子间的化学键(若是配位键,需要用箭头加以表示)
与N原子间的化学键(若是配位键,需要用箭头加以表示)
【推荐3】过渡金属及其化合物在生产生活中有着广泛应用。回答下列问题:
(1)锰、锝、铼位于同一副族相邻位置。类比锰,写出基态锝原子的价层电子排布式
(2)下列状态的铁中,电离最外层的一个电子所需能量最大的是
A. B.
B. C.
C. D.
D.
(3)铁制容器在储存N2O4液体时,会腐蚀生成离子化合物N4O6[Fe(NO3)4]2,N4O 的离子为平面结构,其结构图如图1,中心N原子的杂化类型为
的离子为平面结构,其结构图如图1,中心N原子的杂化类型为

(4)EAN规则指的是配合物中心原子价电子数和配体提供的电子数之和为18.符合EAN规则的配合物分子结构和化学性质都较稳定。已知Fe(CO)5和Ni(CO)x均符合EAN规则,性质稳定,而Co(CO)4则容易在化学反应中表现氧化性。
①x=
②从结构角度解释Co(CO)4则容易在化学反应中表现氧化性的原因
(5) Ni和As形成某种晶体的晶胞图如图2所示。其中,大球为Ni,小球为As,距离As最近的Ni构成正三棱柱,其中晶胞下方As原子坐标为(1/3,2/3,1/4)。

①Ni的配位数为
②已知晶胞底面边长为apm,高为cpm,NA为阿伏加德罗常数。则晶胞密度为
(1)基态K原子中,核外电子占据最高能层的符号是
(2)元素K的焰色为
(3)I的原子结构示意图为
(4)X射线衍射测定发现,
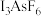 中存在
中存在 离子。
离子。 离子的空间结构为
离子的空间结构为(5)
 晶体是一种性能良好的非线性光学材料,其晶胞结构如图所示,晶胞中K、I、O分别处于顶角、体心、面心位置,棱长为anm。K与O间的最短距离为
晶体是一种性能良好的非线性光学材料,其晶胞结构如图所示,晶胞中K、I、O分别处于顶角、体心、面心位置,棱长为anm。K与O间的最短距离为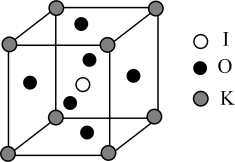
(6)在
 晶胞结构的另一种表示中,I处于各顶角位置,则K处于
晶胞结构的另一种表示中,I处于各顶角位置,则K处于 是一种污染性气体,减少
是一种污染性气体,减少 在大气中的排放是环境保护的重要内容,回答下列问题:
在大气中的排放是环境保护的重要内容,回答下列问题:(1)
 分子的空间构型为
分子的空间构型为 中心原子的杂化方式为
中心原子的杂化方式为(2)下列为二氧化硫和氮的氧化物转化的部分环节:
I.
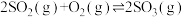
 kJ·mol-1
kJ·mol-1II.
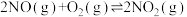
 kJ·mol-1
kJ·mol-1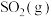 与
与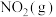 反应生成
反应生成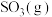 和
和 的热化学方程式为
的热化学方程式为 和
和 通入恒温、恒容反应器发生上述反应,不能判断达到平衡的是
通入恒温、恒容反应器发生上述反应,不能判断达到平衡的是A.混合气体密度保持不变
B.
 与
与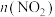 的比值保持不变
的比值保持不变C.

D.在给定条件下,可逆反应完成程度达到最大
(3)利用反应:
 ,可减少
,可减少 在大气中的排放,800℃,在1.0L的恒容密闭容器中投入1.0mol
在大气中的排放,800℃,在1.0L的恒容密闭容器中投入1.0mol 和120gC,容器中压强为
和120gC,容器中压强为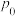 kPa,发生反应
kPa,发生反应 ,5min时容器中
,5min时容器中 的体积分数为20%,10min时达平衡,容器中压强为p kPa时。0~5min
的体积分数为20%,10min时达平衡,容器中压强为p kPa时。0~5min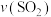
(4)实验室中常用氢氧化钠溶液吸收二氧化硫尾气。当溶液溶质为
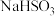 时,若往溶液中加入氨水至中性,则
时,若往溶液中加入氨水至中性,则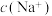
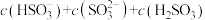 (填“>”、“<”或“=”)。当溶液溶质为
(填“>”、“<”或“=”)。当溶液溶质为 时,若往溶液种加入少量
时,若往溶液种加入少量 固体,完全溶解后(此时溶液是不饱和溶液),溶液中
固体,完全溶解后(此时溶液是不饱和溶液),溶液中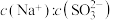 的比值
的比值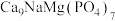 。请回答下列问题:
。请回答下列问题:(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)某同学把
 原子价电子的轨道表示式写成了以下形式:
原子价电子的轨道表示式写成了以下形式: ,这种写法违背了
,这种写法违背了(3)
 原子最高能级电子的电子云轮廓形状为
原子最高能级电子的电子云轮廓形状为(4)
 分子空间结构为
分子空间结构为 与
与 反应生成
反应生成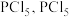 结构为
结构为 ,
, 是
是A.sp B.
 C.
C. D.
D.
氟化镁
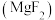 晶体广泛应用在光学、冶金、国防、医疗等领域。氟化镁晶胞是长方体,其结构如下图所示:
晶体广泛应用在光学、冶金、国防、医疗等领域。氟化镁晶胞是长方体,其结构如下图所示: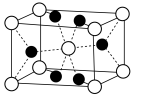
 晶胞示意图中:
晶胞示意图中:a. 表示
表示
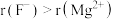 ,结合离子结构示意图解释原因:
,结合离子结构示意图解释原因:一种由
 制备
制备 的工艺流程如下。
的工艺流程如下。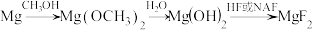
已知:i.
 易溶于甲醇;
易溶于甲醇;ii.
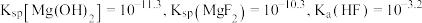
(6)比较相同条件下化学反应速率的大小:①
 与
与 ;②
;② 与
与 。小组同学预测化学反应速率:①<②。实验表明化学反应速率:①>②。分析其原因可能是
。小组同学预测化学反应速率:①<②。实验表明化学反应速率:①>②。分析其原因可能是(7)上述流程中Mg(OH)2开始转化为MgF2所需氟化物的浓度:c(HF)
(1)Co元素在周期表中属于
(2)
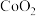 晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述
晶体的层状结构如图所示(小球表示Co原子,大球表示O原子),下列用实线圈出的结构单元示意图还能描述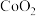 化学组成的是________(填序号)。
化学组成的是________(填序号)。A. | B.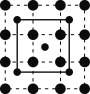 | C. | D. |
(3)二氯二吡啶合铂分子是一种铂配合物,有顺式和反式两种同分异构体(如图)。科学研究表明,顺式分子具有抗癌活性。
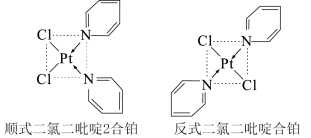
①顺式二氯二吡啶合铂分子中含有的化学键类型为
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
②反式二氯二吡啶合铂分子是
③常用
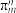 表示分子中的大
表示分子中的大 键,其中m代表参与形成大
键,其中m代表参与形成大 键的原子总数,n代表参与形成大
键的原子总数,n代表参与形成大 键的电子总数,如苯分子中存在
键的电子总数,如苯分子中存在 大
大 键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为
键,吡啶分子是大体积平面形配体,则吡啶中N原子的杂化方式为 键可表示为
键可表示为(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y、z轴的投影图均为如下图所示,则铂原子采取的堆积方式为
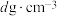 ,则晶胞参数
,则晶胞参数
(1) 由离子键和非极性键构成的是
(2) 由极性键和非极性键构成的是
(3) 不存在化学键的是
(4) 共价化合物有
(5) 写出下列物质的电子式:Na2O2
Ⅱ、某元素原子的价电子构型为4s24p1,它属于第
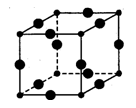
Ⅲ、Cu3N的晶胞结构如图,N3-的配位数为
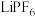 )的碳酸酯作电解液。
)的碳酸酯作电解液。(1)
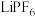 中各元素第一电离能从大到小的关系是
中各元素第一电离能从大到小的关系是(2)
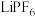 中存在的化学键_______(填序号)。
中存在的化学键_______(填序号)。| A.共价键 | B.离子键 | C.金属键 | D.配位键 |
Ⅱ.碳酸二甲酯是一种低毒、环保性能优异、用途广泛的化工原料。还可以用于汽车、医疗器械等领域。由
 、甲醇为原料合成绿色化学品碳酸二甲酯(
、甲醇为原料合成绿色化学品碳酸二甲酯( )的过程如图,请回答下列问题:
)的过程如图,请回答下列问题:
(3)碳酸二甲酯分子中O—C—O键的键角
 (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。(4)尿素中N的第一电离能比O的高,原因是:
①O失去的是已经配对的电子,配对电子相互排斥,因而第一电离能较低;
②
(5)下列说法不正确的是
A.上述过程a中,从反应物到产物,C和N元素的杂化方式均保持不变
B.
 极易溶解在水中,主要是因为氨分子与水分子间的范德华力作用强
极易溶解在水中,主要是因为氨分子与水分子间的范德华力作用强C.尿素的沸点比碳酸二甲酯的高,主要原因为前者能形成分子间氢键,而后者不能形成分子间氢键
Ⅲ.废旧锂离子电池含
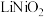 的正极材料经预处理后,可采用如图原理富集Ni元素。
的正极材料经预处理后,可采用如图原理富集Ni元素。
(6)基态Ni+价电子的轨道表示式是
(7)DMG中N原子均与
 配位,且
配位,且 的配位数是4;DMG-Ni中两个配体之间形成分子内氢键。写出DMG—Ni的结构简式
的配位数是4;DMG-Ni中两个配体之间形成分子内氢键。写出DMG—Ni的结构简式Ⅳ.石墨可作锂离子电池的负极材料。充电时,嵌入石墨层间。当嵌入最大量时,晶体部分结构的俯视示意图如图。

(8)此时C与
 的个数比是
的个数比是(1)基态Fe2+的价电子层的电子排布式为
(2)元素的第一电离能用I1表示,则I1(Li)
(3)生产磷酸铁锂离子电池的原料是草酸亚铁(FeC2O4·2H2O)、磷酸氢二铵[(NH4)2HPO4]和碳酸锂(Li2CO3)等。
①
 的空间构型为
的空间构型为②磷酸氢二铵中电负性最高的元素是
 中含σ键的数目为
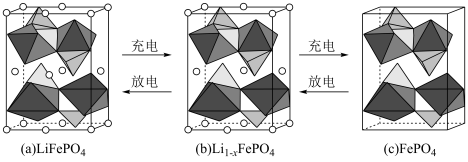
中含σ键的数目为(4)LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有
(1)镍氢电池放电时的总反应为NiOOH+MH=Ni(OH)2+M,M表示储氢合金。基态Ni3+的价层电子排布图为
(2)可用KBH4和NaH2PO4处理储氢合金电极。
①KBH4中阴离子的空间构型是
②NaH2PO4中各元素的电负性由大到小的顺序为
(3)某储氢材料是第三周期金属元素M的氢化物,M的部分电离能如下表所示。M是
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |

①若铁镁合金晶胞沿着体对角线方向的投影如图乙所示(虚线圆圈表示Fe原子的投影),请在图乙中用实心圆点画出Mg原子的投影位置
②储氢时,H2分子在晶胞的体心和棱的中心位置,且最近的两个铁原子之间的距离为dnm,NA表示阿伏加德罗常数的值。则储氢后的晶体密度计算式为

(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为
(3)X晶体内部空腔可吸附小分子,要增强X与H2O的吸附作用,可在L2-上引入
| A.-Cl | B.-OH | C.-NH2 | D.-CH3 |

②X晶体中Zn2+的配位数为
③已知ZnO键长为dnm,理论上图中A、B两个Zn2+之间的最短距离的计算式为
④已知晶胞参数为2anm,阿伏加德罗常数的值为NA,L2-与[Zn4O]6+的相对分子质量分别为M1和M2,则X的晶体密度为



