二氧化碳捕获技术用于去除气流中的二氧化碳或者分离出二氧化碳作为气体产物,其中CO2催化合成甲醇是一种很有前景的方法。如下图所示为该反应在无催化剂及有催化剂时的能量变化。
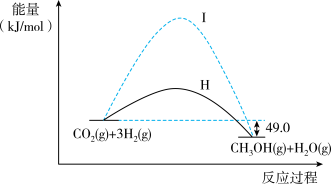
(1)从图可知,有催化剂存在的是过程_________ (填“Ⅰ”或“Ⅱ”)。
(2)写出图中CO2催化合成甲醇的热化学方程式:_________ 。
(3)若要提高反应速率,可以采取的措施有_________ 。
(4)若要提高上述可逆反应 中甲醇的平衡产率,可以采取的措施有_________ 。
(5)已知:1 mol液态甲醇完全气化需吸热37.4 kJ,1 mol液态水完全气化需吸热44.0 kJ,由CO2合成1 mol液态甲醇和1 mol液态水将_________ (填“吸收”或“放出”)_________ kJ热量。
(6)关于CO2催化合成甲醇的反应,下列说法中,合理的是_________ (填字母序号)。
a.该反应中所有原子都被用于合成甲醇
b.该反应可用于CO2的转化,有助于缓解温室效应
c.使用催化剂可以降低该反应的ΔH,从而使反应放出更多热量
d.降温分离出液态甲醇和水,将剩余气体重新通入反应器,可以提高CO2与H2的利用率

(1)从图可知,有催化剂存在的是过程
(2)写出图中CO2催化合成甲醇的热化学方程式:
(3)若要提高反应速率,可以采取的措施有
(4)若要提高上述
(5)已知:1 mol液态甲醇完全气化需吸热37.4 kJ,1 mol液态水完全气化需吸热44.0 kJ,由CO2合成1 mol液态甲醇和1 mol液态水将
(6)关于CO2催化合成甲醇的反应,下列说法中,合理的是
a.该反应中所有原子都被用于合成甲醇
b.该反应可用于CO2的转化,有助于缓解温室效应
c.使用催化剂可以降低该反应的ΔH,从而使反应放出更多热量
d.降温分离出液态甲醇和水,将剩余气体重新通入反应器,可以提高CO2与H2的利用率
更新时间:2022-12-05 09:33:54
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】一氧化二氮可以用作火箭氧化剂,在室温下稳定,易于储存和飞行使用。现利用汽车尾气中的 与
与 反应来制备
反应来制备 气体,回答下列问题。
气体,回答下列问题。
(1)已知: 的燃烧热为
的燃烧热为
①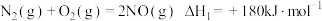
②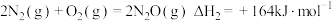
③
反应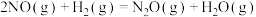 的
的
___________  。
。
(2)总反应分为两步进行;
第①步: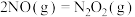
第②步:___________ 。
实验发现,第①步反应几乎不影响总反应到达平衡所用的时间,由此推断,下列关于该反应叙述正确的是___________ 。(填序号)
A.更换催化剂,可改变反应的 B.步骤①的逆反应活化能一定小于②的
B.步骤①的逆反应活化能一定小于②的
C.步骤②的有效碰撞频率小于步骤① D.反应进程中 属于中间产物
属于中间产物
(3)工业上也可用 生产甲醇。在一容积可变的密闭容器中充入
生产甲醇。在一容积可变的密闭容器中充入 与
与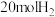 ,容器体积为2L,在催化剂作用下发生反应:
,容器体积为2L,在催化剂作用下发生反应: 。
。 的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。
的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。
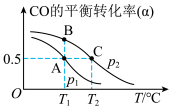
①压强为
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②在起始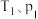 条件下,2L恒容容器中,反应的平衡常数
条件下,2L恒容容器中,反应的平衡常数
___________  。
。
(4)煤化工通常研究不同条件下CO的转化率以解决实际问题。已知在催化剂存在条件下发生反应: 中
中 的平衡转化率随投料比
的平衡转化率随投料比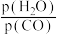 及温度变化关系如图所示:
及温度变化关系如图所示:
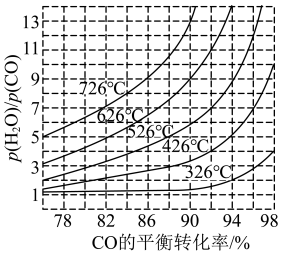
①该反应是___________ 反应(填“吸热”或“放热”);
②在以铁镁为催化剂的工业中,一般控制温度为 左右、投料比2)=3~5,采用此条件的原因可能是
左右、投料比2)=3~5,采用此条件的原因可能是___________ 。
 与
与 反应来制备
反应来制备 气体,回答下列问题。
气体,回答下列问题。(1)已知:
 的燃烧热为
的燃烧热为
①
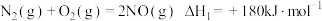
②
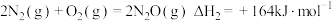
③

反应
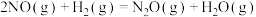 的
的
 。
。(2)总反应分为两步进行;
第①步:
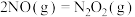
第②步:
实验发现,第①步反应几乎不影响总反应到达平衡所用的时间,由此推断,下列关于该反应叙述正确的是
A.更换催化剂,可改变反应的
 B.步骤①的逆反应活化能一定小于②的
B.步骤①的逆反应活化能一定小于②的C.步骤②的有效碰撞频率小于步骤① D.反应进程中
 属于中间产物
属于中间产物(3)工业上也可用
 生产甲醇。在一容积可变的密闭容器中充入
生产甲醇。在一容积可变的密闭容器中充入 与
与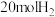 ,容器体积为2L,在催化剂作用下发生反应:
,容器体积为2L,在催化剂作用下发生反应: 。
。 的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。
的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。
①压强为

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②在起始
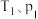 条件下,2L恒容容器中,反应的平衡常数
条件下,2L恒容容器中,反应的平衡常数
 。
。(4)煤化工通常研究不同条件下CO的转化率以解决实际问题。已知在催化剂存在条件下发生反应:
 中
中 的平衡转化率随投料比
的平衡转化率随投料比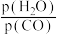 及温度变化关系如图所示:
及温度变化关系如图所示:
①该反应是
②在以铁镁为催化剂的工业中,一般控制温度为
 左右、投料比2)=3~5,采用此条件的原因可能是
左右、投料比2)=3~5,采用此条件的原因可能是
您最近一年使用:0次
【推荐2】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
① 甲硅烷(SiH4)固态时属于__________ 晶体。
② 已知室温下1g甲硅烷自燃生成SiO2和液态水放出热量44.6kJ,则其热化学方程式为____________ 。
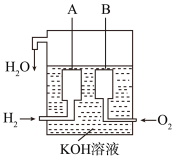
(2)美国阿波罗宇宙飞船上使用了一种新型电池装置,其构造如下图所示,A、B两个电极均由多孔的炭块组成。该电池的负极反应式为:_____________________ 。若该电池工作时增加了1mol H2O,电路中转移电子的物质的量为__________ 。
(3)化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是____________ 。

A. 该反应是吸热反应
B. 断裂1mol A-A键和1mol B-B键放出x kJ的能量
C. 断裂2mol A-B键需要吸收y kJ的能量
D. 2mol AB的总能量高于1mol A2和1mol B2的总能量
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
① 甲硅烷(SiH4)固态时属于
② 已知室温下1g甲硅烷自燃生成SiO2和液态水放出热量44.6kJ,则其热化学方程式为
(2)美国阿波罗宇宙飞船上使用了一种新型电池装置,其构造如下图所示,A、B两个电极均由多孔的炭块组成。该电池的负极反应式为:

(3)化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是

A. 该反应是吸热反应
B. 断裂1mol A-A键和1mol B-B键放出x kJ的能量
C. 断裂2mol A-B键需要吸收y kJ的能量
D. 2mol AB的总能量高于1mol A2和1mol B2的总能量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】研究化学反应中的能量变化时,在一只小烧杯里,加入20 g已研磨成粉末的Ba(OH)2·8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10 g NH4Cl晶体,根据下图所示实验步骤进行操作。回答下列问题:
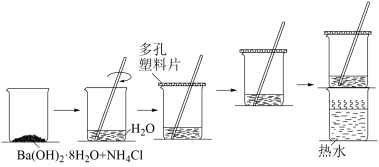
(1)写出实验过程中发生反应的化学方程式:________________________________ 。
(2)检验有NH3生成的方法是_______________________________________________ 。
(3)反应中产生的NH3会污染环境,对人体有害。为减少其挥发,实验时在烧杯上方盖了一个多孔塑料板,反应后移走多孔塑料板,发现混合物成糊状,证明有_____ 生成。为了更好的解决NH3的污染问题,可以做一个简单的改进,你的改进方法是__________________ 。

(1)写出实验过程中发生反应的化学方程式:
(2)检验有NH3生成的方法是
(3)反应中产生的NH3会污染环境,对人体有害。为减少其挥发,实验时在烧杯上方盖了一个多孔塑料板,反应后移走多孔塑料板,发现混合物成糊状,证明有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】2022年,第24届冬奥会将在中国北京、张家口两地举办。中国绿色碳汇基金会发起“我们的冬奥碳汇林”众筹项目,计划在张家口市崇礼区种植小树。碳汇,是指通过植树造林、森林管理、植被恢复等措施,利用植物光合作用吸收大气中的二氧化碳[6CO2(g)+6H2O(l)→C6H12O6(s)+6CO2(g)],并将其固定在植被和土壤中,从而减少温室气体在大气中浓度的过程、活动或机制。已知利用植物的光合作用每吸收1molCO2需要吸收的能量约为470kJ。请回答下列问题:
(1)碳汇过程中能量的转化形式为___________ 能转化为___________ 能;有资料表明,某块林木通过光合作用大约吸收了1.88×107kJ能量,则吸收的CO2为___________ kg;葡萄糖完全燃烧生成液态水的热化学方程式为___________ 。
(2)工业废气中的CO2可用碱液吸收。已知:
①CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l) =-akJ/mol;
=-akJ/mol;
②CO2(g)+NaOH(aq)=NaHCO3(aq) =-bkJ/mol。
=-bkJ/mol。
反应CO2(g)+H2O(l)+Na2CO3(aq)=2NaHCO3(aq)的 =
=___________ kJ/mol(用含a、b的代数式表示)。
(3)生产液晶显示器的过程中使用的化学清洗剂NF3和CO2一样,也是一种温室气体,其在大气中能够稳定存在数百年。下表是几种化学键的键能:
①关于反应N2(g)+3F2(g)=2NF3(g),下列说法中不正确的是__________ 。
A.过程N2(g)=2N(g)放出能量
B.反应N2(g)+3F2(g)=2NF3(g)放出能量
C.使用催化剂能减小反应的
②NF3对半导体硅进行蚀刻时,在蚀刻物表面不留任何残留物,试写出蚀刻反应方程式___________ 。
(1)碳汇过程中能量的转化形式为
(2)工业废气中的CO2可用碱液吸收。已知:
①CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l)
 =-akJ/mol;
=-akJ/mol;②CO2(g)+NaOH(aq)=NaHCO3(aq)
 =-bkJ/mol。
=-bkJ/mol。反应CO2(g)+H2O(l)+Na2CO3(aq)=2NaHCO3(aq)的
 =
=(3)生产液晶显示器的过程中使用的化学清洗剂NF3和CO2一样,也是一种温室气体,其在大气中能够稳定存在数百年。下表是几种化学键的键能:
| 化学键 | N≡N | F-F | N-F |
| 键能/kJ/mol | 946.0 | 157.0 | 283.0 |
①关于反应N2(g)+3F2(g)=2NF3(g),下列说法中不正确的是
A.过程N2(g)=2N(g)放出能量
B.反应N2(g)+3F2(g)=2NF3(g)放出能量
C.使用催化剂能减小反应的

②NF3对半导体硅进行蚀刻时,在蚀刻物表面不留任何残留物,试写出蚀刻反应方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】I.氨是最基本的化工原料之一,工业合成氨生产流程示意图如下:
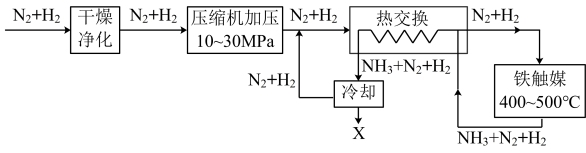
(1)X的化学式为___________
(2)对于合成氨的反应下列说法正确的是___________(填编号)
II.历史上诺贝尔化学奖曾经有3次颁给研究氮气与氢气合成氨的化学家,目前Haber-Bosch法是工业合成氨的主要方式,其生产条件需要高温高压,为了有效降低能耗,过渡金属催化还原氮气合成氨被认为是具有巨大前景的替代方法。催化过程一般有吸附—解离—反应—脱附等过程,图1为N2和H2在固体催化剂表面合成氨反应路径的势能面图(部分数据略),其中“*”表示被催化剂吸附。
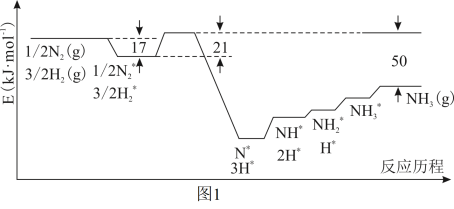
(3)氨气的脱附是______ (填吸热、放热)过程,合成氨反应的热化学方程式:_______
(4)合成氨的捷姆金和佩热夫速率方程式为 ,v为反应的瞬时总速率,即正反应速率和逆反应速率之差,k1、k2分别是正、逆反应速率常数。已知:Kp是用平衡分压代替平衡浓度而得到的平衡常数(平衡分压=总压×物质的量分数),则合成氨反应
,v为反应的瞬时总速率,即正反应速率和逆反应速率之差,k1、k2分别是正、逆反应速率常数。已知:Kp是用平衡分压代替平衡浓度而得到的平衡常数(平衡分压=总压×物质的量分数),则合成氨反应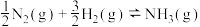 的平衡常数Kp=
的平衡常数Kp=______ (用含k1、k2的代数式表示)。
(5)已知催化剂在不同温度下催化活性不同。在使用同一催化剂时,将2mol N2和6mol H2通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应(如图2)。曲线A表示T2时n(H2)的变化,曲线B表示T1时n(NH3)的变化,T2时反应到a点恰好达到平衡。

①T2温度下反应进行到某时刻,测得容器内气体的压强为起始时的80%,则此时v(正)______ v(逆)(填“>”、“<”或“=”)。
②由图分析可得,温度T1________ T2(填“>”、“<”或“=”或“不确定”)。

(1)X的化学式为
(2)对于合成氨的反应下列说法正确的是___________(填编号)
| A.该反应在任意条件下都可以自发进行 |
| B.铁触媒在该温度时活性大 |
| C.若平衡后保持温度和容积不变,充入氮气和氢气,使氮气氢气的浓度均变为原来的二倍,则氮气的转化率将减小 |
D.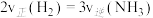 ,混合气体的平均摩尔质量不再随时间变化均可以作为平衡的标志 ,混合气体的平均摩尔质量不再随时间变化均可以作为平衡的标志 |
II.历史上诺贝尔化学奖曾经有3次颁给研究氮气与氢气合成氨的化学家,目前Haber-Bosch法是工业合成氨的主要方式,其生产条件需要高温高压,为了有效降低能耗,过渡金属催化还原氮气合成氨被认为是具有巨大前景的替代方法。催化过程一般有吸附—解离—反应—脱附等过程,图1为N2和H2在固体催化剂表面合成氨反应路径的势能面图(部分数据略),其中“*”表示被催化剂吸附。

(3)氨气的脱附是
(4)合成氨的捷姆金和佩热夫速率方程式为
 ,v为反应的瞬时总速率,即正反应速率和逆反应速率之差,k1、k2分别是正、逆反应速率常数。已知:Kp是用平衡分压代替平衡浓度而得到的平衡常数(平衡分压=总压×物质的量分数),则合成氨反应
,v为反应的瞬时总速率,即正反应速率和逆反应速率之差,k1、k2分别是正、逆反应速率常数。已知:Kp是用平衡分压代替平衡浓度而得到的平衡常数(平衡分压=总压×物质的量分数),则合成氨反应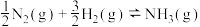 的平衡常数Kp=
的平衡常数Kp=(5)已知催化剂在不同温度下催化活性不同。在使用同一催化剂时,将2mol N2和6mol H2通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应(如图2)。曲线A表示T2时n(H2)的变化,曲线B表示T1时n(NH3)的变化,T2时反应到a点恰好达到平衡。

①T2温度下反应进行到某时刻,测得容器内气体的压强为起始时的80%,则此时v(正)
②由图分析可得,温度T1
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知X、Y、Z为常见的单质,其它为化合物,X的组成元素是地壳中含量最多的金属元素。B是一种能使湿润的红色石蕊试纸变蓝的气体,D是一种常见的两性氢氧化物。各物质间的转化关系如下图所示(部分条件与产物已略去)。
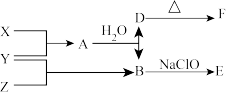
回答下列问题:
(1)E是一种高能燃料,其组成元素与B相同,1 mol E分子中不同原子的数目比为1:2,且含有18 mol电子,则E的化学式为___________ 。
(2)NaClO的电子式为___________ 。
(3)X的原子核外电子占据最高能级的电子云轮廓图为___________ 形。
(4)A与H2O反应的化学方程式为___________ 。
(5)D与强碱溶液反应的离子方程式为___________ 。
(6)B与NaClO反应时,1 mol NaClO参加反应,转移2 mol电子,该反应的化学方程式为___________ 。
(7)一定条件下,X与TiO2、C(石墨)反应只生成F和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知,该反应生成1 mol F时放出526 kJ热量,其热化学方程式为___________ 。
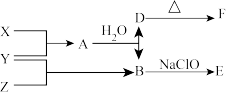
回答下列问题:
(1)E是一种高能燃料,其组成元素与B相同,1 mol E分子中不同原子的数目比为1:2,且含有18 mol电子,则E的化学式为
(2)NaClO的电子式为
(3)X的原子核外电子占据最高能级的电子云轮廓图为
(4)A与H2O反应的化学方程式为
(5)D与强碱溶液反应的离子方程式为
(6)B与NaClO反应时,1 mol NaClO参加反应,转移2 mol电子,该反应的化学方程式为
(7)一定条件下,X与TiO2、C(石墨)反应只生成F和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知,该反应生成1 mol F时放出526 kJ热量,其热化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】《化学反应原理》对于深入了解化学反应的本质及其规律是极为重要的,它们不仅具有理论意义,而且具有实际价值;它们不仅是核心的基础化学知识,而且对学生今后从事科学研究与技术创新具有重要的指导作用。 有甲、乙两个研究性学习小组分别设计了以下实验
I.甲组同学,为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图A、B所示的实验。请回答下列问题:
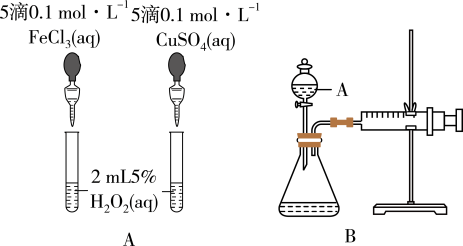
(1)定性比较:图A可通过观察_________ ,定性比较得出结论。有同学提出将CuSO4改为CuCl2更合理,其理由是_________ 。
(2)定量比较:如图B所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是________ ,实验中需要测量的数据是___________ 。
(3)将0.1 mol MnO2粉末加入到50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。计算H2O2的初始物质的量浓度________________ 。(请保留两位有效数字)

Ⅱ.乙组同学按照如图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)。
(1)实验原理:硫代硫酸钠溶液与稀硫酸反应,其化学方程式为:___ 。
(2)实验目的:
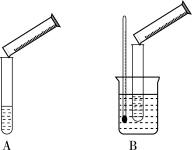
装置A,探究浓度对化学反应速率的影响;装置B,探究__________ 对化学反应速率的影响。
(3)通过A、B装置,分别进行了三组实验,数据记录如下,并经分析得出相关结论:
结论1:由Ⅰ和Ⅱ两组数据可知,_______ ;
结论2:由Ⅱ和Ⅲ两组数据可知,________ 。
I.甲组同学,为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图A、B所示的实验。请回答下列问题:

(1)定性比较:图A可通过观察
(2)定量比较:如图B所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是
(3)将0.1 mol MnO2粉末加入到50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。计算H2O2的初始物质的量浓度

Ⅱ.乙组同学按照如图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)。
(1)实验原理:硫代硫酸钠溶液与稀硫酸反应,其化学方程式为:
(2)实验目的:

装置A,探究浓度对化学反应速率的影响;装置B,探究
(3)通过A、B装置,分别进行了三组实验,数据记录如下,并经分析得出相关结论:
| 实验组号 | 温度/℃ | Na2S2O3溶液 | H2SO4 | 加入H2O 的体积/mL | 出现沉淀所需时间/s | ||
| 体积 /mL | 浓度/ (mol • L−1) | 体积/mL | 浓度/(mol • L−1) | ||||
| I | 0 | 5 | 0.1 | 10 | 0.1 | 5 | 8 |
| Ⅱ | 0 | 5 | 0.1 | 5 | 0.1 | 10 | 12 |
| Ⅲ | 30 | 5 | 0.1 | 5 | 0.1 | 10 | 4 |
结论2:由Ⅱ和Ⅲ两组数据可知,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学小组利用酸性KMnO4与草酸(H2C2O4)反应,设计以下实验探究化学反应快慢的影响因素。
实验用品:0.04 mol/L KMnO4溶液、0.2 mol/L H2C2O4溶液、0.36 mol/L稀硫酸、蒸馏水、MnSO4溶液、5mL量筒、胶头滴管、井穴板、细玻璃棒及秒表等
实验内容及记录:
回答下列问题:
(1)写出酸性KMnO4与草酸反应的离子方程式___________ 。
(2)V1=___________ mL,V2=___________ mL,理由是___________ 。
(3)欲探究温度对反应速率的影响,应选择的实验是___________ (填编号)。
(4)为验证“Mn2+对该反应有催化作用”,该小组同学用如图装置进行了实验④和⑤,其中实验所用酸性KMnO4溶液由0.36 mol/L稀硫酸与0.04 mol/L KMnO4溶液溶液以体积比1∶1混合所得。
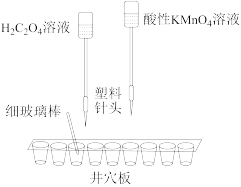
实验④:向一个井穴中滴入10滴0.2 mol/L H2C2O4溶液,逐滴加入酸性KMnO4溶液,并记录各滴加入后的褪色时间。
实验⑤:向三个井穴中分别滴加10滴0.2 mol/L H2C2O4溶液,依次滴加1、2、3滴 溶液和3、2、1滴蒸馏水,搅拌均匀,再各滴加1滴酸性KMnO4溶液,并记录褪色时间及混合体系颜色变化。
溶液和3、2、1滴蒸馏水,搅拌均匀,再各滴加1滴酸性KMnO4溶液,并记录褪色时间及混合体系颜色变化。
实验记录如下:
已知:MnO2为难溶于水的褐色固体;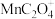 溶液呈红色,不稳定,会缓慢分解为Mn2+和CO2。
溶液呈红色,不稳定,会缓慢分解为Mn2+和CO2。
i.实验④中第5滴出现褐色沉淀可能的原因是___________ (用离子方程式表示)。
ii.实验④和⑤的现象验证了“ 对该反应有催化作用”,催化过程如下:
对该反应有催化作用”,催化过程如下:
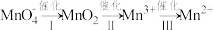
实验⑤中催化剂用量增加,褪色时间却略有延长,说明催化剂过量易催化到“催化过程”的第___________ 步,反应过程出现红色的原因是___________ 。
实验用品:0.04 mol/L KMnO4溶液、0.2 mol/L H2C2O4溶液、0.36 mol/L稀硫酸、蒸馏水、MnSO4溶液、5mL量筒、胶头滴管、井穴板、细玻璃棒及秒表等
实验内容及记录:
| 实验编号 | 试管中所加试剂及用量/mL | 温度/℃ | 紫色褪去所需时间/min | |||
| H2C2O4溶液 | KMnO4溶液 | 稀硫酸 | 蒸馏水 | |||
| ① | 2.0 | 1.0 | 1.0 | 2.0 | 20 | 4.1 |
| ② | 3.0 | 1.0 | 1.0 | V1 | 20 | 3.7 |
| ③ | V2 | 1.0 | 1.0 | 2.0 | 80 | t |
(1)写出酸性KMnO4与草酸反应的离子方程式
(2)V1=
(3)欲探究温度对反应速率的影响,应选择的实验是
(4)为验证“Mn2+对该反应有催化作用”,该小组同学用如图装置进行了实验④和⑤,其中实验所用酸性KMnO4溶液由0.36 mol/L稀硫酸与0.04 mol/L KMnO4溶液溶液以体积比1∶1混合所得。

实验④:向一个井穴中滴入10滴0.2 mol/L H2C2O4溶液,逐滴加入酸性KMnO4溶液,并记录各滴加入后的褪色时间。
实验⑤:向三个井穴中分别滴加10滴0.2 mol/L H2C2O4溶液,依次滴加1、2、3滴
 溶液和3、2、1滴蒸馏水,搅拌均匀,再各滴加1滴酸性KMnO4溶液,并记录褪色时间及混合体系颜色变化。
溶液和3、2、1滴蒸馏水,搅拌均匀,再各滴加1滴酸性KMnO4溶液,并记录褪色时间及混合体系颜色变化。实验记录如下:
| 实验④ | KMnO4溶液 | 第1滴 | 第2滴 | 第3滴 | 第4滴 | 第5滴 |
| 紫色褪去所需时间/s | 100 | 20 | 10 | 5 | 出现褐色沉淀 | |
| 实验⑤ | MnSO4溶液 | 1滴 | 2滴 | 3滴 | 体系颜色变化:红色→浅红色→无色 | |
| 蒸馏水 | 3滴 | 2滴 | 1滴 | |||
| 紫色褪去所需时间/s | 12 | 16 | 16 | |||
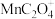 溶液呈红色,不稳定,会缓慢分解为Mn2+和CO2。
溶液呈红色,不稳定,会缓慢分解为Mn2+和CO2。i.实验④中第5滴出现褐色沉淀可能的原因是
ii.实验④和⑤的现象验证了“
 对该反应有催化作用”,催化过程如下:
对该反应有催化作用”,催化过程如下: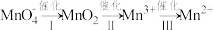
实验⑤中催化剂用量增加,褪色时间却略有延长,说明催化剂过量易催化到“催化过程”的第
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】乙酸制氢过程有如下反应:
反应Ⅰ:CH3COOH(g) 2CO(g)+2H2(g) △H1
2CO(g)+2H2(g) △H1
反应Ⅱ:CH3COOH(g) CH4(g)+CO2(g) △H2
CH4(g)+CO2(g) △H2
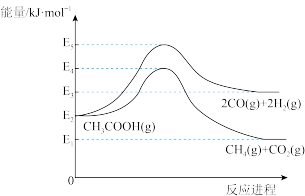
(1)由如图可知,△H1=_______ kJ/mol(用有关E的代数式表示)。
(2)在容积相同的密闭容器中,加入等量乙酸蒸气制氢,在相何时间测得温度与气体产率的关系如图。
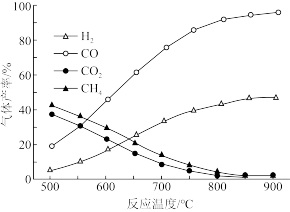
①650℃之前,氢气产率低于甲烷的原因是_______ 。
②分析图象发现,该容器内还发生了其他的副反应,分析理由是_______ 。
③若保持其他条件不变,在乙酸蒸气中掺杂一定量水,氢气的产率显著提高而CO的产率下降,请用化学方程式表示可能发生的反应_______ 。
(3)按照符合“绿色化学”要求(原子利用率100%),可采用光催化反应技术直接合成乙酸,下列原料组合符合要求的是_______(填标号)
(4)用甲醇与CO反应来制备乙酸。反应如下:CH3OH(g)+CO(g) =CH3COOH(1) 。在恒压密闭容器中通入0.20 mol的CH3OH和0.22mol的CO气体,回答如下问题:
①恒温恒压下,不能说明上述反应达到平衡状态的是_______ (填编号)。
A.容器内混合气体的密度保持不变 B.容器内压强保持不变
C.CH3OH的浓度保持不变 D.CO的体积分数保持不变
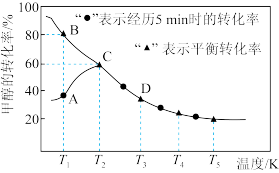
②测得甲醇的转化率随温度变化如图所示。温度为T1时,该反应的正反应速率:v(B)正_______ v(A)正(填“>”,“=”或“<”)。温度为T1时,在恒压容器中,上述反应已达到平衡,再通入0.10molCH3OH和0.11molCO的混合气体,再次达到平衡,甲醇的转化率_______ 80%(“>”,“=”或“<”)。
反应Ⅰ:CH3COOH(g)
 2CO(g)+2H2(g) △H1
2CO(g)+2H2(g) △H1反应Ⅱ:CH3COOH(g)
 CH4(g)+CO2(g) △H2
CH4(g)+CO2(g) △H2(1)由如图可知,△H1=

(2)在容积相同的密闭容器中,加入等量乙酸蒸气制氢,在相何时间测得温度与气体产率的关系如图。

①650℃之前,氢气产率低于甲烷的原因是
②分析图象发现,该容器内还发生了其他的副反应,分析理由是
③若保持其他条件不变,在乙酸蒸气中掺杂一定量水,氢气的产率显著提高而CO的产率下降,请用化学方程式表示可能发生的反应
(3)按照符合“绿色化学”要求(原子利用率100%),可采用光催化反应技术直接合成乙酸,下列原料组合符合要求的是_______(填标号)
| A.CO2+H2 | B.CO+H2 | C.H2O+CH4 | D.CO2+CH4 |
①恒温恒压下,不能说明上述反应达到平衡状态的是
A.容器内混合气体的密度保持不变 B.容器内压强保持不变
C.CH3OH的浓度保持不变 D.CO的体积分数保持不变
②测得甲醇的转化率随温度变化如图所示。温度为T1时,该反应的正反应速率:v(B)正

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】甲醇是一种化工产品,也是潜在储氢材料。工业合成甲醇的原理:
(1)在恒温恒容密闭容器中充入 和
和 发生上述反应合成甲醇,下列情况表明达到平衡状态的是___________。
发生上述反应合成甲醇,下列情况表明达到平衡状态的是___________。
(2)在反应器中充入 、
、 合成
合成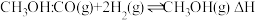 。已知:达到平衡时,升高温度,逆反应速率大于正反应速率。下列措施能提高
。已知:达到平衡时,升高温度,逆反应速率大于正反应速率。下列措施能提高 平衡转化率的是___________,
平衡转化率的是___________,
(3)甲醇分解制备 反应历程如图所示(*表示吸附在催化剂表面)。
反应历程如图所示(*表示吸附在催化剂表面)。
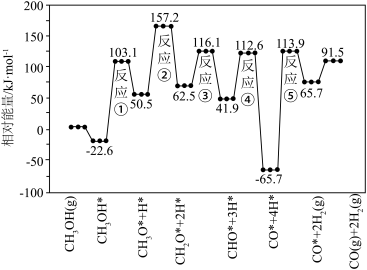
决速步骤的反应式为_________________________ 。总反应的热化学方程式为______________________ 。
(4)体积均为 的甲、乙恒容密闭容器中起始都充入
的甲、乙恒容密闭容器中起始都充入 和
和 ,合成
,合成 。分别在恒温、绝热情况下发生反应,测得混合气体压强变化如图所示。
。分别在恒温、绝热情况下发生反应,测得混合气体压强变化如图所示。
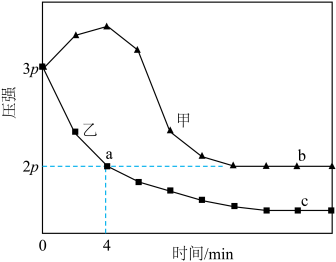
①正反应速率:b_____ c(填“>”“<”或“=”,下同),气体总物质的量:a_____ b。
②a点时,乙容器体系中浓度熵Q等于________  ,b点对应的平衡常数K
,b点对应的平衡常数K______ Q。

(1)在恒温恒容密闭容器中充入
 和
和 发生上述反应合成甲醇,下列情况表明达到平衡状态的是___________。
发生上述反应合成甲醇,下列情况表明达到平衡状态的是___________。| A.混合气体密度不随时间变化 | B. 体积分数不随时间变化 体积分数不随时间变化 |
| C.气体总压强不随时间变化 | D.气体平均摩尔质量不随时间变化 |
(2)在反应器中充入
 、
、 合成
合成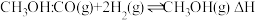 。已知:达到平衡时,升高温度,逆反应速率大于正反应速率。下列措施能提高
。已知:达到平衡时,升高温度,逆反应速率大于正反应速率。下列措施能提高 平衡转化率的是___________,
平衡转化率的是___________,| A.升高温度 | B.增大压强 | C.加入催化剂 | D.增大投料比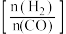 |
(3)甲醇分解制备
 反应历程如图所示(*表示吸附在催化剂表面)。
反应历程如图所示(*表示吸附在催化剂表面)。
决速步骤的反应式为
(4)体积均为
 的甲、乙恒容密闭容器中起始都充入
的甲、乙恒容密闭容器中起始都充入 和
和 ,合成
,合成 。分别在恒温、绝热情况下发生反应,测得混合气体压强变化如图所示。
。分别在恒温、绝热情况下发生反应,测得混合气体压强变化如图所示。
①正反应速率:b
②a点时,乙容器体系中浓度熵Q等于
 ,b点对应的平衡常数K
,b点对应的平衡常数K
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】化学反应原理与生产、生活密切相关。请回答以下问题。
(1)嫦娥5号采用液态偏二甲肼(C2H8N2)为燃料,与液态N2O4反应产生能量做为动力,反应生成无毒、无污染的气体和液态水。室温下,已知1.5g该燃料完全燃烧释放出的能量为50kJ,写出该反应的热化学方程式_______ 。
(2)工业炼铝的阳极反应式为_______ 。工业上每生产1吨铝,阳极大约会损失0.6吨石墨。假设阳极生成的氧气全部与石墨电极反应,石墨的氧化产物是_______ 。
(3)25℃时,将pH=10的NaOH溶液和pH=13的NaOH溶液等体积混合(忽略混合过程中的体积变化),溶液的pH为_______ (已知lg2=0.3)。
(4)在溶液中无法用AlCl3和Na2S反应制取Al2S3固体,请利用离子方程式解释原因_______ 。
(5)一定条件下,在某体积可变的密闭容器中发生反应 。达到平衡后对该容器进行压缩,平衡移动方向为
。达到平衡后对该容器进行压缩,平衡移动方向为_______ (填“正向移动”、“逆向移动”或“不移动”)。如果升高温度有利于氢气的生成,则正反应为_______ (填“放热反应”“吸热反应”)。
(1)嫦娥5号采用液态偏二甲肼(C2H8N2)为燃料,与液态N2O4反应产生能量做为动力,反应生成无毒、无污染的气体和液态水。室温下,已知1.5g该燃料完全燃烧释放出的能量为50kJ,写出该反应的热化学方程式
(2)工业炼铝的阳极反应式为
(3)25℃时,将pH=10的NaOH溶液和pH=13的NaOH溶液等体积混合(忽略混合过程中的体积变化),溶液的pH为
(4)在溶液中无法用AlCl3和Na2S反应制取Al2S3固体,请利用离子方程式解释原因
(5)一定条件下,在某体积可变的密闭容器中发生反应
 。达到平衡后对该容器进行压缩,平衡移动方向为
。达到平衡后对该容器进行压缩,平衡移动方向为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下图所示:
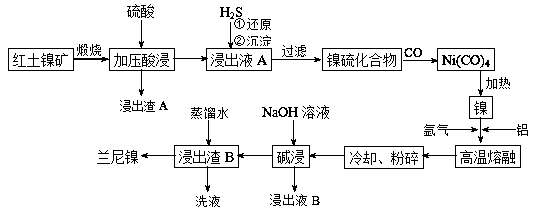
(1)在形成Ni(CO)4的过程中,碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为___________ ;
(2)已知红土镍矿煅烧后生成Ni2O3,而加压酸浸后浸出液A中含有Ni2+,写出有关镍元素的加压酸浸的化学反应方程式______________________ ;
(3)向浸出液A中通入H2S气体,反应的离子方程式是____________________ ;
(4)“高温熔融”时能否将通入氩气换为CO并说明原因_____________________ ;
(5)“碱浸”的目的是使镍铝合金产生多孔结构,从而增强对氢气的强吸附性,此过程
中发生反应的离子方程式为___________________ 。浸出反应所用的NaOH溶液的浓度要大,若NaOH溶液较稀时,则会产生少量的Al(OH)3沉淀而阻止浸出反应的持续进行,请用化学反应原理加以解释:________________________ 。
(6)浸出液B可以回收,重新生成铝以便循环利用。请设计简单的回收流程:
浸出液B→________________________ 。(示例:CuOCu2+Cu)

(1)在形成Ni(CO)4的过程中,碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为
(2)已知红土镍矿煅烧后生成Ni2O3,而加压酸浸后浸出液A中含有Ni2+,写出有关镍元素的加压酸浸的化学反应方程式
(3)向浸出液A中通入H2S气体,反应的离子方程式是
(4)“高温熔融”时能否将通入氩气换为CO并说明原因
(5)“碱浸”的目的是使镍铝合金产生多孔结构,从而增强对氢气的强吸附性,此过程
中发生反应的离子方程式为
(6)浸出液B可以回收,重新生成铝以便循环利用。请设计简单的回收流程:
浸出液B→
您最近一年使用:0次



