在不同温度下,向2 L密闭容器中加入1 mol NO和1 mol活性炭,发生反应:2NO(g)+C(s)  N2(g)+CO2(g) ΔH=-213.5 kJ/mol,达到平衡时的数据如下:
N2(g)+CO2(g) ΔH=-213.5 kJ/mol,达到平衡时的数据如下:
下列说法不正确 的是
 N2(g)+CO2(g) ΔH=-213.5 kJ/mol,达到平衡时的数据如下:
N2(g)+CO2(g) ΔH=-213.5 kJ/mol,达到平衡时的数据如下:| 温度/℃ | n(活性炭)/mol | n(CO2)/mol |
| T1 | 0. 70 | ___________ |
| T2 | ___________ | 0.25 |
| A.上述信息可推知:T1<T2 |
B.T1℃时,该反应的平衡常数K=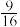 |
| C.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小 |
| D.T2℃时,平衡后,再充入1.5mol NO,0.75mol N2,0.75mol CO2和足量的碳,平衡不移动 |
更新时间:2022-12-26 17:37:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知在25 ℃时,反应①②③的化学方程式及化学平衡常数为①N2(g)+O2(g)  2NO(g),K1=1×10-30;②2H2(g)+O2(g)
2NO(g),K1=1×10-30;②2H2(g)+O2(g)  2H2O(g),K2=2×1081;③2CO(g)+O2(g)
2H2O(g),K2=2×1081;③2CO(g)+O2(g)  2CO2(g),K3=2.5×1091.下列说法正确的是
2CO2(g),K3=2.5×1091.下列说法正确的是
 2NO(g),K1=1×10-30;②2H2(g)+O2(g)
2NO(g),K1=1×10-30;②2H2(g)+O2(g)  2H2O(g),K2=2×1081;③2CO(g)+O2(g)
2H2O(g),K2=2×1081;③2CO(g)+O2(g)  2CO2(g),K3=2.5×1091.下列说法正确的是
2CO2(g),K3=2.5×1091.下列说法正确的是A.NO分解反应NO(g)   N2(g)+ N2(g)+ O2(g)的平衡常数为1×1030 O2(g)的平衡常数为1×1030 |
| B.根据K3的值可知常温下CO和O2很容易发生反应生成CO2 |
| C.温度升高,上述三个反应的平衡常数均减小 |
| D.常温下,NO、H2O、CO2分别发生分解反应生成O2的倾向顺序为NO>H2O>CO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向某密闭容器中充入 ,发生反应:
,发生反应: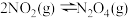 。其它条件相同时,不同温度下,平衡体系中各物质的物质的量分数如下表:(已知:
。其它条件相同时,不同温度下,平衡体系中各物质的物质的量分数如下表:(已知: 为无色气体)
为无色气体)
下列说法不正确 的是
 ,发生反应:
,发生反应: 。其它条件相同时,不同温度下,平衡体系中各物质的物质的量分数如下表:(已知:
。其它条件相同时,不同温度下,平衡体系中各物质的物质的量分数如下表:(已知: 为无色气体)
为无色气体)| T/℃ | 27 | 35 | 49 | 70 |
 % % | 20 | 25 | 40 | 66 |
 % % | 80 | 75 | 60 | 34 |
A.49℃时,该平衡体系中 的转化率为75% 的转化率为75% |
B.平衡时, 的消耗速率为 的消耗速率为 消耗速率的2倍 消耗速率的2倍 |
C.室温时,将盛有 的密闭玻璃球放入冰水中其颜色会变浅 的密闭玻璃球放入冰水中其颜色会变浅 |
D.增大 起始量,可增大相同温度下该反应的化学平衡常数 起始量,可增大相同温度下该反应的化学平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:A(g)+2B(g) 3C(s)+3D(g) △H<0。若在容积可变的密闭容器中进行反应,下列对图像的分析中不正确的是
3C(s)+3D(g) △H<0。若在容积可变的密闭容器中进行反应,下列对图像的分析中不正确的是
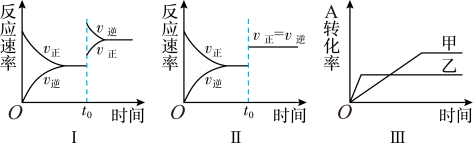
 3C(s)+3D(g) △H<0。若在容积可变的密闭容器中进行反应,下列对图像的分析中不正确的是
3C(s)+3D(g) △H<0。若在容积可变的密闭容器中进行反应,下列对图像的分析中不正确的是
| A.图I研究的是t0时升高温度对反应速率的影响 |
| B.图II可能是t0时使用催化剂对反应速率的影响 |
| C.图III研究的是温度对化学平衡的影响,且乙的温度较高 |
| D.图III研究的是压强对化学平衡的影响,且乙的压强较大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在密闭容器中发生如下反应:mA(g)+nB(g)  pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的 ,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
 pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的 ,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )A.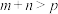 | B.平衡向逆反应方向移动 |
| C.A的转化率不变 | D.C的体积分数增加 |
您最近一年使用:0次
单选题
|
适中
(0.65)
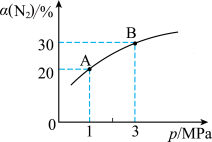
【推荐1】某温度下,发生反应
 ,
, 的平衡转化率(
的平衡转化率( )与体系总压强(p)的关系如图所示。下列说法正确的是
)与体系总压强(p)的关系如图所示。下列说法正确的是

 ,
, 的平衡转化率(
的平衡转化率( )与体系总压强(p)的关系如图所示。下列说法正确的是
)与体系总压强(p)的关系如图所示。下列说法正确的是
A.将1mol 和3mol 和3mol 置于1L密闭容器中发生反应,放出的热量小于92.4kJ 置于1L密闭容器中发生反应,放出的热量小于92.4kJ |
B.平衡状态由A到B时,平衡常数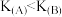 |
C.上述反应在达到平衡后,增大压强, 的产率减小 的产率减小 |
D.反应建立平衡后分离出部分 时,浓度商Q大于平衡常数K 时,浓度商Q大于平衡常数K |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:某温度下,H2(g)+I2(g) 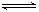 2HI(g)的平衡常数为K1;1/2H2(g)+ 1/2I2(g)
2HI(g)的平衡常数为K1;1/2H2(g)+ 1/2I2(g) 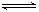 HI(g)的平衡常数为K2,则K1、K2的关系为
HI(g)的平衡常数为K2,则K1、K2的关系为
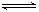 2HI(g)的平衡常数为K1;1/2H2(g)+ 1/2I2(g)
2HI(g)的平衡常数为K1;1/2H2(g)+ 1/2I2(g) 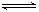 HI(g)的平衡常数为K2,则K1、K2的关系为
HI(g)的平衡常数为K2,则K1、K2的关系为| A.K1= 2K2 | B.K1= K22 | C.K1 = K2 | D.不能确定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对于反应
 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是A.只要氧气过量,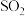 就可以实现转化率100% 就可以实现转化率100% |
| B.其他条件不变,升高体系的温度,该反应的平衡常数K增大 |
C.保持其他条件不变,增大 浓度能提高 浓度能提高 的反应速率和转化率 的反应速率和转化率 |
| D.使用催化剂能改变反应途径,不能改变反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法错误的是
A.H2O2(l)= O2(g)+H2O(l) △H=-98kJ/mol,该反应在任何温度下均能自发进行 O2(g)+H2O(l) △H=-98kJ/mol,该反应在任何温度下均能自发进行 |
B.将0.1mol/L的NH3·H2O溶液加水稀释,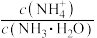 值增大 值增大 |
| C.对于可逆反应,化学平衡向正反应方向移动,则平衡常数一定增大,反应物的转化率增大 |
| D.pH=6的溶液可能呈酸性,因为升高温度,水的离子积Kw增大 |
您最近一年使用:0次


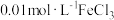 溶液加热,溶液颜色变深
溶液加热,溶液颜色变深 ,压缩容器体积增加压强,平衡体系颜色变深
,压缩容器体积增加压强,平衡体系颜色变深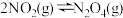 ,扩大容器体积,平衡逆向移动,所以平衡体系颜色变深
,扩大容器体积,平衡逆向移动,所以平衡体系颜色变深 ,为使氨的产率提高,理论上应采取高温高压的措施
,为使氨的产率提高,理论上应采取高温高压的措施



