锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态 Ge 原子的简化电子排布式为_______ 。
(2)Ge 与 C 是同族元素,C 原子之间可以形成双键、三键,但 Ge 原子之间难以形成双键或三键。从原子结构角度分析,原因是_______ 。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_______ 。
(4)Ge 单晶具有金刚石型结构,其中 Ge 原子的杂化方式为_______ ,微粒之间存在的作用力是_______ 。
(5)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,下图为 Ge 单晶的晶胞,其中原子坐标参数 A 为(0, 0,0);B 为(1/2 ,0,1/2);C 为(1/2 ,1/2 ,0);则 D 原子的坐标参数为_______ 。与 C 原子最近的原子有_______ 个。
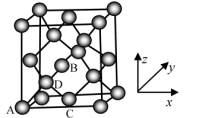
②晶胞参数,描述晶胞的大小和形状,已知 Ge 单晶的晶胞参数 a=565.76 pm,其密度为_______ g·cm-3(列出计算式即可)。
(1)基态 Ge 原子的简化电子排布式为
(2)Ge 与 C 是同族元素,C 原子之间可以形成双键、三键,但 Ge 原子之间难以形成双键或三键。从原子结构角度分析,原因是
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(5)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,下图为 Ge 单晶的晶胞,其中原子坐标参数 A 为(0, 0,0);B 为(1/2 ,0,1/2);C 为(1/2 ,1/2 ,0);则 D 原子的坐标参数为

②晶胞参数,描述晶胞的大小和形状,已知 Ge 单晶的晶胞参数 a=565.76 pm,其密度为
22-23高二上·广东广州·期末 查看更多[2]
广东实验中学、广州广雅中学、广州市执信中学、广州市第二中学、广州市第六中学五校2022-2023学年高二上学期期末联考化学试题(已下线)2023年高考浙江卷化学真题(6月)变式题(结构与性质)
更新时间:2023-01-09 18:58:00
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】CdSnAs2是一种高迁移率的新型热电材料。回答下列问题:
(1)砷和磷为同一主族的元素,则As的价层电子排布式为___________ ,第一电离能:磷___________ 砷(填“大于”、“小于”或“等于”)。
(2)SnCl4是制备有机锡化合物的原料,染色的媒染剂,缩合剂。SnCl4中锡原子的杂化方式为___________ ,SnCl4的空间结构为___________ (用文字描述)。
(3)砷化镉(Cd,As)是一种验证三维量子霍尔效应的材料。
①砷和卤素可形成多种卤化物,AsBr3、AsCl3、AsF3的熔点由低到高的顺序为___________
②砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是___________
③Cd2+与 形成配离子[Cd(NH3)4]2+中,中心离子的配位数为
形成配离子[Cd(NH3)4]2+中,中心离子的配位数为___________ ,画出配离子的结构式___________ (不考虑立体构型)。
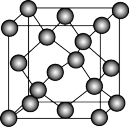
(4)灰锡的晶胞结构如图。已知:晶胞边长为648.9pm。晶体密度为5.75g•cm-3,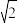 =1.414,
=1.414,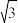 =1.732.则锡原子的半径为
=1.732.则锡原子的半径为___________ pm,锡的相对原子质量为___________ (只需写出计算表达式)。
(1)砷和磷为同一主族的元素,则As的价层电子排布式为
(2)SnCl4是制备有机锡化合物的原料,染色的媒染剂,缩合剂。SnCl4中锡原子的杂化方式为
(3)砷化镉(Cd,As)是一种验证三维量子霍尔效应的材料。
①砷和卤素可形成多种卤化物,AsBr3、AsCl3、AsF3的熔点由低到高的顺序为
②砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是
③Cd2+与
 形成配离子[Cd(NH3)4]2+中,中心离子的配位数为
形成配离子[Cd(NH3)4]2+中,中心离子的配位数为(4)灰锡的晶胞结构如图。已知:晶胞边长为648.9pm。晶体密度为5.75g•cm-3,
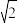 =1.414,
=1.414,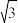 =1.732.则锡原子的半径为
=1.732.则锡原子的半径为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铜的化合物具有广泛的用途。
(1)Cu2+基态核外电子排布式为__________________ 。
(2)往硫酸铜溶液中加入过量氨水,溶液最终变成深蓝色,继续加入乙醇,可析出[Cu(NH3)4]SO4·H2O,N、O、S原子的第一电离能由大到小的顺序为__________________ ,与SO42-互为等电子体的分子的化学式为__ ,每个乙醇分子中sp3杂化的原子个数为_________________ 。
(3)铜的一种氧化物晶体结构如图所示,其中O原子的配位数为_________________ 。
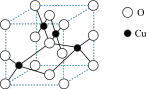
(4) Cu2O的熔点比Cu2S高的原因是__________________ 。
(1)Cu2+基态核外电子排布式为
(2)往硫酸铜溶液中加入过量氨水,溶液最终变成深蓝色,继续加入乙醇,可析出[Cu(NH3)4]SO4·H2O,N、O、S原子的第一电离能由大到小的顺序为
(3)铜的一种氧化物晶体结构如图所示,其中O原子的配位数为

(4) Cu2O的熔点比Cu2S高的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】钛镍形状记忆合金(TiNi)被广泛用于人造卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式:_________ ,Ni在元素周期表中的位置是_________ 。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为______ ,中心原子的轨道杂化类型是_______ 。
(3)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是____________ ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 _______________ 。
(4)一种钛镍合金的立方晶胞结构如图所示:
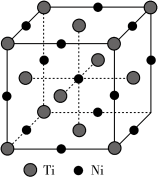
①该合金中Ti的配位数为________ 。
②若合金的密度为d g/cm3,晶胞边长a=________ pm。(用含d的计算式表示)
(1)写出基态Ti原子的电子排布式:
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为
(3)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是
(4)一种钛镍合金的立方晶胞结构如图所示:

①该合金中Ti的配位数为
②若合金的密度为d g/cm3,晶胞边长a=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为周期表的一部分,其中的编号代表对应的元素。请回答下列问题:
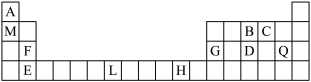
(1)表中属于ds区元素的是_______ (填元素符号)。BC 的
的 模型为
模型为_______ 。
(2)基态L原子的价电子排布图_______ ,同一周期且最外层电子数与L相同的元素有_______ 种。
(3)由A、B、C三元素形成的离子化合物中B原子的_______ 杂化轨道与A原子的_______ 轨道重叠形成_______ 键。
(4)上述元素中金属性最强的为_______ (填名称),其与C以原子个数比为1∶2形成化合物甲,则甲的电子式为_______ ,其中所含化学键类型为_______ 。
(5)工业上用电解法冶炼G的单质,阳极的电极反应式为_______ 。

(1)表中属于ds区元素的是
 的
的 模型为
模型为(2)基态L原子的价电子排布图
(3)由A、B、C三元素形成的离子化合物中B原子的
(4)上述元素中金属性最强的为
(5)工业上用电解法冶炼G的单质,阳极的电极反应式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】【化学一选修3:物质结构与性质】化学材料的研发和使用,为开发太阳能资源,寻求经济发展的新动力提供有力支撑。请根据你所学知识回答:
(1)太阳能热水器吸热涂层常使用一种以镍或镍合金空心球做吸收剂,则基态镍原子的外围电子排布式____________。
(2)由氧、镍和碳三种元素组成的化合物四碳基镍[Ni(CO)4]为无色挥发性剧毒液体,熔点-25℃,沸点43℃。不溶于水,易溶于乙醇、乙醚、苯、四氯化碳等有机溶剂,四碳基镍的晶体类型是_________,写出一种与配体等电子体的化学式___________________。
(3)三氟化氮在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应的化学方程式为3F2+4NH3=NF3+3NH4F,生成物NH4F固体所含化学键类型是_____________。往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_____________________。
(4)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硒化镓、硫化锌薄膜电池等。
①砷和稼的第一电离能关系为:As_____Ga(填“>”、“<”或“=”)
②SeO2分子的空间构型为________。
③硫化锌的晶胞结构如右图所示,锌离子的配位数是______。
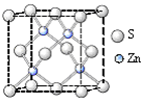
已知此晶胞立方体的边长为a pm ,晶体的密度为ρg/cm3,则阿伏加德罗常数可表示为__________mol-1(用含a、ρ的代数式表示)。
(1)太阳能热水器吸热涂层常使用一种以镍或镍合金空心球做吸收剂,则基态镍原子的外围电子排布式____________。
(2)由氧、镍和碳三种元素组成的化合物四碳基镍[Ni(CO)4]为无色挥发性剧毒液体,熔点-25℃,沸点43℃。不溶于水,易溶于乙醇、乙醚、苯、四氯化碳等有机溶剂,四碳基镍的晶体类型是_________,写出一种与配体等电子体的化学式___________________。
(3)三氟化氮在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应的化学方程式为3F2+4NH3=NF3+3NH4F,生成物NH4F固体所含化学键类型是_____________。往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_____________________。
(4)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硒化镓、硫化锌薄膜电池等。
①砷和稼的第一电离能关系为:As_____Ga(填“>”、“<”或“=”)
②SeO2分子的空间构型为________。
③硫化锌的晶胞结构如右图所示,锌离子的配位数是______。

已知此晶胞立方体的边长为a pm ,晶体的密度为ρg/cm3,则阿伏加德罗常数可表示为__________mol-1(用含a、ρ的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】教材插图是对教材内容高度概括的体现,也是为说明、理解、深化文字内容服务的。请回答下列问题:
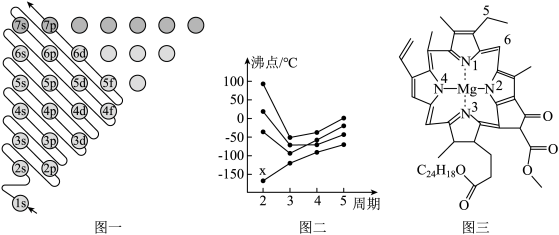
(1)图一为构造原理示意图,其含义是从H原子开始随着原子核电荷数递增,原子核每增加一个质子,核外便增加一个电子,电子大多按如图顺序填充。第四周期中,基态4s能级半充满的元素有___ 种,其中原子序数最大的基态原子的外围电子排布式为___ 。
(2)图二中,每条折线代表周期表中IVA-VIIA某一族元素简单氢化物的沸点变化,其他三条折线与x所在折线变化趋势不完全相同的原因为___ ;与x点对应的简单氢化物互为等电子体的离子为___ (写一种)。
(3)图三为卟啉配合物叶绿素的结构示意图,1号N原子和3号N原子与Mg2+形成的化学键类型为___ ;5号C原子和6号C原子的杂化方式分别为___ 、___ ;该分子中所含非金属元素的电负性由小到大的顺序为___ 。
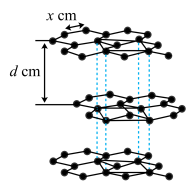
(4)从石墨晶体结构示意图中截取石墨的晶胞如图所示,设阿伏加 德罗常数为NA,已知sin60°= ),石墨晶体的密度为
),石墨晶体的密度为___ g·cm-3(列出计算式)。

(1)图一为构造原理示意图,其含义是从H原子开始随着原子核电荷数递增,原子核每增加一个质子,核外便增加一个电子,电子大多按如图顺序填充。第四周期中,基态4s能级半充满的元素有
(2)图二中,每条折线代表周期表中IVA-VIIA某一族元素简单氢化物的沸点变化,其他三条折线与x所在折线变化趋势不完全相同的原因为
(3)图三为卟啉配合物叶绿素的结构示意图,1号N原子和3号N原子与Mg2+形成的化学键类型为
(4)从石墨晶体结构示意图中截取石墨的晶胞如图所示,设阿伏加 德罗常数为NA,已知sin60°=
 ),石墨晶体的密度为
),石墨晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钙铜合金可用作电解法制备金属钙的阴极电极材料。回答下列问题:
(1)铜在元素周期表中位于_______ (填“s”、“p”、“d”或“ds”)区。
(2)基态Ca原子的价电子排布式为_______ 。Co与Ca位于同一周期,且最外层电子数相同,但金属Co的熔点、沸点均比金属Ca的高,原因是_______ 。
(3)硫酸铜稀溶液呈蓝色,则硫酸铜稀溶液中不存在的作用力有_______ (填标号),其中硫酸根的空间构型为_______ 。
A.配位键 B.金属键 C.共价键 D.氢键 E.范德华力
(4)Cu的一种配位化合物(Me为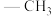 )的结构如图所示,其中Cu的配位数为
)的结构如图所示,其中Cu的配位数为_______ ,碳原子的杂化类型为_______ ,C、N、O的第一电离能从小到大的顺序是_______ (填元素符号)。
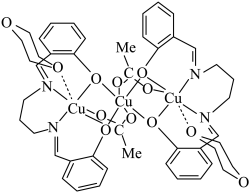
(5)一种钙铜合金的结构如图(III可看作是由I、II两种原子层交替堆积排列而形成的,其晶胞结构为IV)。
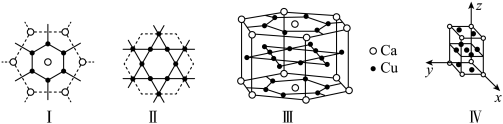
该钙铜合金中铜原子与钙原子的个数比为_______ ;晶体的坐标系称为晶轴系,晶轴系以晶胞参数为晶轴的单位向量如上图(IV),在图中画出上图(IV)中Cu原子沿z轴方向向x—y平面投影的位置_______ (用“ ”表示铜原子)。
”表示铜原子)。
(1)铜在元素周期表中位于
(2)基态Ca原子的价电子排布式为
(3)硫酸铜稀溶液呈蓝色,则硫酸铜稀溶液中不存在的作用力有
A.配位键 B.金属键 C.共价键 D.氢键 E.范德华力
(4)Cu的一种配位化合物(Me为
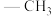 )的结构如图所示,其中Cu的配位数为
)的结构如图所示,其中Cu的配位数为
(5)一种钙铜合金的结构如图(III可看作是由I、II两种原子层交替堆积排列而形成的,其晶胞结构为IV)。

该钙铜合金中铜原子与钙原子的个数比为
 ”表示铜原子)。
”表示铜原子)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】GaN是制造5G芯片的材料,氮化镓铝和氮化铝LED可发出紫外光。回答下列问题:
(1)基态N原子核外电子排布式为__ ;下列状态的铝元素中,电离最外层的一个电子所需能量最小的是__ 。(填标号)
A.[Ne]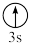 B.[Ne]
B.[Ne]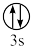 C.[Ne] D.[Ne]
C.[Ne] D.[Ne]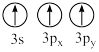
(2)8—羟基喳啉合铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与8—羟基噎啉)合成。LiAlH4中阴离子的中心原子Al的杂化方式为__ ;8—羟基喹啉合铝中所含元素电负性最大的是__ (填元素符号,下同),第一电离能最大的是__ (填元素符号)。
(3)已知下列化合物的熔点:
表格中卤化物的熔点产生差异的原因是__ 。
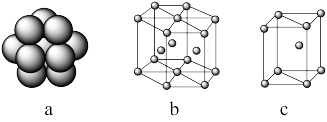
(4)镁单质晶体中原子的堆积模型为六方最密堆积(如图),紧邻的四个镁原子的中心连线构成的正四面体几何体的体积是2acm3,镁单质的密度为ρg•cm-3,已知阿伏加 德罗常数为NA,则镁的摩尔质量的计算式是__ 。
(1)基态N原子核外电子排布式为
A.[Ne]
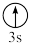 B.[Ne]
B.[Ne]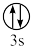 C.[Ne] D.[Ne]
C.[Ne] D.[Ne]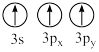
(2)8—羟基喳啉合铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与8—羟基噎啉)合成。LiAlH4中阴离子的中心原子Al的杂化方式为
(3)已知下列化合物的熔点:
| 化合物 | AlF3 | GaF3 | AlCl3 |
| 熔点/℃ | 1040 | 1000 | 194 |
表格中卤化物的熔点产生差异的原因是
(4)镁单质晶体中原子的堆积模型为六方最密堆积(如图),紧邻的四个镁原子的中心连线构成的正四面体几何体的体积是2acm3,镁单质的密度为ρg•cm-3,已知阿伏加 德罗常数为NA,则镁的摩尔质量的计算式是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
真题
解题方法
【推荐3】C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Ge的原子核外电子排布式为____________ 。
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是___________ 。
(3)按要求指出下列氧化物的空间构型、成键方式或性质。
①CO2分子的空间构型及碳氧之间的成键方式___________ ;
②SiO2晶体的空间构型及硅氧之间的成键方式___________ 。;
③已知SnO2是离子晶体,写出其主要物理性质___________ (写出2条即可)
(4)CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为_______ 。
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度______ (填字母)
A.强 B.弱 C.相等 D.无法判断
(1)Ge的原子核外电子排布式为
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是
(3)按要求指出下列氧化物的空间构型、成键方式或性质。
①CO2分子的空间构型及碳氧之间的成键方式
②SiO2晶体的空间构型及硅氧之间的成键方式
③已知SnO2是离子晶体,写出其主要物理性质
(4)CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度
A.强 B.弱 C.相等 D.无法判断
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】使用铜基催化剂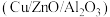 ,以
,以 和
和 合成
合成 是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:
是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:
(1) 的
的 模型名称是
模型名称是___________ , 分子中O的杂化轨道类型是
分子中O的杂化轨道类型是___________ 。
(2)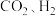 和
和 中,属于极性分子的是
中,属于极性分子的是___________ ,由非极性键结合成的非极性分子是___________ 。
(3) 的沸点
的沸点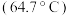 介于
介于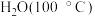 和
和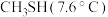 之间,其原因是
之间,其原因是___________ 。
(4) 属于
属于___________ 晶体, 属于
属于___________ 晶体。
(5) 的一种立方晶胞结构如图所示,每个
的一种立方晶胞结构如图所示,每个 周围与它最近且相等距离的
周围与它最近且相等距离的 有
有___________ 个。若该立方晶胞参数为 ,则正负离子的核间距最小为
,则正负离子的核间距最小为___________  ,晶体密度
,晶体密度
___________  (列出算式,阿伏加德罗常数的值为
(列出算式,阿伏加德罗常数的值为 )。
)。
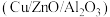 ,以
,以 和
和 合成
合成 是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:
是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:(1)
 的
的 模型名称是
模型名称是 分子中O的杂化轨道类型是
分子中O的杂化轨道类型是(2)
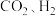 和
和 中,属于极性分子的是
中,属于极性分子的是(3)
 的沸点
的沸点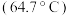 介于
介于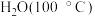 和
和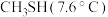 之间,其原因是
之间,其原因是(4)
 属于
属于 属于
属于(5)
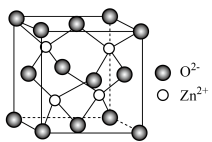
 的一种立方晶胞结构如图所示,每个
的一种立方晶胞结构如图所示,每个 周围与它最近且相等距离的
周围与它最近且相等距离的 有
有 ,则正负离子的核间距最小为
,则正负离子的核间距最小为 ,晶体密度
,晶体密度
 (列出算式,阿伏加德罗常数的值为
(列出算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁和氮是化学学习中的重要元素,高附加值的铁和氮的化合物也逐渐融入我们的学习和生活中。
Ⅰ、富马酸亚铁(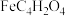 )是一种补铁剂,富马酸分子结构模型如图:
)是一种补铁剂,富马酸分子结构模型如图:
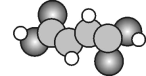
(1)基态铁原子的价电子排布式是_____ 。
(2)由富马酸分子的结构模型可知其结构简式为 ,则富马酸分子中
,则富马酸分子中 键与
键与 键的数目比为
键的数目比为_____ 。
Ⅱ、磷酸铁锂( )电池是绿色环保型电池
)电池是绿色环保型电池
(3)Fe、P、O三种元素电负性从大到小的顺序是_____ 。
(4)写出一种与 互为等电子体的分子
互为等电子体的分子_____ (填化学式)。
(5)磷酸铁锂( )电池的负极材料是镶嵌了
)电池的负极材料是镶嵌了 的石墨,
的石墨, 嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为
嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为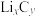 的嵌入化合物,平面结构如图所示,则
的嵌入化合物,平面结构如图所示,则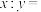
_____ 。

Ⅲ、雷氏盐是分析化学中常用的试剂,其化学式为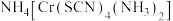 。
。
(6) 的沸点比
的沸点比 高的主要原因是
高的主要原因是_____ , 分子易与
分子易与 形成配离子,而
形成配离子,而 不易形成配离子的原因是
不易形成配离子的原因是_____ 。
(7)雷氏盐中阳离子的空间结构为_____ (填字母,下同),阴离子的空间结构最可能的是_____ 。
Ⅰ、富马酸亚铁(
 )是一种补铁剂,富马酸分子结构模型如图:
)是一种补铁剂,富马酸分子结构模型如图:
(1)基态铁原子的价电子排布式是
(2)由富马酸分子的结构模型可知其结构简式为
 ,则富马酸分子中
,则富马酸分子中 键与
键与 键的数目比为
键的数目比为Ⅱ、磷酸铁锂(
 )电池是绿色环保型电池
)电池是绿色环保型电池(3)Fe、P、O三种元素电负性从大到小的顺序是
(4)写出一种与
 互为等电子体的分子
互为等电子体的分子(5)磷酸铁锂(
 )电池的负极材料是镶嵌了
)电池的负极材料是镶嵌了 的石墨,
的石墨, 嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为
嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为 的嵌入化合物,平面结构如图所示,则
的嵌入化合物,平面结构如图所示,则

Ⅲ、雷氏盐是分析化学中常用的试剂,其化学式为
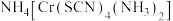 。
。(6)
 的沸点比
的沸点比 高的主要原因是
高的主要原因是 分子易与
分子易与 形成配离子,而
形成配离子,而 不易形成配离子的原因是
不易形成配离子的原因是(7)雷氏盐中阳离子的空间结构为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】A、B、C、D为前四周期元素.A元素的原子价电子排布为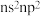 ,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P轨道中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P轨道中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
 当
当 时,
时,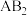 属于
属于 ______ 分子 填“极性”或“非极性”
填“极性”或“非极性” .
.
 当
当 时,A与B形成的晶体属于
时,A与B形成的晶体属于 ______ 晶体.
 若A元素的原子价电子排布为
若A元素的原子价电子排布为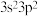 ,A、C、D三种元素的第一电离能由大到小的顺序是
,A、C、D三种元素的第一电离能由大到小的顺序是 ______  用元素符号表示
用元素符号表示 。
。
 已知某红紫色配合物的组成为
已知某红紫色配合物的组成为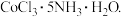 该配合物中的中心离子钴离子在基态时核外电子排布式为
该配合物中的中心离子钴离子在基态时核外电子排布式为 ______ ,又已知中心离子钴离子的配位数是6,1mol该物质与足量的硝酸银反应可生成3molAgCl,则该物质化学式是 ______ 。
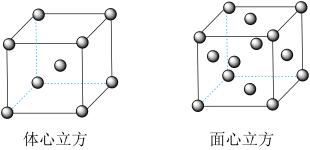
 金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为
金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为 ______ 。
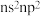 ,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P轨道中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P轨道中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。  当
当 时,
时,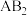 属于
属于  填“极性”或“非极性”
填“极性”或“非极性” .
. 当
当 时,A与B形成的晶体属于
时,A与B形成的晶体属于  若A元素的原子价电子排布为
若A元素的原子价电子排布为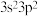 ,A、C、D三种元素的第一电离能由大到小的顺序是
,A、C、D三种元素的第一电离能由大到小的顺序是  用元素符号表示
用元素符号表示 。
。 已知某红紫色配合物的组成为
已知某红紫色配合物的组成为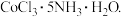 该配合物中的中心离子钴离子在基态时核外电子排布式为
该配合物中的中心离子钴离子在基态时核外电子排布式为  金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为
金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为 
您最近一年使用:0次



