工业制硫酸的重要反应: ,下列做法能用勒夏特列原理解释的是
,下列做法能用勒夏特列原理解释的是
 ,下列做法能用勒夏特列原理解释的是
,下列做法能用勒夏特列原理解释的是| A.保持体系较高的反应温度 | B.实际生产中 与 与 的体积比为1:50 的体积比为1:50 |
| C.选择常压为反应条件 | D.原料需要净化、干燥,防止催化剂中毒 |
22-23高二上·浙江杭州·期末 查看更多[4]
浙江省杭州第二中学东河校区2023-2024学年高二上学期期末考试化学试题(已下线)【2023】【高二上】【余高】【期末考】【高中化学】【朱奎正收集】浙江省杭州市八区县2022-2023学年高二上学期期末检测化学试题浙江省杭州市临平区2022-2023学年高二上学期期未学业水平测试化学试题
更新时间:2023-02-09 16:04:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在密闭容器中发生如下反应: ,反应达到平衡后保持温度不变,将气体体积压缩到原来的
,反应达到平衡后保持温度不变,将气体体积压缩到原来的 ,当再次达到平衡时,W的浓度为原平衡时的1.8倍.下列叙述中不正确的是
,当再次达到平衡时,W的浓度为原平衡时的1.8倍.下列叙述中不正确的是
 ,反应达到平衡后保持温度不变,将气体体积压缩到原来的
,反应达到平衡后保持温度不变,将气体体积压缩到原来的 ,当再次达到平衡时,W的浓度为原平衡时的1.8倍.下列叙述中不正确的是
,当再次达到平衡时,W的浓度为原平衡时的1.8倍.下列叙述中不正确的是| A.平衡向逆反应方向移动 | B.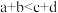 |
| C.Z的体积分数增大 | D.X的转化率下降 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某温度下,反应N2O4(g) 2NO2(g)△H>0,在密闭容器中达到平衡。下列说法不正确的是
2NO2(g)△H>0,在密闭容器中达到平衡。下列说法不正确的是
 2NO2(g)△H>0,在密闭容器中达到平衡。下列说法不正确的是
2NO2(g)△H>0,在密闭容器中达到平衡。下列说法不正确的是| A.加压时(体积变小),将使正反应速率增大 |
| B.保持体积不变,升高温度,再达平衡时颜色变深 |
| C.保持体积不变,加入少许N2O4,再达到平衡时,颜色变深 |
| D.保持体积不变,加入少许NO2,将使正反应速率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
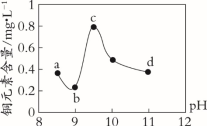
【推荐1】某电路板生产企业的水质情况及国家允许排放的污水标准如下表所示。为研究废水中Cu2+处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。
查阅资料,平衡I:Cu(OH)2 + 4NH3 [Cu(NH3)4]2+ + 2OH-;
[Cu(NH3)4]2+ + 2OH-;
平衡II:Cu(OH)2 + 2OH- [Cu(OH-)4]2-
[Cu(OH-)4]2-
下列说法不正确 的是

查阅资料,平衡I:Cu(OH)2 + 4NH3
 [Cu(NH3)4]2+ + 2OH-;
[Cu(NH3)4]2+ + 2OH-;平衡II:Cu(OH)2 + 2OH-
 [Cu(OH-)4]2-
[Cu(OH-)4]2-| 项目 | 废水水质 | 排放标准 |
| pH | 1.0 | 6~9 |
| Cu2+/ mg·L-1 | 72 | ≤0.5 |
| NH4+/ mg·L-1 | 2632 | ≤15 |
下列说法
| A.废水中Cu2+处理的最佳pH约为9 |
| B.b~c段:随pH升高,Cu(OH)2的量增加,平衡I正向移动,铜元素含量上升 |
| C.c~d段:随pH升高,c(OH-)增加,平衡I逆向移动,铜元素含量下降 |
| D.d点以后,随c(OH-)增加,铜元素含量可能上升 |
您最近一年使用:0次
单选题
|
适中
(0.65)
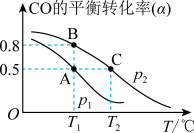
【推荐2】CO可用于合成甲醇,其反应的化学方程式为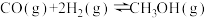 。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法
。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法不正确 的是
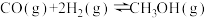 。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法
。一容积可变的密闭容器中充有10 molCO与20 mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)压强(p)的关系如图所示。下列说法
| A.合成甲醇的反应为放热反应 |
| B.压强为P1<P2 |
| C.A、B、C三点的平衡常数为KA=KB>KC |
| D.A点的v正和C点的v逆相等 |
您最近一年使用:0次

 ,碳的质量不再改变说明反应已达平衡
,碳的质量不再改变说明反应已达平衡 ,其他条件不变,缩小反应容器体积,正逆反应速率不变
,其他条件不变,缩小反应容器体积,正逆反应速率不变 已经平衡,则A、C不能同时是气体
已经平衡,则A、C不能同时是气体 ,达到平衡状态后向容器中再充入0.10 mol NO,再次平衡时NO的体积分数将增大
,达到平衡状态后向容器中再充入0.10 mol NO,再次平衡时NO的体积分数将增大

