变色硅胶干燥剂含有 ,根据颜色可判断干燥剂是否已经失效。已知
,根据颜色可判断干燥剂是否已经失效。已知 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色, 为无色。现将
为无色。现将 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: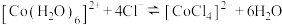
 ,将该溶液分为三份做实验,溶液的颜色变化如下:
,将该溶液分为三份做实验,溶液的颜色变化如下:
以下结论或解释正确的是
 ,根据颜色可判断干燥剂是否已经失效。已知
,根据颜色可判断干燥剂是否已经失效。已知 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色, 为无色。现将
为无色。现将 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: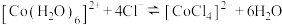
 ,将该溶液分为三份做实验,溶液的颜色变化如下:
,将该溶液分为三份做实验,溶液的颜色变化如下:| 装置 | 序号 | 操作 | 现象 |
 | ① | 将试管置于冰水浴中 | 溶液均呈粉红色 |
| ② | 加水稀释 | ||
| ③ | 加少量 固体 固体 |
A.由实验①可知: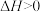 |
| B.由实验②可推知加水稀释,浓度商Q<K,平衡逆向移动 |
C.由实验③可知: 络合 络合 能力比 能力比 络合 络合 能力弱 能力弱 |
D.变色硅胶干燥剂含有 主要起干燥作用 主要起干燥作用 |
更新时间:2023-02-12 17:03:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列事实能用勒夏特列原理来解释的是
A.SO2被氧化为SO3,往往需要使用催化剂:2SO2(g)+O2(g) 2SO3(g) 2SO3(g) |
B.500℃左右的温度比室温更有利于合成氨反应:N2(g)+3H2(g) 2NH3(g)ΔH<0 2NH3(g)ΔH<0 |
| C.实验室采用排饱和食盐水的方法收集氯 |
D.H2、I2、HI平衡混合气体加压后颜色加深:H2(g)+I2(g) 2HI(g) 2HI(g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡: (橙色)+ H2O⇌2H++ 2
(橙色)+ H2O⇌2H++ 2 (黄色)
(黄色)
①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。
②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应: + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
+ 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
下列分析正确的是
 (橙色)+ H2O⇌2H++ 2
(橙色)+ H2O⇌2H++ 2 (黄色)
(黄色)①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。
②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:
 + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
+ 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。下列分析正确的是
| A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡 |
B.实验②能说明氧化性: >Fe3+ >Fe3+ |
C. 和Fe2+在酸性溶液中可以大量共存 和Fe2+在酸性溶液中可以大量共存 |
| D.向K2Cr2O7溶液中加入水时,平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验目的、实验操作及现象、结论均正确的是
| 选项 | 实验目的 | 实验操作及现象 | 结论 |
| A | 判断强酸和弱酸 |  溶液显碱性, 溶液显碱性, 溶液显酸性 溶液显酸性 | 可以确定 是弱酸,无法判断 是弱酸,无法判断 是否为弱酸 是否为弱酸 |
| B | 判断反应物的浓度对平衡的影响 | 向 溶液中加入 溶液中加入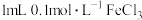 溶液,达到平衡,再加入 溶液,达到平衡,再加入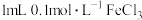 溶液,溶液红色加深 溶液,溶液红色加深 | 说明增大反应物浓度,化学平衡正向移动 |
| C | 验证 的氧化性 的氧化性 | 向黄绿色的氯水中加入 溶液,溶液黄绿色褪去 溶液,溶液黄绿色褪去 |  有强氧化性 有强氧化性 |
| D | 验证菠菜中含有铁元素 | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入几滴KSCN溶液,溶液不变红 | 说明菠菜中不含铁元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】若在催化剂作用下 和
和 合成甲酸主要涉及以下反应:
合成甲酸主要涉及以下反应:
I.
II.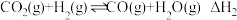
在 恒容密闭容器中,
恒容密闭容器中, 和
和 各投
各投 发生反应,平衡时
发生反应,平衡时 的转化率及
的转化率及 和
和 的选择性(产物的选择性:生成的
的选择性(产物的选择性:生成的 或
或 与转化的
与转化的 的比值)随温度变化如图所示。
的比值)随温度变化如图所示。
下列说法正确的是

 和
和 合成甲酸主要涉及以下反应:
合成甲酸主要涉及以下反应:I.

II.
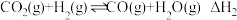
在
 恒容密闭容器中,
恒容密闭容器中, 和
和 各投
各投 发生反应,平衡时
发生反应,平衡时 的转化率及
的转化率及 和
和 的选择性(产物的选择性:生成的
的选择性(产物的选择性:生成的 或
或 与转化的
与转化的 的比值)随温度变化如图所示。
的比值)随温度变化如图所示。下列说法正确的是

A.反应II: |
B.曲线a表示平衡时 的转化率 的转化率 |
C. 时,反应I的平衡常数 时,反应I的平衡常数 |
| D.合成甲酸应选择在较高温度下甲酸选择性高的催化剂 |
您最近一年使用:0次
【推荐2】工业上由焦炭和 在高温反应制得CO。现将焦炭和
在高温反应制得CO。现将焦炭和 放入体积为2L的密闭容器中,高温下进行下列反应:
放入体积为2L的密闭容器中,高温下进行下列反应: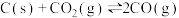
 ,下图为
,下图为 、
、 的物质的量n随时间t的变化关系图。下列说法正确的是
的物质的量n随时间t的变化关系图。下列说法正确的是

 在高温反应制得CO。现将焦炭和
在高温反应制得CO。现将焦炭和 放入体积为2L的密闭容器中,高温下进行下列反应:
放入体积为2L的密闭容器中,高温下进行下列反应: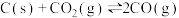
 ,下图为
,下图为 、
、 的物质的量n随时间t的变化关系图。下列说法正确的是
的物质的量n随时间t的变化关系图。下列说法正确的是
A.0~1min, ;1~3min时, ;1~3min时, |
B.当容器内的气体压强不变时,反应一定达到平衡状态且 |
| C.5min时再充入一定量的CO,a、d曲线分别表示n(CO)、n(CO2)的变化 |
D.若3min时改变的条件是温度,可推知 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应:H2NCOONH4(s) 2NH3(g)+CO2(g),在不同温度下,该反应达平衡状态时的部分数据如表所示。下列说法正确的是( )
2NH3(g)+CO2(g),在不同温度下,该反应达平衡状态时的部分数据如表所示。下列说法正确的是( )
 2NH3(g)+CO2(g),在不同温度下,该反应达平衡状态时的部分数据如表所示。下列说法正确的是( )
2NH3(g)+CO2(g),在不同温度下,该反应达平衡状态时的部分数据如表所示。下列说法正确的是( )| 温度 | 平衡浓度(mol·L-1) | |
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | 0.1 | |
| A.若T2>T1,则该反应的ΔH<0 |
| B.向容器中充入N2,H2NCOONH4质量增加 |
| C.NH3体积分数不变时,说明该反应达到平衡 |
| D.T1、T2时,转化的H2NCOONH4的物质的量Δn(T2)=2Δn(T1) |
您最近一年使用:0次



