若在催化剂作用下 和
和 合成甲酸主要涉及以下反应:
合成甲酸主要涉及以下反应:
I.
II.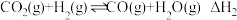
在 恒容密闭容器中,
恒容密闭容器中, 和
和 各投
各投 发生反应,平衡时
发生反应,平衡时 的转化率及
的转化率及 和
和 的选择性(产物的选择性:生成的
的选择性(产物的选择性:生成的 或
或 与转化的
与转化的 的比值)随温度变化如图所示。
的比值)随温度变化如图所示。
下列说法正确的是

 和
和 合成甲酸主要涉及以下反应:
合成甲酸主要涉及以下反应:I.

II.
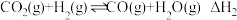
在
 恒容密闭容器中,
恒容密闭容器中, 和
和 各投
各投 发生反应,平衡时
发生反应,平衡时 的转化率及
的转化率及 和
和 的选择性(产物的选择性:生成的
的选择性(产物的选择性:生成的 或
或 与转化的
与转化的 的比值)随温度变化如图所示。
的比值)随温度变化如图所示。下列说法正确的是

A.反应II: |
B.曲线a表示平衡时 的转化率 的转化率 |
C. 时,反应I的平衡常数 时,反应I的平衡常数 |
| D.合成甲酸应选择在较高温度下甲酸选择性高的催化剂 |
21-22高二下·江苏徐州·期末 查看更多[5]
江苏省徐州市2021-2022学年高二下学期期末抽测化学试题(已下线)2.4 化学反应的调控-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)江苏省句容高级中学、句容市第三中学等三校2022-2023学年高二10月学情检测调研化学试题江苏省苏州市南京航空航天大学苏州附属中学2022-2023学年高二上学期12月月考化学试题山西大学附属中学校2023-2024学年高二上学期10月模块诊断化学试题
更新时间:2022-06-28 22:20:33
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中,不能用勒夏特列原理解释的是
| A.向K2Cr2O4溶液中滴入浓的NaOH溶液后,溶液黄色加深 |
| B.高压比常压更有利于合成SO3 |
C.反应2SO2+O2 2SO3 ΔH<0,工业上采取高温的措施有利于提高SO2的转化率 2SO3 ΔH<0,工业上采取高温的措施有利于提高SO2的转化率 |
D.合成氨反应:N2+3H2 2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施 2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施 |
您最近一年使用:0次
【推荐2】一定条件下,将N2与H2物质的量各1mol置于1L恒容的密闭容器中发生反应,到平衡时容器内的总压强变成了原来的4/5,下列说法不正确的是
| A.氮气的转化率是80% |
| B.氮气剩余体积占总体积的50% |
| C.该反应的平衡常数是3.125 |
| D.该反应随温度升高平衡会向逆反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应: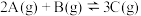
 ,若经2s后平衡,测得
,若经2s后平衡,测得 的体积分数为50%,下列说法中正确的是
的体积分数为50%,下列说法中正确的是
①2s内,用A表示的平均速率为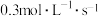
②平衡时物质A的转化率为50%
③平衡时物质B的浓度为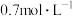
④平衡常数为6.75
⑤在绝热恒容条件下,当容器中气体总压强恒定时,可判断反应达到平衡状态
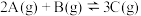
 ,若经2s后平衡,测得
,若经2s后平衡,测得 的体积分数为50%,下列说法中正确的是
的体积分数为50%,下列说法中正确的是①2s内,用A表示的平均速率为
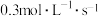
②平衡时物质A的转化率为50%
③平衡时物质B的浓度为
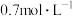
④平衡常数为6.75
⑤在绝热恒容条件下,当容器中气体总压强恒定时,可判断反应达到平衡状态
| A.②④⑤ | B.①③ | C.②③⑤ | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一恒容密闭容器中发生反应: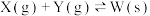
 ,
, ℃时,
℃时,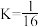 ,按不同配比充入
,按不同配比充入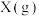 、
、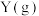 ,容器中
,容器中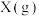 、
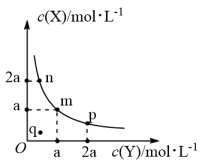
、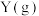 的平衡浓度如图所示,下列说法正确的是
的平衡浓度如图所示,下列说法正确的是
 ,
, ℃时,
℃时,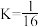 ,按不同配比充入
,按不同配比充入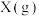 、
、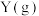 ,容器中
,容器中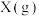 、
、 的平衡浓度如图所示,下列说法正确的是
的平衡浓度如图所示,下列说法正确的是
A.若q点为 ℃时的平衡点,则 ℃时的平衡点,则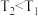 |
B. 点为该反应进行到 点为该反应进行到 时的平衡点,则 时的平衡点,则 内 内 |
C. 点时, 点时, 的转化率为50% 的转化率为50% |
D. 、 、 、 、 三点的 三点的 依次减小 依次减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】TK时,现有25mL含KCl和KCN的溶液,用0.1000mol•L-1的硝酸银标准溶液对该混合液进行电位滴定(CN-与H+的反应可以忽略),获得电动势(E)和硝酸银标准溶液体积(V)的电位滴定曲线如图所示:

已知:Ⅰ.Ag+与CN-反应过程为:①Ag++2CN-=[Ag(CN)2]-②[Ag(CN)2]-+Ag+=2AgCN↓。
Ⅱ.TK时,Ksp(AgCN)=2×10-l6,Ksp(AgCl)=2×10-10。
Ⅲ.电极电位E发生突跃时,说明滴定到达终点,即曲线上的转折点为化学计量点。
下列说法正确的是

已知:Ⅰ.Ag+与CN-反应过程为:①Ag++2CN-=[Ag(CN)2]-②[Ag(CN)2]-+Ag+=2AgCN↓。
Ⅱ.TK时,Ksp(AgCN)=2×10-l6,Ksp(AgCl)=2×10-10。
Ⅲ.电极电位E发生突跃时,说明滴定到达终点,即曲线上的转折点为化学计量点。
下列说法正确的是
| A.在A点,生成AgCN的物质的量为0.025mol |
| B.c(KCN)=0.02000mol•L-1,c(KCl)=0.03000mol•L-1 |
| C.反应①的平衡常数为K1,反应②的平衡常数为K2,则K1×K2=2Ksp(AgCN) |
| D.将AgCN饱和溶液和AgCl饱和溶液等体积混合,加入足量硝酸银溶液,析出固体AgCN多与AgCl |
您最近一年使用:0次

 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)

