合成NH3是重要的研究课题,一种合成NH3的流程示意如图。
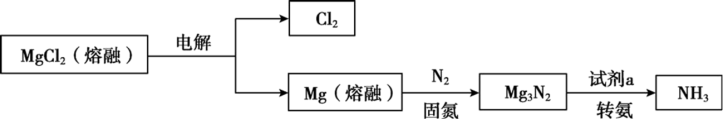
相关数据如表:
已知:Mg3N2溶于水发生反应Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
I.固氮:
(1)从结构上解释N2化学性质稳定的原因_____ 。上述固氮反应的化学方程式是_____ 。固氮的适宜温度范围是_____ 。(填编号)
a.500~600℃ b.700~800℃ c.900~1000℃
(2)检测固氮作用:向固氮后的产物中加水,_____ (填操作和现象),说明Mg能起到固氮作用。
II.转氨:选用试剂a完成转化。
(3)选用H2O进行转化,发现从体系中分离出NH3较困难,若选用HCl气体进行转化,发现能产生NH3,且产物MgCl2能直接循环利用,但NH3的收率较低,原因是_____ 。
活性炭还原NO2的原理为2NO2(g)+2C(s) N2(g)+2CO2(g)。一定温度下,在2L恒容密闭容器中充入1molNO2和足量C发生该反应(不考虑2NO2
N2(g)+2CO2(g)。一定温度下,在2L恒容密闭容器中充入1molNO2和足量C发生该反应(不考虑2NO2 N2O4)。实验测得NO2的转化率与时间的关系如图所示:
N2O4)。实验测得NO2的转化率与时间的关系如图所示:
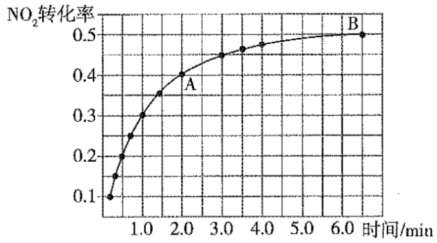
(4)反应达到平衡时CO2的体积分数为_____ ,混合气体的平均摩尔质量 (A)
(A)_____  (B)(填“大于”“小于”或“等于”)。
(B)(填“大于”“小于”或“等于”)。
(5)下列能够判断该反应已达到平衡状态的是_____ 。(填序号)
a.CO2的质量分数保持不变
b.容器中N2与CO2的百分含量之比保持不变
c.2v(逆)(NO2)=V(正)(N2)
d.混合气体的颜色保持不变

相关数据如表:
| 物质 | 熔点/℃ | 沸点/℃ | 与N2反应温度/℃ | 分解温度/℃ |
| Mg | 649 | 1090 | >300 | Mg3N2:>800 |
已知:Mg3N2溶于水发生反应Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
I.固氮:
(1)从结构上解释N2化学性质稳定的原因
a.500~600℃ b.700~800℃ c.900~1000℃
(2)检测固氮作用:向固氮后的产物中加水,
II.转氨:选用试剂a完成转化。
(3)选用H2O进行转化,发现从体系中分离出NH3较困难,若选用HCl气体进行转化,发现能产生NH3,且产物MgCl2能直接循环利用,但NH3的收率较低,原因是
活性炭还原NO2的原理为2NO2(g)+2C(s)
 N2(g)+2CO2(g)。一定温度下,在2L恒容密闭容器中充入1molNO2和足量C发生该反应(不考虑2NO2
N2(g)+2CO2(g)。一定温度下,在2L恒容密闭容器中充入1molNO2和足量C发生该反应(不考虑2NO2 N2O4)。实验测得NO2的转化率与时间的关系如图所示:
N2O4)。实验测得NO2的转化率与时间的关系如图所示:
(4)反应达到平衡时CO2的体积分数为
 (A)
(A) (B)(填“大于”“小于”或“等于”)。
(B)(填“大于”“小于”或“等于”)。(5)下列能够判断该反应已达到平衡状态的是
a.CO2的质量分数保持不变
b.容器中N2与CO2的百分含量之比保持不变
c.2v(逆)(NO2)=V(正)(N2)
d.混合气体的颜色保持不变
更新时间:2023-02-22 19:54:02
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示。
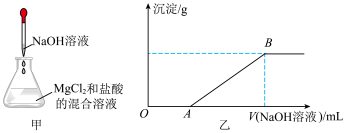
请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有___ 。
A.天平 B.烧杯 C.漏斗 D.玻璃棒
(2)OA段反应的离子方程式为___ 。
(3)AB段反应的离子方程式为___ 。
(4)B点对应的溶液中的溶质为___ ,往B点溶液中滴加AgNO3溶液,发生反应的离子方程式为___ 。

请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有
A.天平 B.烧杯 C.漏斗 D.玻璃棒
(2)OA段反应的离子方程式为
(3)AB段反应的离子方程式为
(4)B点对应的溶液中的溶质为
您最近一年使用:0次
【推荐2】以菱镁矿(主要成分为MgCO3,含少量FeCO3等)为原料制备高纯氧化镁的流程如图:
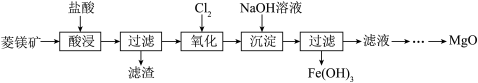
(1)采用搅拌、___ 、___ 适当增大盐酸的浓度等措施可以提高“酸浸”率。
(2)“氧化”过程中发生反应的化学方程式为___ 。
(3)“沉淀”时需严格控制NaOH溶液的用量,其目的是___ 。
(4)“滤液”中继续加入NaOH溶液,___ 、___ 、灼烧,制得氧化镁。
(5)工业可用氯化镁和碳酸铵为原料,采用直接沉淀法制备纳米MgO。取少量制得的该物质溶于某种液体溶剂中(两者不反应),能说明有纳米MgO存在的简单方法是___ 。

(1)采用搅拌、
(2)“氧化”过程中发生反应的化学方程式为
(3)“沉淀”时需严格控制NaOH溶液的用量,其目的是
(4)“滤液”中继续加入NaOH溶液,
(5)工业可用氯化镁和碳酸铵为原料,采用直接沉淀法制备纳米MgO。取少量制得的该物质溶于某种液体溶剂中(两者不反应),能说明有纳米MgO存在的简单方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子,并尽可能减少AlCl3的损失.请回答下列问题:
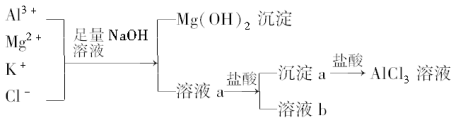
(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:________ 、________ 、________ .氢氧化钠溶液能否用氨水代替,为什么?______________________ .
(2)溶液a中存在的离子有________ ;在溶液a中加入盐酸时需控制溶液的pH,为什么?________ ;为此,改进方法是____________________ .
(3)为了研究AlCl3晶体的性质,在得到AlCl3溶液后,如何得到AlCl3晶体?____________________ .

(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:
(2)溶液a中存在的离子有
(3)为了研究AlCl3晶体的性质,在得到AlCl3溶液后,如何得到AlCl3晶体?
您最近一年使用:0次
【推荐1】随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了普遍关注,目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图所示。
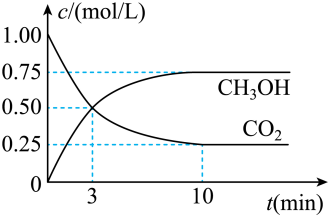
(1)应开始到平衡,H2的平均反应速率v(H2)=___________ mol/(L·min),H2的转化率为___________ 。
(2)能判断该反应是否达到化学平衡状态的依据是___________ 。
a.容器中压强不变 b.混合气体中c(CO2)=c(H2O)
c.混合气体的平均分子量不变 d.混合气体的密度不变
(3)下列措施中能使活化分子百分数增大的是___________ 。
A.升高温度 B.增大反应物浓度 C.增大压强 D.使用正催化剂
(4)一种新型燃料电池,一极通入空气,另一极通入甲醇气体;燃料电池内部是熔融的K2CO3,在其内部可以传导CO 。在电池内部CO
。在电池内部CO 移向
移向___________ ,该电池的负极反应为___________ 。
(5)氮氧化物的污染也受到高度重视,硝酸厂常用催化还原法处理尾气:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.5kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+133kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是___________ 。
 CH3OH(g)+H2O(g) △H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(1)应开始到平衡,H2的平均反应速率v(H2)=
(2)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中c(CO2)=c(H2O)
c.混合气体的平均分子量不变 d.混合气体的密度不变
(3)下列措施中能使活化分子百分数增大的是
A.升高温度 B.增大反应物浓度 C.增大压强 D.使用正催化剂
(4)一种新型燃料电池,一极通入空气,另一极通入甲醇气体;燃料电池内部是熔融的K2CO3,在其内部可以传导CO
 。在电池内部CO
。在电池内部CO 移向
移向(5)氮氧化物的污染也受到高度重视,硝酸厂常用催化还原法处理尾气:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.5kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+133kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】消除氮氧化物污染对优化环境至关重要。
(1)用 催化还原
催化还原 消除氮氧化物污染的变化如下:
消除氮氧化物污染的变化如下:
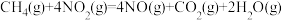
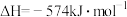

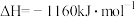
若用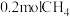 还原
还原 至
至 ,整个过程中放出的热量为
,整个过程中放出的热量为___________ kJ。(假设水全部以气态形成存在)
(2)活性炭(C)可处理大气污染物NO。在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F,当温度分别在 和
和 时,测得各物质平衡时物质的量如下表:
时,测得各物质平衡时物质的量如下表:
①根据上表数据,可推测NO与活性炭反应的化学方程式为___________ 。
②如果已知 ,则该反应正反应的
,则该反应正反应的
___________ 0(填“>”、“<”或“=”)。
③在 温度下反应达到平衡后,下列措施能增大NO的转化率的是
温度下反应达到平衡后,下列措施能增大NO的转化率的是___________ 。
a.降低温度 b.增大压强 c.增大 d.移去部分F
d.移去部分F
(3)汽车尾气处理中的反应有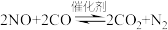 。某温度时,在1L密闭容器中充入0.1mol CO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率
。某温度时,在1L密闭容器中充入0.1mol CO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率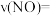
___________ 。此平衡体系中,CO、NO、 、
、 的物质的量比为
的物质的量比为___________ 。
(1)用
 催化还原
催化还原 消除氮氧化物污染的变化如下:
消除氮氧化物污染的变化如下: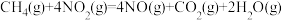
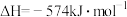

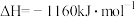
若用
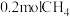 还原
还原 至
至 ,整个过程中放出的热量为
,整个过程中放出的热量为(2)活性炭(C)可处理大气污染物NO。在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F,当温度分别在
 和
和 时,测得各物质平衡时物质的量如下表:
时,测得各物质平衡时物质的量如下表:| 物质 n/mol T/℃ | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.100 | 0 | 0 |
 | 2.000 | 0.040 | 0.030 | 0.030 |
 | 2.005 | 0.050 | 0.025 | 0.025 |
②如果已知
 ,则该反应正反应的
,则该反应正反应的
③在
 温度下反应达到平衡后,下列措施能增大NO的转化率的是
温度下反应达到平衡后,下列措施能增大NO的转化率的是a.降低温度 b.增大压强 c.增大
 d.移去部分F
d.移去部分F(3)汽车尾气处理中的反应有
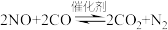 。某温度时,在1L密闭容器中充入0.1mol CO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率
。某温度时,在1L密闭容器中充入0.1mol CO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率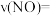
 、
、 的物质的量比为
的物质的量比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】在某一容积为5L的体积不变的密闭容器内,加入0.3mol的CO和0.3mol的 ,在催化剂存在和800℃的条件下,发生反应:
,在催化剂存在和800℃的条件下,发生反应:
 ,
, 的浓度随时间变化情况如图:
的浓度随时间变化情况如图:

(1)可以说明该反应已达平衡的是_______ (填序号)。
①体系内压强不再改变 ② 的浓度不再改变
的浓度不再改变
③容器内气体的密度不再改变 ④
⑤
(2)根据图上数据,该温度(800℃)下的平衡常数
_______ 。若保持温度和容器的体积不变,在上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后, 的转化率
的转化率_______ (填升高、降低或不变)。
(3)在体积不变的条件下,改变下列条件能增大平衡常数K的有_______ (填字母)。
A.升高温度 B.降低温度 C.增大压强 D.加入一氧化碳气体 E.加入催化剂
(4)在800℃下,改变其他条件,测得在某一时刻
 mol⋅L-1;
mol⋅L-1;
 mol⋅L-1,则此时正、逆反应速率的大小:
mol⋅L-1,则此时正、逆反应速率的大小:
_______ (填“>”“<”或“=”) 。
。
 ,在催化剂存在和800℃的条件下,发生反应:
,在催化剂存在和800℃的条件下,发生反应:
 ,
, 的浓度随时间变化情况如图:
的浓度随时间变化情况如图:
(1)可以说明该反应已达平衡的是
①体系内压强不再改变 ②
 的浓度不再改变
的浓度不再改变③容器内气体的密度不再改变 ④

⑤

(2)根据图上数据,该温度(800℃)下的平衡常数

 的转化率
的转化率(3)在体积不变的条件下,改变下列条件能增大平衡常数K的有
A.升高温度 B.降低温度 C.增大压强 D.加入一氧化碳气体 E.加入催化剂
(4)在800℃下,改变其他条件,测得在某一时刻
 mol⋅L-1;
mol⋅L-1; mol⋅L-1,则此时正、逆反应速率的大小:
mol⋅L-1,则此时正、逆反应速率的大小:
 。
。
您最近一年使用:0次
【推荐1】如图所示的过程是目前直接利用太阳能的研究热点。人们把通过人工光化学手段合成燃料的过程叫做人工光合作用。
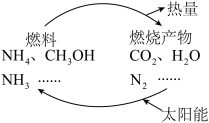
(1)在图构想的物质和能量循环中太阳能最终转化为___ 能;
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH(甲醇),该反应的化学方程式为:2CO2(g)+4H2O(g) 2CH3OH(g)+3O2(g)。
2CH3OH(g)+3O2(g)。
一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如表所示:
用CH3OH、H2O分别表示0~3min内该反应的平均反应速率为___ mol/(L·min)-1、____ mol/(L·min)-1;
②能说明该反应已达到平衡状态的是___ (填序号);
A.v正(H2O)=2v逆(CO2) B.n(CH3OH)∶n(O2)=2∶3
C.容器内压强保持不变 D.容器内混合气体密度保持不变
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的____ 极(填“正”或“负”),完成并配平通入氧气一极的电极反应式:___ 。

(1)在图构想的物质和能量循环中太阳能最终转化为
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH(甲醇),该反应的化学方程式为:2CO2(g)+4H2O(g)
 2CH3OH(g)+3O2(g)。
2CH3OH(g)+3O2(g)。一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如表所示:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
用CH3OH、H2O分别表示0~3min内该反应的平均反应速率为
②能说明该反应已达到平衡状态的是
A.v正(H2O)=2v逆(CO2) B.n(CH3OH)∶n(O2)=2∶3
C.容器内压强保持不变 D.容器内混合气体密度保持不变
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】下表中的数据是破坏1mol物质中的化学键所消耗的能量:
根据上述数据回答下列问题:
(1)下列物质中本身具有的能量最低的是_________ (填字母).
(2)下列氢化物中最稳定的是_________ (填字母)。
A.HCl B.HBr C.HI
(3) (X代表Cl、Br、I)的反应,反应物的总能量
(X代表Cl、Br、I)的反应,反应物的总能量_________ (填“高于”或“低于”)生成物的总能量。
(4)相同条件下,X2(X代表Cl、Br、I分别与氢气反应,当消耗1mol的氢气时,放出或吸收的热量最多是________ kJ(填数字)。
(5)恒温恒容下) (X代表Cl、Br、I)的反应,当X2是I2时,该反应是可逆反应,下列描述能表示该反应达平衡状态的是
(X代表Cl、Br、I)的反应,当X2是I2时,该反应是可逆反应,下列描述能表示该反应达平衡状态的是_____________ 。
A.容器内的混合气体的平均相对分子质量不再改变
B.容器内压强不再发生变化
C.
D.X的体积分数不再改变
E.生成1mol的氢气,同时消耗2molHX
F.断开1molH-H键,同时断开2molH-X键
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量/kJ | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
(1)下列物质中本身具有的能量最低的是
| A.H2 | B.Cl2 | C.Br2 | D.I2 |
A.HCl B.HBr C.HI
(3)
 (X代表Cl、Br、I)的反应,反应物的总能量
(X代表Cl、Br、I)的反应,反应物的总能量(4)相同条件下,X2(X代表Cl、Br、I分别与氢气反应,当消耗1mol的氢气时,放出或吸收的热量最多是
(5)恒温恒容下)
 (X代表Cl、Br、I)的反应,当X2是I2时,该反应是可逆反应,下列描述能表示该反应达平衡状态的是
(X代表Cl、Br、I)的反应,当X2是I2时,该反应是可逆反应,下列描述能表示该反应达平衡状态的是A.容器内的混合气体的平均相对分子质量不再改变
B.容器内压强不再发生变化
C.

D.X的体积分数不再改变
E.生成1mol的氢气,同时消耗2molHX
F.断开1molH-H键,同时断开2molH-X键
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】将一定量纯净的氨基甲酸铵( )固体置于密闭容器中(假设容器容积不变),在一定温度下使其达到分解平衡:
)固体置于密闭容器中(假设容器容积不变),在一定温度下使其达到分解平衡: (正反应为吸热反应)。回答下列问题:
(正反应为吸热反应)。回答下列问题:
(1)可以判断该分解反应已经达到化学平衡状态的是__________________ (填标号,双选)。
a. b.密闭容器中总压强不变
b.密闭容器中总压强不变
c.密闭容器中混合气体的密度不变 d.密闭容器中氨的体积分数不变
(2)当反应达到平衡状态时,其他条件不变,在容器中充入少量HCl气体,平衡将向____________ (填“正反应方向”或“逆反应方向”,下同)移动。当反应达到平衡状态时,其他条件不变,温度升高,平衡将向__________________________ 移动。
 )固体置于密闭容器中(假设容器容积不变),在一定温度下使其达到分解平衡:
)固体置于密闭容器中(假设容器容积不变),在一定温度下使其达到分解平衡: (正反应为吸热反应)。回答下列问题:
(正反应为吸热反应)。回答下列问题:(1)可以判断该分解反应已经达到化学平衡状态的是
a.
 b.密闭容器中总压强不变
b.密闭容器中总压强不变c.密闭容器中混合气体的密度不变 d.密闭容器中氨的体积分数不变
(2)当反应达到平衡状态时,其他条件不变,在容器中充入少量HCl气体,平衡将向
您最近一年使用:0次



