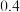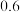下列溶液中各微粒的浓度关系不正确的是
A.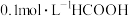 溶液中: 溶液中: |
B. 的溶液中: 的溶液中:  |
C. 溶液中: 溶液中: |
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液显碱性: 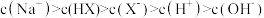 |
更新时间:2023-03-02 23:04:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,分别向浓度均为0.1 mol/L,体积均为20 mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的c(H+)与加入氨水的体积变化关系如图所示。下列说法正确的是
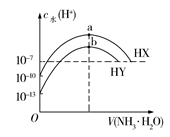

A.HX的电离方程式为HX H++X− H++X− |
B.b点时溶液中c( )=c(Y−)>c(H+)=c(OH−) )=c(Y−)>c(H+)=c(OH−) |
| C.HX的电离平衡常数约为1×10−7 mol/L |
| D.a、b两点对应溶液中存在的微粒种类数目相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液里-lgc(Cu2+)与Na2S溶液体积[V(Na2S)]的关系如图所示。已知:Ksp(ZnS)=3.0×10-25,下列有关说法正确的是


| A.a、b、c三点中,水的电离程度最大的为b点 |
| B.该温度下Ksp(CuS)=1.0×10-18 |
C.该温度下反应:ZnS(s)+Cu2+(aq) CuS(s)+Zn2+(aq)的平衡常数为3.33×10-11 CuS(s)+Zn2+(aq)的平衡常数为3.33×10-11 |
| D.如果忽略CuS的溶解,则c点溶液有:2[c(S2-)+c(HS-)+c(H2S)]=c(Cl-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】 时,某二元酸
时,某二元酸 的
的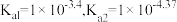 。
。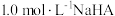 溶液稀释过程中
溶液稀释过程中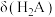 、
、 、
、 与
与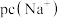 的关系如图。已知:
的关系如图。已知: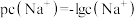 ,
, 表示微粒的分布分数,如
表示微粒的分布分数,如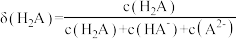 ,a、b两点坐标分别为
,a、b两点坐标分别为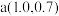 、
、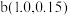 。下列说法错误的是
。下列说法错误的是

 时,某二元酸
时,某二元酸 的
的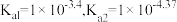 。
。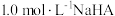 溶液稀释过程中
溶液稀释过程中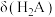 、
、 、
、 与
与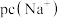 的关系如图。已知:
的关系如图。已知: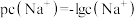 ,
, 表示微粒的分布分数,如
表示微粒的分布分数,如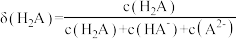 ,a、b两点坐标分别为
,a、b两点坐标分别为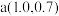 、
、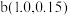 。下列说法错误的是
。下列说法错误的是
A.曲线X为 的变化曲线 的变化曲线 | B.a点: |
C.b点: | D.c点: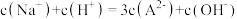 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】草酸(H2C2O4)是一种二元弱酸,在菠菜、苋菜、甜菜等植物中含量较高。25℃时,向H2C2O4溶液中滴加NaOH溶液,混合溶液中lgX [X表示 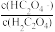 或
或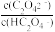 随pH的变化关系如图所示。下列说法不正确的是
随pH的变化关系如图所示。下列说法不正确的是
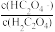 或
或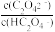 随pH的变化关系如图所示。下列说法不正确的是
随pH的变化关系如图所示。下列说法不正确的是 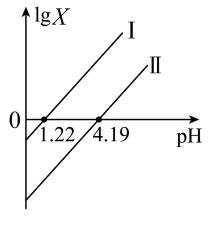
A.直线I中X表示的是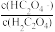 |
| B.直线I、Ⅱ的斜率均为1 |
| C.0.1mol/ L NaHC2O4溶液中:c(Na+)>c(HC2O4-)> c(C2O42-)> c(H2C2O4) |
| D.已知:25℃时,NH3·H2O的电离常数为10-4.69,则(NH4)2C2O4溶液呈碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,在20 mL 0.1 mol·L-1NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确 的是


| A.在A点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B.在B点:c(OH-)=c(H+),c(Na+)=c(CH3COO-) |
| C.在C点:c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| D.在C点:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
您最近一年使用:0次

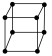 ,其配位数为8
,其配位数为8 分子中,S原子的价层电子对数为3,中心原子上孤电子对数为1,S原子为
分子中,S原子的价层电子对数为3,中心原子上孤电子对数为1,S原子为 杂化,是直线型分子
杂化,是直线型分子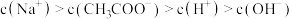
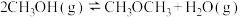 ,某温度下的平衡常数为400,此温度下,在恒容密闭容器中加入一定量
,某温度下的平衡常数为400,此温度下,在恒容密闭容器中加入一定量 ,某时刻测得各组分浓度如表,则此时正、逆反应速率的大小关系为:
,某时刻测得各组分浓度如表,则此时正、逆反应速率的大小关系为: