某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液里-lgc(Cu2+)与Na2S溶液体积[V(Na2S)]的关系如图所示。已知:Ksp(ZnS)=3.0×10-25,下列有关说法正确的是


| A.a、b、c三点中,水的电离程度最大的为b点 |
| B.该温度下Ksp(CuS)=1.0×10-18 |
C.该温度下反应:ZnS(s)+Cu2+(aq) CuS(s)+Zn2+(aq)的平衡常数为3.33×10-11 CuS(s)+Zn2+(aq)的平衡常数为3.33×10-11 |
| D.如果忽略CuS的溶解,则c点溶液有:2[c(S2-)+c(HS-)+c(H2S)]=c(Cl-) |
2022·四川泸州·一模 查看更多[3]
四川省泸县第二中学、泸县二中实验学校2022届高三上学期一诊模拟考试理综化学试题(已下线)易错点26 沉淀溶解平衡-备战2023年高考化学考试易错题安徽省合肥市第六中学2022-2023学年高二下学期3月段考化学试题
更新时间:2022-07-06 18:26:47
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】 是一种二元弱酸,
是一种二元弱酸, 溶液中各型体浓度在其总浓度中所占比值叫其分布系数,常温下某浓度的
溶液中各型体浓度在其总浓度中所占比值叫其分布系数,常温下某浓度的 溶液中各型体分布系数随pH的变化如图所示,据此分析,下列说法不正确的是
溶液中各型体分布系数随pH的变化如图所示,据此分析,下列说法不正确的是

 是一种二元弱酸,
是一种二元弱酸, 溶液中各型体浓度在其总浓度中所占比值叫其分布系数,常温下某浓度的
溶液中各型体浓度在其总浓度中所占比值叫其分布系数,常温下某浓度的 溶液中各型体分布系数随pH的变化如图所示,据此分析,下列说法不正确的是
溶液中各型体分布系数随pH的变化如图所示,据此分析,下列说法不正确的是
A.曲线a代表 ,曲线b代表 ,曲线b代表 |
B.常温下0.1mol/L的 溶液显酸性 溶液显酸性 |
C.常温下, 的电离平衡常数 的电离平衡常数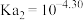 |
D. 从1.30至4.30时, 从1.30至4.30时, 先增大后减小 先增大后减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在0.1 mol·L-1的Na2CO3溶液中,下列关系正确的是
A.c(Na+)=2c(CO ) ) | B.c(OH-)=2c(H+) |
C.c(HCO )>c(H2CO3) )>c(H2CO3) | D.c(Na+)<c(CO )+c(HCO )+c(HCO ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】H2R为二元弱酸,向一定体积的0.1mol/L的H2R溶液中逐滴加入一定浓度的NaOH溶液,溶液中不同形态的粒子(H2R、HR-、R2-)的物质的量分数a(X)随pH的变化曲线如图所示[a(X)=c(X)/[c(H2R)+c(HR-)+c(R2-)]]。下列说法错误的是


| A.常温下,K2(H2R)=1.0×10-11 |
| B.常温下,HR-在水中的电离程度大于其水解程度 |
| C.pH=9时, c(Na+)>c(HR-)+2c(R2-) |
| D.pH=7时,c(H2R)=c(HR-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】以硫铁矿为原料生产硫酸所得的酸性废水中砷元表含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表,若混合溶液中Ca2+、Al3+、Fe3+的浓度均为1.0×10-3 mol•L-1,c(AsO43-)最大是
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×l0-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| A.5.7×10-18 mol•L-1 | B.2.6×10-5 mol•L-1 |
| C.1.6×10-13 mol•L-1 | D.5.7×10-24 mol•L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】溶液中除铁时还常用NaClO3作氧化剂,在较小的pH条件下最终生成一种浅黄色的黄铁矾钠[Na2Fe6(SO4)4(OH)12]沉淀除去。如图是温度-pH与生成的沉淀关系图,图中阴影部分是黄铁矾稳定存在的区域。下列说法不正确的是( ){已知25℃,Ksp[Fe(OH)3]=2.64×10-39}


| A.在25℃时溶液经氧化,调节溶液pH=4,此时溶液中c(Fe3+)=2.64×10-9mol·L-1 |
| B.用氯酸钠在酸性条件下氧化Fe2+离子方程式为:6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O |
| C.pH=6,温度从80℃升高至150℃体系得到的沉淀被氧化 |
| D.工业生产黄铁矾钠,温度控制在85~95℃pH=1.5左右 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】向3mol/L的FeCl3溶液中滴入氢氧化钠溶液,当Fe3+恰好完全沉淀[c(Fe3+)≤10-5mol/L],测得pH=1.5,则常温下 =_____(
=_____( 表示氢氧化铁溶度积常数的负对数)
表示氢氧化铁溶度积常数的负对数)
 =_____(
=_____( 表示氢氧化铁溶度积常数的负对数)
表示氢氧化铁溶度积常数的负对数)| A.37.5 | B.9.5 | C.42.5 | D.47.5 |
您最近一年使用:0次
【推荐2】常温时, 的溶度积
的溶度积 ,
, 在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是
在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是


 的溶度积
的溶度积 ,
, 在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是
在水中的沉淀溶解平衡曲线如图所示.下列有关推断正确的是

A.常温时, 在 在 溶液中的 溶液中的 比在水中的小 比在水中的小 |
B.常温时, 的溶度积 的溶度积 |
C.向含等浓度 、 、 的混合溶液中滴加 的混合溶液中滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
D.向Y点溶液中加入 溶液,可使Y点移到Z点 溶液,可使Y点移到Z点 |
您最近一年使用:0次

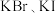 混合溶液中依次加入少量氯水和
混合溶液中依次加入少量氯水和 振荡,静置
振荡,静置
 元素
元素 溶液②
溶液② 溶液
溶液 酸性弱于
酸性弱于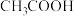
 沉淀的试管中加入适量饱和
沉淀的试管中加入适量饱和 溶液,振荡
溶液,振荡 结合
结合 使
使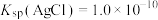 ,
, ,现有等体积的AgCl和AgI的饱和溶液的清液。下列说法错误的是
,现有等体积的AgCl和AgI的饱和溶液的清液。下列说法错误的是 固体,则溶液中
固体,则溶液中 增大,
增大,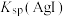 不变
不变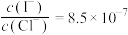
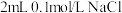 溶液中滴加2滴
溶液中滴加2滴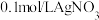 溶液,产生白色沉淀;再向其中滴加4滴
溶液,产生白色沉淀;再向其中滴加4滴 的KI溶液,有黄色沉淀产生,则可验证
的KI溶液,有黄色沉淀产生,则可验证


